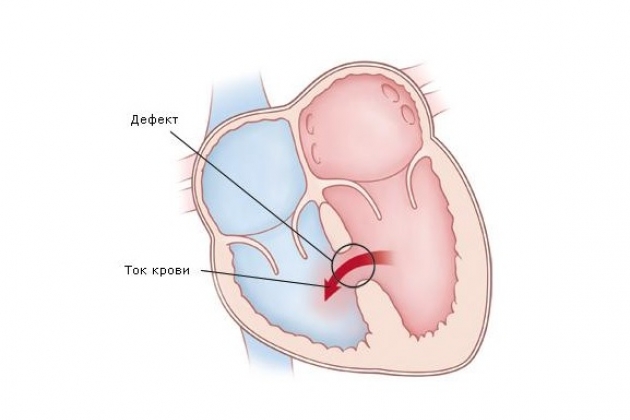
Врожденный дефект межжелудочковой перегородки
В 1879 г. Roger впервые описал клинические признаки небольшого дефекта межжелудочковой перегородки. В 1897 г. Eisenmenger опубликовал посмертные находки у синего больного, умершего в возрасте 32 года: большой ДМЖП и смещенную вправо аорту. С младенческого возраста у пациента имели место цианоз и одышка, выслушивались шумы недостаточности трехстворчатого и легочного клапанов. На аутопсии были обнаружены гипертрофия и дилатация правого желудочка, расширенное кольцо трехстворчатого клапана, большой ДМЖП со смещенной аортой, атеросклероз легочных артерий и геморрагический инфаркт легких вследствие тромбоза легочной артерии. Abbott писала, что первое упоминание об этом пороке появилось в 1847 г. в публикации Dalrymple, однако она ввела термин комплекс Eisenmenger. Это наименование применяется для обозначения стадии естественного течения большого ДМЖП с высоким сопротивлением легочных сосудов и преимущественно право-левым шунтом.
Частота
Изолированный ДМЖП является самым частым ВПС, если исключить двустворчатый аортальный клапан, и составляет 20% всех врожденных аномалий у детей, родившихся живыми; 1,5 – 3,5 случая на 1000 родившихся в срок и 4,5 – 7 – на 1000 родившихся раньше срока. Меньшая частота этого порока среди взрослых с ВПС вызвана главным образом спонтанным закрытием многих дефектов. Дефект межжелудочковой перегородки чаще диагностируется у лиц женского пола – в 56% случаев против 44% у лиц мужского пола. Дефект межжелудочковой перегородки является наиболее частым пороком при большинстве хромосомных синдромов:
-
трисомии 13;
-
трисомии 18;
-
трисомии 21.
В большинстве случаев дефект не сочетается с хромосомными аномалиями. Этиология порока является мультифакторной. Причинами могут служить как наследственная предрасположенность, так и влияние факторов внешней среды.
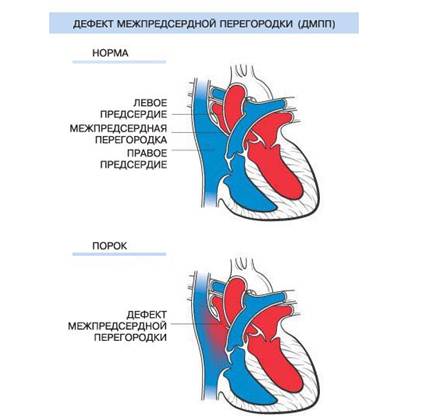
Эмбриология
Межжелудочковая перегородка начинает формироваться в конце 4-й недели внутриутробного развития. Нормальное закрытие межжелудочковой перегородки происходит благодаря трем конкурирующим механизмам:
-
росту конотрункусного гребня книзу, что формирует перегородку тракта оттока;
-
росту эндокардиальных подушечек, в результате чего образуется приточная перегородка;
-
росту мышечной перегородки, которая формирует апикальную и среднемышечную части перегородки.
Если к 7-8-й неделе гестации слияние этих образований неполное, остается отверстие, через которое сообщаются полости желудочков. Если же процесс слияния первичной перегородки с аортолегочной перегородкой, разделяющей магистральные сосуды, будет прерван, образуется дефект конусной части межжелудочковой перегородки или перимембранозный дефект. Неполное слияние эндокардиальных отростков с первичной межжелудочковой перегородкой приводит к формированию дефекта приточной части межжелудочковой перегородки под перегородочной створкой трехстворчатого клапана. Нарушение формирования самой первичной перегородки приводит к образованию дефекта в области мышечной части межжелудочковой перегородки, чаще всего в области верхушки сердца. Специалисты считают, что эти дефекты являются следствием нарушения эмбрионального процесса уплотнения первичного губчатого миокарда в области мышечной перегородки у верхушки.
На формирование ДМЖП влияют хромосомные, наследственные и географические факторы. Некоторые исследователи обнаружили связь дефектов конусной перегородки с микроделециями в хромосоме 22q11.2. С этой же причиной связывают образование перимембранозных ДМЖП. У детей родителей с ДМЖП наблюдается большая частота формирования ВПС, однако это могут быть необязательно ДМЖП.
Анатомия
Размеры дефектов варьируют от минимальных, гемодинамически не значимых, до крупных, конкурирующих по размерам с устьем аорты. По предложению Rowe, размеры межжелудочковых дефектов сравнивают с диаметром корня аорты. Если соотношение диаметра ДМЖП и диаметра корня аорты >0,8, дефект считают большим, если диаметр ДМЖП составляет 1/2 диаметра аорты – средним, меньше 1/4 диаметра аорты – малым.
В большинстве случаев дефект является простым отверстием в межжелудочковой перегородке. Реже дефект обусловлен тем, что первичная и инфундибулярная перегородки расположены в разных плоскостях, они не соосны и поэтому не сращены. Конусная перегородка может отклоняться кпереди в сторону правого желудочка или кзади, в сторону левого желудочка. Перегородка отклоняется влево или вправо, как дверь на фиксированных петлях. Наиболее часто встречается отклонение инфундибулярной перегородки кпереди. В этих случаях она отклоняется в сторону выводного тракта правого желудочка, что приводит к образованию большого ДМЖП и нависанию аорты над первичной перегородкой. Этот тип дефекта характерен для комплекса Eisenmenger. При выраженном вторжении конусной перегородки в выводной тракт правого желудочка создается анатомия тетрады Фалло. При отклонении конусной перегородки кзади в выводной тракт левого желудочка на "шарнире", крепящемся вдоль аортального клапана, образуются ДМЖП и мышечный субаортальный стеноз. При выраженном отклонении инфундибулярной перегородки влево клапан легочной артерии может нависать над межжелудочковой перегородкой. Задний несоосный дефект часто сочетается с обструктивной патологией дуги аорты; он получил наименование дефекта коарктационного типа. Такой дефект часто наблюдается у больных с перерывом дуги аорты. Несоосность между предсердной и мышечной межжелудочковой перегородками является причиной нависающих AV- клапанов и клапанов-наездников.
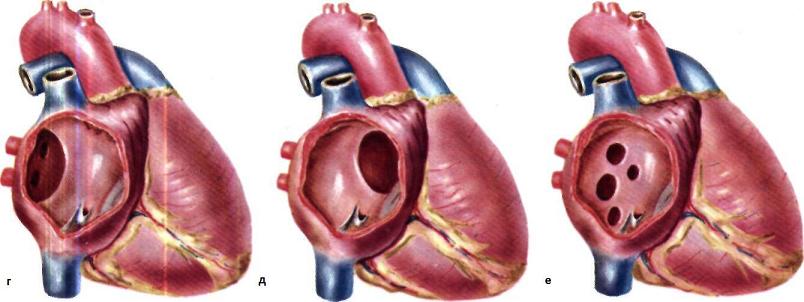
Классификация ДМЖП основана на локализации дефектов. Наиболее исчерпывающая классификация была опубликована Soto и соавторами.
Межжелудочковую перегородку подразделяют на 4 части:
-
приточную часть, отделяющую митральный и трехстворчатый клапаны;
-
трабекулярную перегородку, которая простирается от места прикрепления папиллярных мышц трехстворчатого клапана книзу до верхушки и кверху до наджелудочкового гребня;
-
гладкостенную выводную, или инфундибулярную, перегородку, которая находится между наджелудочковым гребнем и легочным клапаном;
-
относительно небольшую мембранозную перегородку, которая обычно разделена на две части перегородочной створкой трехстворчатого клапана.
Наиболее частым дефектом является перимембранозный. Он располагается в выводном тракте левого желудочка непосредственно под аортальным клапаном и обычно простирается в прилежащие мышечную, приточную и выводную область. Со стороны правого желудочка дефект лежит под наджелудочковым гребнем и кзади от папиллярной мышцы конуса. Дефекты межжелудочковой перегородки этой области часто вовлекают прилежащие отделы мышечной перегородки, поэтому их называют перимембранозными – перимембранозными приточными, перимембранозными трабекулярными, перимембранозными инфундибулярными.
В связи с наличием лево-правого сброса развиваются вторичные приобретенные аномалии трехстворчатого клапана в виде избыточных тканей перегородочной створки или мешочков, которые могут частично или полностью закрыть дефект. Эти мешочки раньше называли «аневризмами межжелудочковой перегородки» и связывали с возможностью спонтанного закрытия дефекта. При перимембранозном дефекте инфундибулярная перегородка иногда смещена кпереди, и в результате нарушения соосности между инфундибулярной и передней межжелудочковой перегородкой аортальный клапан нависает над дефектом. Смещение конусной перегородки кзади или влево приводит к образованию субаортального стеноза. В случаях, когда имеется дефицит перегородочной комиссуры трехстворчатого клапана в месте ее прикрепления к атриовентрикулярной мембранозной перегородке, происходит лево-правый сброс крови из левого желудочка в правое предсердие. При таких дефектах шунт крови происходит на желудочковом и предсердном уровнях. Изредка встречается изолированный дефект между левым желудочком и правым предсердием. При таких дефектах имеют место аномалии трехстворчатого клапана в виде перфорации, деформации, расщепления, диастаза комиссуры.
В период эмбриогенеза закрытие межжелудочкового отверстия зависит от трех факторов: роста соединительной ткани на гребне мышечной перегородки; роста гребней, разделяющих конус и артериальный трункус; прорастания в AV-канал правосторонних подушечек. Благодаря множеству механизмов, принимающих участие в закрытии мембранозной перегородки, дефект образуется чаще всего именно в этом месте.
Дефекты, расположенные в выводном тракте правого желудочка ниже легочного клапана, называют надгребешковыми, инфундибулярными, конусными, подлегочными или субартериальными дефектами с двойной связью с аортальным и легочным клапанами. Эти дефекты в западных популяциях встречаются у 5-7% больных с ВПС, за исключением Японии и других дальневосточных стран, где такая локализация встречается гораздо чаще – почти у 30% пациентов.
У пациентов с подлегочными дефектами конуса часто отсутствует мышечная или фиброзная опора аортального клапана, что приводит к грыжевидному выпячиванию правой аортальной створки в ДМЖП. Провисание обусловлено не только отсутствием опорной стромы прилежащих створок, но и инжекционным присасывающим эффектом струи крови. Выпадающая створка может создать градиент давления в выводном тракте правого желудчка. Аортальные комиссуры обычно нормальные. У больных с перимембранозным межжелудочковым дефектом и аортальной недостаточностью пролабируют правая и/или некоронарная створки, аортальные комиссуры часто аномальные, нередко имеет место инфундибулярный стеноз легочной артерии. Пролабирующая аортальная створка частично закрывает небольшой дефект перегородки, препятствуя лево-правому шунтированию. Частота аортальной недостаточности при субартериальных дефектах увеличивается с 5% в возрасте младше 3 лет до 50% к 13-15 годам.
Аортальная недостаточность не всегда связана с пролабированием створок и может быть обусловлена двустворчатым клапаном.
Приточные дефекты, которые расположены кзади и книзу от мембранозных дефектов под перегородочной створкой трехстворчатого клапана и ниже папиллярной мышцы конуса, ранее называли атриовентрикулярными септальными дефектами. Однако в данном случае это наименование нельзя признать правильным, так как эти дефекты обычно не сопровождаются аномалиями митрального и трехстворчатого клапанов и общий атриовентрикулярный пучок Гиса не проходит ниже дефекта, как при истинном АВСД. Приточные дефекты встречаются в 5-8% случаев.
Дефекты в мышечной перегородке нередко бывают множественными и встречаются с частотой 5-20%. Мышечные дефекты подразделяют на верхушечные, центральные и краевые, или передние. Верхушечные дефекты встречаются чаще остальных. Они плохо видны со стороны правого желудочка, поскольку обычно окружены и покрыты трабекулами, образующими извитые каналы. Со стороны левого желудочка трабекул мало и множественные отверстия часто соединяются и приобретают вид одного дефекта. Иногда верхушечные дефекты имеют большие размеры.
Другим вариантом мышечных дефектов являются центральные дефекты, расположенные позади перегородочно-краевой трабекулы и в средней части перегородки. Обычно они частично прикрыты трабекулами и могут создавать впечатление множественных дефектов. Со стороны левого желудочка такой дефект выглядит единичным, имеет округлую форму и расположен вдали от верхушки, передней и задней стенок левого желудочка.
Маленькие мышечные дефекты в области соединения перегородки и свободной стенки называют краевыми, или передними, дефектами. Они обычно множественные, мелкие, извитые и выстроены вдоль края перегородки. Множественные мышечные дефекты могут создавать решетчатость перегородки, образно называемой «швейцарским сыром». Эти ДМЖП типа швейцарского сыра крайне трудны для хирургического закрытия. Взаимоотношения атриовентрикулярных проводящих путей с ДМЖП очень важны с хирургической точки зрения. При перимембранозном дефекте пучок Гиса проходит субэндокардиально по задненижнему краю дефекта. При приточных дефектах пучок Гиса огибает дефект спереди и сверху. Мышечные и субартериальные дефекты располагаются вдали от пучка Гиса, если они не простираются в перимембранозную область.
Блокада правой ножки пучка Гиса возникает часто после закрытия ДМЖП и, вероятно, связана с вентрикулотомией или прямым повреждением правой ножки, которая проходит вдоль задненижнего края перимембранозного дефекта. Блокада правой ножки возникает в 60% случаев при закрытии мышечных дефектов через поперечную вентрикулотомию и в 44% – при закрытии перимембранозных дефектов доступом через правое предсердие. При вертикальной вентрикулотомии частота блокады правой ножки увеличивается до 80%. Предполагается, что блокада правой ножки связана с пересечением дистальной ветви правой ножки, а не с повреждением разветвлений Пуркинье.
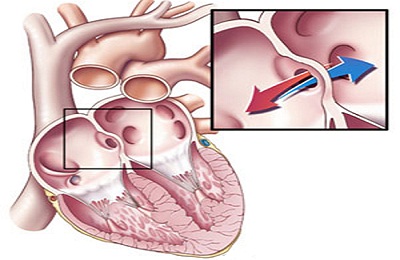
Гемодинамика
Выраженность гемодинамических нарушений зависит от разметов дефекта. При малых и средних размерах дефект ограничивает сброс крови слева направо. Большие дефекты, приблизительно равные размеру устью аорты, не оказывают существенного сопротивления току крови через дефект. Его объем определяется соотношением сопротивлений сосудов системного и легочного кругов кровообращения.
Влияние ЛСС на структуру и функцию сердечно-сосудистой системы
После рождения фетальные резистивные мышечные легочные артерии малого просвета с утолщенным мышечным слоем в течение 7-10 дней приобретают структуру взрослого типа – стенка артерий истончается, а их просвет увеличивается. Одновременно с морфологическими изменениями снижается ЛСС. При наличии больших дефектов этот процесс отсрочен и увеличенное легочное сопротивление служит защитным механизмом против чрезмерного увеличения легочного кровотока. Повышение давление в левом предсердии играет важную роль в поддержании фазы легочной вазоконстрикции.
Когда легочные сосуды вытягиваются и достигают границ окружающих их фиброзных футляров, кривая давление-кровоток становится линейной, поэтому дальнейшее увеличение кровотока сопровождается повреждением сосудов, которое может индуцировать воспалительный артериит. Хроническая баротравма и напряжение сдвига приводят к утолщению адвентиции, гипертрофии среднего мышечного слоя и повреждению интимы.
У больных с большими дефектами физиологическое снижение ЛСС происходит в течение первых нескольких месяцев жизни, что приводит к увеличению лево-правого сброса крови. Чрезмерный легочный кровоток сдерживается легочной венозной и левопредсердной гипертензией, возникающими вследствие объемной перегорузки левого желудочка. Левое предсердие и желудочек заметно расширяются. При выраженной перегрузке левых отделов сердца развивается застойная сердечная недостаточность в возрасте 2-8 нед. Компенсаторными механизмами, которые позволяют младенцу адаптироваться к объемной перегрузке, являются эффект Frank-Starling, увеличенная симпатическая стимуляция сердца и гипертрофия миокарда. Скорость развития гипертрофии является одним из ведущих факторов способности ребенка адекватно компенсировать ДМЖП с большим лево-правым шунтом.
При умеренно повышенном ЛСС и большом сбросе артериальной крови систолическое давление в легочной артерии и аорте равны. Реакция легочных сосудов на гиперволемию различна. У некоторых пациентов сопротивление повышается незначительно и большой объем легочного кровотока остается стабильным. У других легочные сосуды расширяются и удлиняются, мышечный средний слой стенок легочной артерии гипертрофируется, увеличивается тонус резистивных сосудов, постепенно развиваются склеротические изменения интимы. Эти изменения обычно наблюдаются только при больших дефектах, когда выброс в легочную артерию осуществляют оба желудочка. Гемодинамическими и клиническими последствиями повышения ЛСС являются снижение объема легочного кровотока, уменьшение диастолической перегрузки левых отделов сердца, постепенное уменьшение размеров левого предсердия и левого желудочка и уменьшение мышечной массы левого желудочка. Когда ЛСС превысит таковое в системном бассейне, давление в обоих кругах кровообращения остается равным, но направление сброса крови изменяется преимущественно на право-левое. Эту стадию легочной гипертензии называют синдромом Eisenmenger. У некоторых больных сопротивление легочных артерий после рождения никогда не снижается, т.е. сохраняется плодный тип строения легочных артерий. На протяжении всего младенческого периода у них высокое ЛСС, сбалансированный сброс, почти нормальные размер левого желудочка и масса миокарда. У этих пациентов нет признаков левожелудочковой декомпенсации ни в младенческом, ни в детском возрасте. Последняя стадия синдрома Eisenmenger одинакова в обеих группах. Иногда развивается декомпенсация правого желудочка, обычно в 3-й и 4-й декадах жизни.
Характер рабочей нагрузки на правый желудочек зависит от соотношения величины ЛСС и величины лево-правого сброса. При небольших дефектах систолическое давление в правом желудочке, объемная нагрузка и толщина стенки остаются нормальными. При средних размерах дефектов соотношение объема сброса и ЛСС таково, что давление в легочной артерии умеренно повышено и работа правого желудочка увеличена в основном за счет объемной нагрузки. Гипертрофия желудочка пропорциональна степени повышения давления. Большие дефекты создают систолическую перегрузку правого желудочка, связанную с преодолением высокого ЛСС. Прогрессирует гипертрофия правого желудочка. При больших дефектах происходит диастолическое шунтирование слева направо через дефект, которое сопровождается расширением полости правого желудочка, менее выраженным, чем расширение левого желудочка.
Варианты физиологических состояний
Небольшой дефект с низким ЛСС
Небольшие дефекты оказывают большое сопротивление току крови с выраженным систолическим градиентом давления между желудочками, с малым объемом лево-правого сброса и практически нормальной работой желудочков. Объем сброса крови прямо связан с размером дефекта, и отсутствует тенденция к повышению ЛСС. Благодаря наличию градиента давления в систолу и диастолу шунтирование крови происходит в течение всего сердечного цикла. Сокращение предсердий усиливает диастолический переток крови слева направо. Начало систолы желудочков характеризуется более ранним повышением давления в левом желудочке, чем в правом. Поэтому шунтирование крови начинается в фазу изометрического сокращения. Наибольшие градиент и сброс крови отмечаются в фазу выброса. После закрытия полулунных клапанов во время изоволемического расслабления также происходит сброс крови. В конце изоволемического расслабления во время короткого интервала ранней диастолы, когда давление в левом желудочке падает ниже уровня давления в правом желудочке, лево-правый сброс временно прекращается, а реверсия шунта в этот момент не происходит.
Фонокардиографические исследования показывают, что при большом градиенте давления между желудочками в течение всей систолы определяется голосистолический шум. Диастолический шум отсутствует, несмотря на переток крови через дефект. Это объясняется недостаточной турбулентностью крови из-за малого количества шунтируемой крови.
Дефект средних размеров с вариабельным ЛСС
Дефекты средних размеров оказывают меньшее сопротивление шунтовому току, однако достаточно малы для беспрепятственного лево-правого сброса крови. Величина дефекта обычно меньше или равна половине диаметра аорты, и систолическое давление в правом желудочке достигает 70-85% системного давлению. Легочно-сосудистое сопротивление обычно не повышено. Большой объем шунта крови создает объемную перегрузку левого предсердия и желудочка и приводит к гипертрофии поледнего. Систолическая работа и мышечная масса правого желудочка увеличены незначительно, так как в диастолу желудочек наполняется нормальным количеством крови из полых вен. Во время систолы давление в левом желудочке возрастает быстрее, чем в правом, и градиент давления остается в течение всей систолы и в начальный период изоволемического расслабления. Давление в левом желудочке падает быстрее, чем в правом, поэтому во время релаксации возникает положительный право-левый градиент и венозный сброс в выводной отдел левого желудочка. С началом диастолы перепад давления на межжелудочковой перегородке способствует сбросу крови из левого желудочка в правый. Небольшой объем крови, которая шунтировалась справа налево во время изоволемической релаксации, возвращается в правый желудочек и не поступает в системное кровообращение.
У младенцев, несмотря на рестриктивный дефект, объем шунтового тока относительно большой. Если дефект отстает в росте относительно массы тела, абсолютный объем шунта становится менее значительным.
Большой дефект с умеренным повышением ЛСС
Дефект считается большим, когда его размеры сравнимы с размерами устья аорты. Поскольку дефект не оказывает сопротивления перетоку крови, легочное кровообращение генерируется обоими желудочками. Объем и направление сброса крови определяются соотношением сосудистых сопротивлений малого и большого кругов кровообращения. Кровь шунтируется слева направо также в фазу диастолы, усиливаясь сокращением предсердий. В начале систолы давление в левом желудочке повышается раньше, чем в правом, способствуя перетоку крови через дефект до открытия аортального клапана. Период раннего выброса характеризуется наличием градиента давления на перегородке и шунта через дефект в выходной тракт правого желудочка. Во время позднего периода сердечного выброса давление в правом желудочке превышает таковое в левом. В этот момент сброс крови прекращается. В некоторых случаях возникает право-левый сброс в аорту, когда давление в левом желудочке падает ниже, чем в легочной артерии и аорте. В период релаксации давление в левом желудочке падает быстрее и раньше, чем в правом. Возникают право-левый градиент давления и шунтирование крови из правого желудочка в левый. Венозная кровь подмешивается к артериальной в верхней части левого желудочка и остается там, несмотря на диастолический лево-правый сброс, поэтому в фазу изгнания небольшая часть смешанной крови изгоняется в аорту.
Большой дефект с выраженным повышением ЛСС
В этой ситуации объемная нагрузка левого желудочка нормальная. Шунтирование через дефект обычно справа налево. В диастолу и раннюю систолу сброс крови реверсный. Во время раннего изгнания имеет место очень небольшой сброс крови слева направо. В поздней систоле происходит сброс крови справа налево из правого желудочка в аорту, который продолжается в течение раннего периода релаксации. Шум, генерируемый током крови через дефект во время раннего периода выброса, минимален, а в период право-левого шунтирования он отсутствует.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания









Комментарии