Травма центральной нервной системы. Травма спинного мозга
На травму ЦНС приходится почти половина всех смертей от травмы при анализе смертности в популяции или после поступления в травмоцентр. Кроме того, каждый год более 90000 американцев становятся инвалидами после ЧМТ и от 8000 до 10000 после травмы шейного отдела спинного мозга. Как и при геморрагическом шоке, травма ЦНС состоит из первичного повреждения, при котором ткань повреждается механическим воздействием, и вторичного повреждения, при котором ведущую роль играет реакция организма на повреждение. Смягчение вторичного повреждения зависит от своевременной диагностики и ранней целенаправленной терапии. Хотя не существует иных путей минимизации первичного повреждения ЦНС, кроме стратегии профилактики, вторичное повреждение сопровождается большим количеством смертей и инвалидностей, чем первичная травма. Первичное ведение таких пациентов может достоверно влиять на исход. Внимание к подходу ABCDE имеет первостепенное значение в первичной реанимации, и анестезиолог при травме должен быть теснейшим образом вовлечен в этот процесс. Интенсивное лечение пациентов с ЧМТ описывается в другом разделе данной книги. В данной части описывается короткая дискуссия раннего ведения данных пациентов.
Травму вызывают поперечные силы, которые приводят к первичному повреждению тел нейронов и аксонов и сосудистой сети. Патофизиология вторичного повреждения включает в себя метаболическую недостаточность, оксидативный стресс и каскад биохимических и молекулярных явлений, приводящих к одновременной отсроченной гибели клеток через некроз и апоптоз. Вторичное повреждение нередко усугубляется тканевой гипоксией/ ишемией и воспалительным ответом, и на результаты исхода ЧМТ влияет множество взаимодействующих факторов. Индивидуальные лекарства, такие как поглотители свободных радикалов, противовоспалительные агенты и блокаторы ионных каналов, были эффективны у животных, но не повлияли или имели неутешительные результаты в испытаниях на человеке.
У пациентов с легкой ЧМТ, достигающих стабильного показателя по ШКГ в течение 24 ч. после повреждения, вероятность ухудшения в дальнейшем низка, хотя у них есть опасность развития ряда «посттравматических» явлений, включая:
-
головную боль;
-
потерю памяти;
-
эмоциональную лабильность;
-
расстройства сна.
ЧМТ средней степени тяжести может сопровождаться формированием внутричерепного объема, требующего хирургического удаления, следовательно, у таких пациентов будет показана ранняя КТ. При лечении пациентов с ЧМТ средней степени тяжести могут потребоваться ранняя интубация, механическая вентиляция и тщательное обследование в силу агрессивного и возбужденного поведения и потенциально катастрофических последствий респираторной депрессии или легочной аспирации, возникающих во время диагностического поиска. Экстубация трахеи может быть предпринята, если пациент гемодинамически стабилен и отвечает на вопросы. Лечение вторичного повреждения достигается ранней коррекцией и последующей профилактикой гипоксии, немедленной инфузией и коррекцией сопутствующих повреждений. Время проведения операций за пределами черепа при наличии показаний у подобных пациентов весьма дискутабельно, так как раннее хирургическое вмешательство ассоциируется с увеличением эпизодов гипоксии и гипотензии. Несмотря на это, ряд исследований демонстрировали снижение неврологических последствий после ранних операций, другие же показали увеличение частоты легочных и септических осложнений при задержке ортопедических операций и операций на мягких тканях. Последние обзоры касательно времени оперативного вмешательства не приводят достаточных доказательств повышения риска ранних операций, хотя окончательные проспективные исследования еще не опубликованы.
Неврологический мониторинг пациента с ЧМТ средней степени тяжести состоит из серии манипуляций по оценке сознания и моторной и сенсорной функций. Ухудшение показателей по ШКГ является показанием для немедленной компьютерной томографии с целью выяснения показаний для краниотомии или инвазивного мониторинга внутричерепного давления. Если частый неврологический мониторинг невозможен в силу длительности общей анестезии и потребности в агрессивной аналгезии или профилактике делирия, будет показан инвазивный мониторинг ВЧД. Хотя летальность при ЧМТ средней степени тяжести низкая, большинство пациентов будут длительно болеть.
Тяжелая ЧМТ устанавливается на основании уровня ШКГ в 8 баллов и менее на момент поступления и ассоциируется с достоверным увеличением риска летальности. Раннее и быстрое восстановление системного гомеостаза и терапия, нацеленная на перфузию головного мозга, могут обеспечивать оптимальные исходы в этой сложной популяции. Руководства по всем аспектам ведения пациентов с тяжелой ЧМТ в третьей редакции опубликованы Американской ассоциацией нейрохирургов.
Одиночный эпизод гипоксемии, встречающийся у пациента с тяжелой ЧМТ, ассоциируется с удвоением летальности. Данные по догоспитальной интубации противоречивы. В прошлом было выяснено, что догоспитальная интубация, с целью восстановления проходимости дыхательных путей и адекватной доставки кислорода к мозгу, оптимальна для больных. Однако нет проспективных данных, оценивающих влияние догоспитальной интубации на взрослых пациентов с травмой. Два ретроспективных исследования показали худшие неврологические исходы. Экспертная комиссия, изучившая данный вопрос, заключила, что существующие литературные данные, касающиеся парамедицинских интубаций, являются неубедительными, явные различия в исходах могут быть объяснены:
-
использованием различных методологий и различием сравниваемых групп;
-
использование только одной шкалы ком Глазго для идентификации пациентов с ЧМТ, требующих интубации, ограничено, потребуются дополнительные исследования для уточнения скринирующих критериев;
-
оптимальная техника интубации, равно как и последующая гипервентиляция, может рассматриваться как причина повышения летальности;
-
требуются начальный и дальнейший тренинг, равно как и опыт интубации, для улучшения процедуры интубации;
-
успех программы интубации парамедиками зависит от различных характеристик неотложной медицинской службы и системы оказания помощи при травме.
Пациент должен быть транспортирован как можно быстрее в учреждение, способное оказывать помощь при тяжелой ЧМТ или в ближайшее учреждение, способное интубировать пациента и проводить интенсивную терапию. Обязательным условием является адекватность системной оксигенации.
Пациент с изолированными повреждениями головы может вестись с использованием традиционных вентиляторных стратегий, однако пациенты с травмой груди, аспирацией или интенсивной инфузионной терапией после шока имеют высокий риск развития острого повреждения легких. Классические принципы по применению нулевого или низкого уровня положительного давления в конце выдоха с целью предотвращения повышенного ВЧД неэффективны из-за неадекватной коррекции гипоксемии. При адекватной жидкостной реанимации РЕЕР не увеличивает ВЧД или сниженное церебральное перфузионное давление 150. На самом деле РЕЕР может снижать ВЧД в результате улучшения церебральной оксигенации. Гипервентиляция, бывшая в течение длительного времени основой для ведения пациентов с ЧМТ, более не рекомендуется. Современные руководства подразумевают диапазон РаСО2 между 30 и 35 мм рт. ст., с гипервентиляцией до 30 мм рт. ст. только для эпизодов с повышением ВЧД, которые не могут корригироваться седативными, осмотическими препаратами или барбитуровой комой. Гипервентиляция в течение первых 24 ч вызывает особую озабоченность в силу критического снижения перфузии. Однако эти рекомендации должны выполняться с учетом контекста и должны быть модифицированы в условиях постоянно меняющихся клинических обстоятельств, таких как нарастание объема очага поражения головного мозга и признаков неизбежного вклинения.
Наиболее сложны из всех пациентов те, у которых сочетаются тяжелая ЧМТ и сопутствующий геморрагический шок. Один эпизод гипотензии, определяемый как систолическое артериальное давление менее 90 мм рт. ст., ассоциируются с увеличением заболеваемости и удвоением летальности при тяжелой ЧМТ. Гипотензия совместно с гипоксией ассоциируются с трехкратным увеличением летальности. Следует избегать систолического артериального давления менее 90 мм рт. ст., с достижением целевого уровня среднего АД более 70 мм рт. ст., пока не начат мониторинг ВЧД и уровень ЦПД не может быть достигнут. В отличие от прошлой практики современные рекомендации состоят в достижении у пациента с тяжелой ЧМТ волемического статуса. Поэтому объемная реанимация остается основой терапии, сопровождаемая по потребности вазоактивной терапией. Идеальный раствор все еще не установлен, но растущие доказательства предлагают считать оптимальным, гипертонические растворы солей. Коррекция анемии после потери крови является первым приоритетом для достижения гематокрита более 30%. После начального ведения пациента с тяжелой ЧМТ по протоколу ABCDE начинается поэтапная терапия с достижением церебрального перфузионного давления в рекомендуемом диапазоне от 50 до 70 мм рт. ст. Декомпрессионная краниотомия является хирургической операцией, используемой в наши дни не только для контроля значительного увеличения ВЧД и профилактики грыжеобразования после инсульта, но и в ведении ЧМТ. Декомпрессионная краниотомия показана при отдельных анатомических особенностях ЧМТ, при которых оптимальный уровень ВЧД не может быть достигнут, несмотря на энергичное применение ранее описанных методов терапии, включая барбитуровую кому. Последние доказательства свидетельствуют о том, что уменьшение ВЧД за счет удаления части черепа и использование дуральных заплат может снизить заболеваемость и смертность у ранее бесперспективных пациентов. Декомпрессионная лапаротомия также может быть показана у пациентов с тяжелой ЧМТ, если сопутствующие повреждения или энергичная инфузия увеличили внутрибрюшное давление более 20 мм рт. ст. Увеличенное внутрибрюшное давление ухудшает механику легких, что требует большего уровня среднего давления в дыхательных путях для повышения артериальной сатурации. Увеличение давления на вдохе будет повышать внутригрудное давление и ухудшать венозный дренаж из черепа, и, следовательно, уменьшать ЦПД. В последнее время была предложена новая концепция «множественного компартмент-синдрома» у пациентов с тяжелой ЧМТ. Жидкостная терапия или острое повреждение легких могут повышать внутрибрюшное и внутригрудное давление, тем самым увеличивая ВЧД. Дальнейшее назначение жидкости для поддержки церебральной перфузии или усиление вентиляторной поддержки для лечения острого повреждения легких усугубляет эту проблему. Все это создает порочный цикл формирования множественного компартмент-синдрома и необходимости декомпрессии брюшной полости, даже при отсутствии абдоминальной травмы. Изолированная ЧМТ становится мультисистемным заболеванием.
Подобно гипервентиляционной терапии, имело место изменение отношения к гипотермии при лечении тяжелой ЧМТ. Ранние исследования демонстрировали, что умеренная системная гипотермия уменьшает частоту отека головного мозга и летальность после кортикального повреждения у лабораторных животных. Анализ небольших по объему клинических наблюдений также предположил улучшение исходов у пациентов с ЧМТ, если гипотермия была применена в пределах 24-48 ч. Однако недавно опубликованные рандомизированные многоцентровые исследования эффективности гипотермии в сравнении с нормотермией продемонстрировали отсутствие влияния на исход в популяции больных с тяжелой ЧМТ. Следует отметить, что пациенты, которые поступали в состоянии гипотермии и потом были рандомизированы в группу с нормотермией, имели худший исход в сравнении с теми, кто оставался гипотермичным. Таким образом, согласно рекомендациям, пациенты с тяжелой ЧМТ, которые были гипотермичными при поступлении, не должны подвергаться активному согреванию.
Коррекция внутричерепного давления в операционной
Хотя большинство вмешательств для ведения больных с тяжелой ЧМТ будет происходить в ОРИТ, часто показаны внутричерепная или внечерепная операции. Все описанные предыдущие методы терапии должны продолжаться в течение периоперационного периода, включая позиционную терапию, агрессивный гемодинамический мониторинг и реанимацию, назначение осмотических агентов и глубокий уровень аналгезии и седации. Соответствующий выбор анестетиков включает в себя наркотики и низкие концентрации летучих анестетиков.
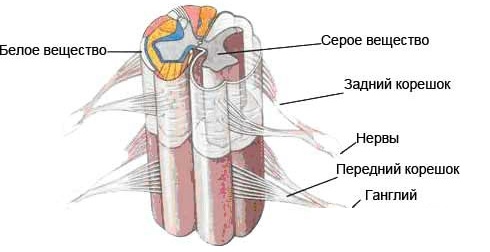
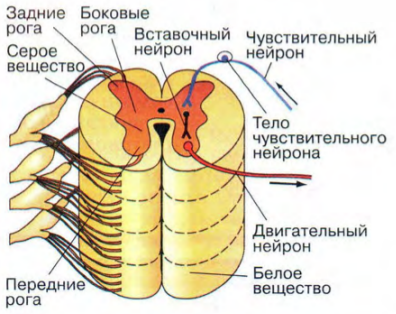
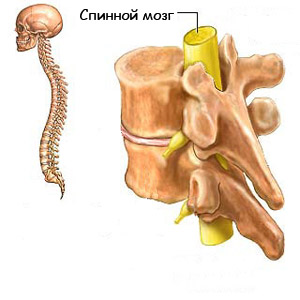
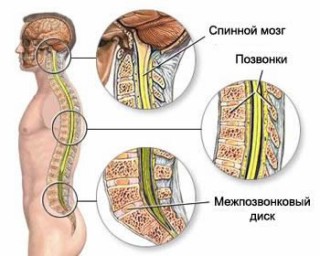
Повреждение спинного мозга
ПСМ после травмы переносит примерно 100000 американцев каждый год. На тупую травму приходится большинство случаев ПСМ:
-
40% - после столкновения автомобилей;
-
20% - после падений;
-
остальное приходится на проникающую травму.
Необратимый неврологический дефицит происходит примерно у 3500 пациентов в год, частичный – у 4500.
Большинство спинальных повреждений определяются на уровне нижнего отдела спинного мозга или верхнего поясничного отдела. Тупая травма спинного мозга наблюдается наиболее часто в наиболее подвижных отделах спинного мозга, особенно на уровне между подвижными и неподвижными сегментами. ПСМ на средне-грудном уровне реже встречается из-за стабилизации ротации за счет грудной клетки и межреберной мускулатуры.
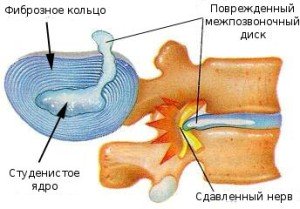
ПСМ обычно сопровождается рентгенологически определяемым повреждением костей позвоночника и сопутствующим нарушением мышц, связок и мягких тканей, поддерживающих их. Однако клинически значимое повреждение шейного отдела спинного мозга может происходить и в отсутствии видимой скелетной травмы. Данная особенность, известная как SCIWORA, наиболее характерна для детей и является предположительно результатом временного переразгибания или поворота шеи, недостаточного для нарушения скелета.
Первичное повреждение спинного мозга, полученное в момент травмы, может усилиться рядом вторичных факторов. ПСМ включает в себя дефицит чувствительности, моторный дефицит или все перечисленное вместе. Неполный дефицит может быть хуже с одной стороны в сравнении с другой и может быстро улучшаться в течение первых минут после травмы. Осложненный дефицит – представленный полным нарушением спинного мозга на одном уровне – гораздо более опасен, обычно с незначительным улучшением в течение длительного времени. Повреждения шейного отдела спинного мозга, вызывающие тетраплегию, сопровождаются значимой гипотензией из-за вазодилатации и потери сократительной способности сердца. Функционирование нижнего отдела спинного мозга постепенно восстанавливается вместе с восстановлением нормального сосудистого тонуса. Диагностика нестабильности шейного отдела позвоночника может быть трудной. Восточная ассоциация хирургии травмы опубликовала руководство, содержащее требования к пациентам, нуждающимся в рентгенографии шейного отдела позвоночника, с объяснением возможного недостатка доказательств повреждений связок у пациента без сознания.
Проведение методики АВС часто дополняется болюсом глюкокортикостероидов у пациентов с открытой ПСМ и полным или частичным неврологическим дефицитом. Болюсная доза 30 мг/кг метилпреднизолона, сопровождающаяся поддерживающей инфузией 5,4 мг/кг/ч назначается, если с момента повреждения прошло не более 8 ч. Инфузия продолжается 24 ч, если начинается в пределах 3 ч от момента повреждения и 48 ч – если начинается от 3 до 8 ч с момента повреждения. Высокодозная терапия глюкокортикоидами привела к небольшому, но достоверному улучшению неврологического статуса после ПСМ в двух многоцентровых исследованиях. Метилпреднизолон демонстрировал улучшение кровообращения спинного мозга, снижение потока внутриклеточного кальция, смягчение формирования свободных радикалов в ишемизированной ткани спинного мозга. Результаты NASCIS были поставлены под сомнение по ряду причин. Положительные преимущества, полученные при назначении высоких доз метилпреднизолона, были вызваны эффективностью у некоторых популяций, но не достигнуты у большинства больных. Изменение уровня повреждения спинного мозга после назначения стероидов не привело к улучшению выживаемости или качества жизни, и результаты не были воспроизведены в других исследованиях острой ПСМ.
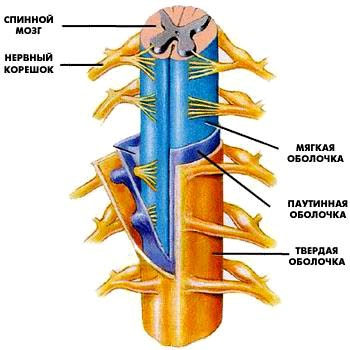
Пациенты с костными повреждениями спинного мозга будут требовать оперативного вмешательства, основанного на их неврологических симптомах и на анатомической стабильности повреждения. Магнитно-резонансная томография показана для оценки повреждения связок и мягких тканей у каждого пациента с переломами позвоночника или неврологическим дефицитом. Операция наиболее часто показана при повреждениях шеи, в то время как поддерживающее крепление или корсет могут быть использованы при грудных и поясничных переломах. Ранняя интубация требуется почти повсеместно у пациентов с переломами шейного отдела и тетраплегией. Вентиляторная поддержка абсолютно показана у пациентов с дефицитом от уровня С4 позвонка, из-за потери функции диафрагмы. Пациенты с уровнем повреждения от С6 до С7 также могут нуждаться в поддержке из-за потери иннервации стенки груди, парадоксального дыхания и невозможности очищать секрет. Рекомендуется и часто выполняется ранняя интубация с использованием фибробронхоскопии в сознании или системы GlideScope до того, как гипоксия превратит пациента в возбужденного и неконтактного. Возможны спонтанная вентиляция и экстубация после хирургической стабилизации и разрешения нейрогенного шока, хотя пневмония является частым и рецидивирующим осложнением, требующим трахеостомии для облегчения туалета трахеобронхиального дерева.
Интраоперационное ведения ПСМ
Пациент, оперируемый по поводу хирургической фиксации позвоночника, представляет собой ряд проблем перед анестезиологом. Первая и важнейшая – потребность в интубации трахеи у пациента с известным повреждением шейного отдела позвоночника. Прямая ларингоскопия со стабилизацией в линию, целесообразна в неотложных случаях у пациентов без сознания, агрессивного больного или у пациента с гипоксемией, при неясном состоянии позвоночника. В операционной пациент в ясном сознании и готовый к сотрудничеству может быть интубирован с использованием множества разных методов, характеризующихся минимальным смещением шейного отдела позвоночника. Наиболее частой в современной клинической практике является техника фиброоптической интубации в сознании. Хотя назальный способ интубации ассоциируется с более легким процессом интубации, он может приводить к повышенному риску синуситов в ОРИТ, если пациент не экстубируется в конце процедуры. Оральная интубация более сложна технически, но предпочтительнее для продленной ИВЛ. Приемлемы назальная интубация «вслепую», использование стилета с подсветкой и использование любого и, вариантов инструментальных систем для непрямой ларингоскопии. Врачу рекомендуется использовать оборудование и методы, с которыми он лучше знаком. Современная концепция состоит в успешном обеспечении трахеальной интубации при минимальной подвижности шейного отдела позвоночника и сохранении вероятности оценки неврологической функции после позиционирования.
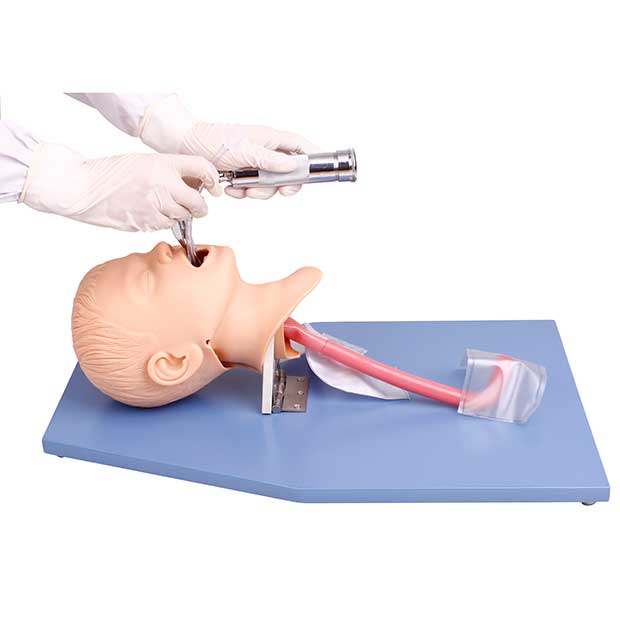
3ащита шейного отдела позвоночника
Стандартная практика диктует, что все пострадавшие с тупой травмой рассматриваются как имеющие нестабильный шейный отдел позвоночника до тех пор, пока данное состояние не будет исключено. Обеспечение проходимости дыхательных путей требует большего внимания от анестезиологов, потому что прямая ларингоскопия вызывает движение шеи с потенциальным обострением повреждения спинного мозга. Стабилизация шейного отдела жестким шейным воротником обычно происходит на догоспитальном этапе. Этот воротник может оставаться на месте в течение нескольких дней до полного завершения выполнения набора тестов по исключению нестабильности шейного отдела позвоночника. Наличие неясного состояния шейного отдела требует использования мануальной стабилизации в течение любой попытки интубации. Этот подход позволяет обеспечить удаление передней поверхности воротника для облегчения широкого открытия рта и смещения челюсти. Стабилизация была тестирована на значительном клиническом опыте и является стандартом в учебной программе ATLS. Экстренная фиброоптическая интубация в сознании хотя и требует меньших манипуляций на шее, как правило, очень трудна в силу наличия секрета и крови в дыхательных путях, быстрой десатурации, недостатка сотрудничества с пациентом, и лучше выполняется у сотрудничающих пациентов с известной нестабильностью шейного отдела. Непрямая видеоларингоскопия с использованием ларингоскопов Bullard или GlideScope предлагает лучшее, что может быть: анестезированный пациент и минимальное движение шейного отдела позвоночника. Тем не менее, потребуются годы клинического опыта, чтобы проверить эту гипотезу.
Персонал
Экстренная интубация требует больше ассистентов, чем интубация, проводимая в контролируемых условиях. Требуются три исполнителя для вентиляции пациента, давления на перстневидный хрящ и обеспечения стабилизации шейного отдела позвоночника; четвертый исполнитель вводит препараты для анестезии и непрерывно наблюдает за пациентом. Дополнительная помощь может требоваться для удерживания пациента, возбужденного вследствие интоксикации или черепно-мозговой травмы.
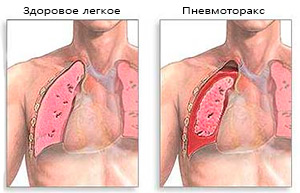
Желательно присутствие хирурга или другого врача, способного оперативно выполнить крикотиреотомию. Даже если хирургическое обеспечение проходимости дыхательных путей не потребуется, дополнительные опытные руки могут оказаться полезными при трудной интубации. Хирург также может пожелать осмотреть верхние дыхательные пути во время ларингоскопии, если произошла травма лица или шеи. Срочное дренирование плевральной полости может оказаться необходимым у некоторых пациентов для устранения напряженного пневмоторакса, который развивается с момента начала вентиляции с положительным давлением.
Анестетики и индукция анестезии
Любой внутривенный анестетик, вводимый пациенту с травмой и геморрагическом шоком, может потенцировать глубокую гипотензию вплоть до остановки сердца, как результат ингибирования циркулирующих катехоламинов. Хотя пропофол и натрия тиопентал являются основой внутривенной индукции в операционной, особенно проблематичным является их использование у травматологических пациентов, потому что оба препарата являются вазодилататорами и оба обладают отрицательными инотропными эффектами. Кроме того, влияние геморрагического шока на мозг, по-видимому, усиливает эффекты данных анестетиков, с пропофолом в малых дозах в размере одной десятой дозы, вызывающей глубокую анестезию у животных при шоке. Этомидат часто называют альтернативой в силу большей гемодинамической стабильности в сравнении с другими внутривенными гипнотическими препаратами у травматологических пациентов, хотя ингибирование катехоламинов может все-таки вызывать глубокую гипотензию.
Кетамин при травме остается популярным для индукции анестезии в силу того, что препарат является стимулятором центральной нервной системы. Однако это также может вызывать прямую депрессию миокарда. У нормальных пациентов эффекты выброса катехоламинов маскируют сердечную депрессию и вызывают гипертензию и тахикардию. У гемодинамически нестабильных больных кардиальная депрессия может привести к коллапсу.
Гипотензия будет развиваться у гиповолемичных пациентов при введении любых анестетиков, так как прерывается симпатическая импульсация и имеет место внезапная смена на вентиляцию с положительным давлением. Исходно здоровые молодые пациенты могут потерять до 40% объема циркулирующей крови, прежде чем артериальное давление снизится, что приводит к катастрофической сосудистой недостаточности с началом индукции анестезии, независимо от выбора анестетика. Доза анестетика должна быть уменьшена при наличии кровотечения, вплоть до минимума у пациентов с угрожающей жизни гиповолемией. Быстрая последовательная индукция и интубация трахеи может трансформироваться только во введение миорелаксантов. Потребности пациента в интубации и немедленных процедурах вариабельны и зависят от:
-
наличия ЧМТ;
-
интоксикации;
-
тяжести геморрагического шока.
Сниженная церебральная перфузия подавляет формирование патологической памяти, но не может быть связана с показателем артериального давления и химическим маркером. Назначение 0,2 мг скополамина может ингибировать формирование патологической памяти при отсутствии анестетика в подобной ситуации, что может помешать последующему неврологическому обследованию из-за длительного периода полувыведения препарата. Небольшие дозы мидазолама снижают вероятность воспоминаний пациента, но также могут способствовать гипотензии. Хотя отзывы о приемном отделении или операционной не являются необычными, ответственность анестезиолога может быть ограничена. Недавний анализ исков о пробуждении во время операций показал их незначительное число в базе данных ASA.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания







Комментарии