Синдром обструктивного апноэ сна: причины, последствия, рекомендации
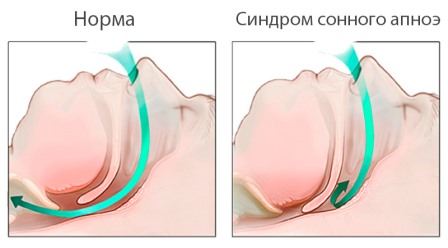
СОАС и обструктивное гипопноэ во сне являются связанными состояниями, характеризующимися повторяющимися эпизодами обструкции верхних дыхательных путей, происходящими во время сна. СОАС определяется как полное прекращение поступления воздуха в легкие длительностью не менее 10 с при сохраняющихся дыхательных усилиях, происходящее во время сна не менее 5 раз в час и сопровождающееся снижением насыщения артериальной крови кислородом по меньшей мере на 4%. Обструктивное гипопноэ во сне определяется как частичное снижение воздушного потока более чем на 50% продолжительностью не менее 10 с, происходящее не менее 15 раз в час во время сна и сопровождающееся падением SaO2 на 4% и более. Диагноз может быть поставлен только на основании полисомнографического исследования, проводимого во сне, во время которого регистрируются:
-
электроэнцефалограмма;
-
ЭКГ;
-
электроокулограмма;
-
капнограмма;
-
скорость воздушных потоков, проходящих через нос или рот;
-
давление в пищеводе;
-
артериальное давление;
-
электромиограмма мышц глотки и конечностей;
-
пульсоксиметрия;
-
интенсивность храпа.
Результаты полисомнографии представляются в виде индекса апноэ/гипопноэ, который является отношением общего количества эпизодов апноэ и гипопноэ к общему времени сна. До настоящего времени нижний предел нормы для ИАГ не был определен в эпидемиологических исследованиях на здоровых субъектах.
Из-за риска развития системной и легочной гипертензии, гипертрофии левого желудочка, аритмий, когнитивных нарушений, стойкой дневной сонливости, а также других состояний активное лечение рекомендуется для пациентов с умеренной или тяжелой формой болезни. Выбор лечения частично зависит от тяжести нарушения дыхания во сне, но большинство врачей сходятся во мнении, что пациентов с умеренным или тяжелым апноэ следует лечить постоянным положительным давлением в дыхательных путях во время сна. Другие консервативные меры могут включать потерю веса, отказ от употребления алкоголя перед сном и сон на боку.
В многочисленных исследованиях подтверждено, что ожирение является важнейшим фактором риска развития СОАГС и около 70% больных с СОАГС страдают ожирением. Тяжелая форма апноэ сна чаще встречается у мужчин, при этом отмечается сильная обратная корреляционная связь между ИАГ и минимальным значением SaO. Важно отметить, что зачастую СОАГС остается не диагностированным до тех пор, пока пациент не подвергается операции. В исследовании на 170 пациентах, которым было запланировано оперативное лечение, только у 15% был уже выставлен диагноз СОАГС, при этом предоперационное обследование выявило наличие данной патологии у 76%. Многие специалисты считают важным, чтобы пациентам с ожирением, которым планируется проведение бариатрических операций, в рамках предоперационной подготовки выполнялось полисомнографическое тестирование для выявления у них СОАГС. Предоперационная диагностика и активное лечение могут иметь следующие преимущества:
-
снижение послеоперационного дефицита сна;
-
улучшение реакции на анестетики и обезболивающие препараты;
-
нормализация сердечно-сосудистых нарушений.
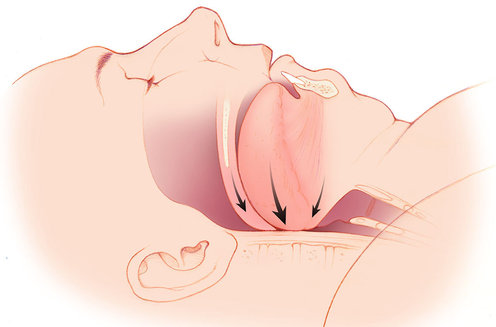
Анатомические особенности пациентов с ожирением и СОАГС обычно включают повышенное количество жировой ткани в полости рта и тканях глотки, включая язычок, миндалины, небные дужки, язык, черпалонадгортанные складки и боковые стенки глотки. Существует обратная зависимость между степенью ожирения и объемом глотки. Накопление жира в боковых стенках уменьшает размер дыхательных путей и придает ротоглотке форму эллипса с короткой поперечной и длинной передне-задней осями. Это может способствовать развитию и усугублению обструкции дыхательных путей, а также увеличить вероятность того, что проходимость дыхательных путей во время масочной вентиляции и выполнение прямой ларингоскопии для интубации трахеи будут затруднены,. Кроме того, использование опиатов и седативных препаратов, необходимых для лечения послеоперационной боли, может утяжелить обструкцию дыхательных путей, поскольку эти лекарства имеют тенденцию снижать тонус расширителя глотки и увеличивать вероятность коллапса верхних дыхательных путей.
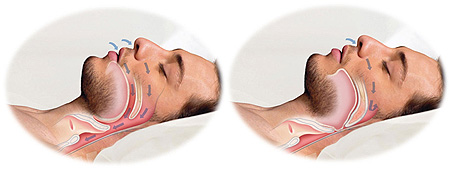
СОАС играет также важную роль в патогенезе воспаления и метаболического синдрома. Эпизоды гипопноэ и апноэ, которые происходят у пациентов с СОАГС, являются частью цикла событий, включающих пробуждение в фазе быстрого сна и падение насыщения гемоглобина кислородом. У пациентов с нелеченым СОАС во время эпизодов гипоксии и реоксигенации активируется симпатическая нервная система, что ведет к повышению уровня провоспалительных цитокинов и оксидативному стрессу в эндотелии сосудов; последнее, в свою очередь, способствует еще большему прогрессированию системного воспаления у пациентов с ожирением и СОАС. У пациентов с СОАГС отмечается повышение уровня различных медиаторов воспаления, в том числе ИЛ-6, С-реактивного белка, лептина, а-ФНО, активных форм кислорода и молекул адгезии, таких как молекула внутриклеточной адгезии 1 типа и молекула адгезии сосудистого эндотелия 1 типа. Таким образом, ожирение, метаболический синдром и СОАГС являются взаимосвязанными заболеваниями, которые существенно изменяют воспалительный ответ и, как результат, увеличивают риск для здоровья, в особенности со стороны сердечно-сосудистой системы и дыхательных путей.
Обеспечение проходимости дыхательных путей
Положение пациента с ожирением является критически важным для ларингоскопии и интубации трахеи. Многие считают, что эти манипуляции гораздо труднее выполнять у пациентов с ожирением, чем у пациентов с нормальным ИМТ. Трудности при ларингоскопии и интубации обычно связывают с наличием у таких пациентов короткой и толстой шеи, большого языка, а также увеличенного объема мягких тканей глотки. Однако в клинической практике не всегда наблюдается корреляция между патологическим ожирением и трудной ларингоскопией. Вполне возможно, что различий между ларингоскопией и интубацией пациентов с нормальным весом и пациентов страдающих ожирением вообще не существует, если следовать простому, но важному подходу, уделяя особое внимание положению пациента перед индукцией анестезии. Правильное положение играет важную роль в обеспечении оптимальных условий для успешной интубации трахеи под контролем зрения.
В исследованиях, целью которых было определение частоты трудной ларингоскопии или интубации у пациентов с ожирением, были получены неоднозначные результаты. В одном из исследований выявили связь между классификацией Маллампати и ИМТ как прогностического фактора сложной ларингоскопии. Во время ларингоскопии пациенты были помещены в улучшенное джексоновское положение независимо от ИМТ. В исследовании, проведенном исключительно на пациентах с ожирением, не была продемонстрирована связь между ИМТ и трудностями при интубации. Высокая градация по шкале Маллампати была определена как предиктор «потенциальных проблем при интубации», однако интубация трахеи при помощи прямой ларингоскопии была успешна у 99 из 100 исследуемых пациентов. Все пациенты были уложены с подушками или полотенцами под плечевым поясом, с приподнятой головой и разогнутой шеей. Другая группа исследователей изучала пациентов, как с нормальным, так и с избыточным весом и пришла к выводу, что градация по шкале Маллампати III или IV является единственным независимым фактором риска трудной интубации в группе больных с ожирением. Авторы продемонстрировали, что для прогнозирования трудной интубации классификация Маллампати обладает низкой специфичностью и низкой положительной прогностической ценностью 62% и 29%, соответственно. Они пришли к выводу, что интубация была более сложной у пациентов с ожирением. Во время интубации пациенты находились в положении полулежа и в улучшенном джексоновском положении. В другом исследовании при помощи ультразвука определялось количество мягких тканей между кожей и передней стенкой трахеи на уровне голосовых связок. Авторы также оценивали дыхательные пути путем измерения тироментального расстояния, открытия рта, степени мобильности шеи, окружности шеи, классификации по Маллампати и наличия СОАС. Только избыток мягких тканей в претрахеальной области, определенный с помощью ультразвука, и окружность шеи продемонстрировали прогностическую значимость в отношении трудной интубации у пациентов в улучшенном джексоновском положении. С целью определения диагностической точности тестов для прогнозирования трудной интубации у пациентов без патологии дыхательных путей был проведен метаанализ 35 исследований. У пациентов с ожирением трудная интубация встречалась в три раза чаще, чем у пациентов без ожирения. Это могло быть следствием неидеального положения пациента. Положение пациента не было четко описано ни в одном из исследований. Также не указано, использовалось ли такая позиция, когда при помощи валиков под плечи и шею добиваются расположения на одной горизонтальной линии наружного слухового прохода и яремной вырезки. В таком положении улучшаются условия ларингоскопии. Collins с колл. провели исследование на пациентах с морбидным ожирением, которых для обеспечения проходимости дыхательных путей уложили или в улучшенное положение по Джексону, или в положение с валиками под плечи и шею, как описано выше. Статистически значимая улучшенная визуализации гортани была продемонстрирована у пациентов, уложенных при помощи валиков.
Основываясь на данных рандомизированных контролируемых исследований, а также другой литературы по обеспечению проходимости дыхательных путей у пациентов, страдающих ожирением, прямая ларингоскопия и интубация не должны вызывать сложности, если пациент тщательно уложен при помощи валиков под плечи и шею. Пациенты с ожирением должны быть обследованы на предмет общих объективных признаков потенциально трудной интубации, к которым относятся небольшое открытие рта, большие и выступающие зубы, ограниченная подвижность шеи и ретрогнатия. Одним из альтернативных методов ведения пациентов с прогнозируемой трудной интубацией является прямая ларингоскопия в сознании под местной анестезией с легкой седацией; в зависимости от полученной ларингоскопической картины в последующем может быть проведена индукция анестезии или же выполнена фиброоптическая интубация в сознании под седацией. При этом должны быть доступны средства для экстренного обеспечения проходимости дыхательных путей, в том числе ларингеальные маски и фибробронхоскоп.
Еще одним вопросом, которому следует уделять особое внимание в периоперационном периоде у пациентов с ожирением, является физиология дыхания. Важно поддерживать адекватную оксигенацию и легочные объемы.
-
Во-первых, у пациентов с ожирением снижены жизненная емкость легких, емкость вдоха, резервный объем выдоха и функциональная остаточная емкость.
-
Во-вторых, объем закрытия альвеол у пациентов с ожирением близок или может находиться в пределах дыхательного объема, особенно в положении лежа на спине.
В результате этих физиологических изменений у больных с ожирением, как правило, происходит быстрое снижение насыщения крови кислородом, особенно в периоды апноэ, например, во время индукции анестезии. В процессе анестезии у пациентов может продолжаться процесс дерекрутирования или коллапса альвеол. Были изучены разные способы поддержания адекватной оксигенации и легочных объемов у пациентов с ожирением.
В одном из исследований по изучению скорости развития гипоксемии у пациентов во время апноэ, больные получали 100% кислород через маску с целью денитрогенизации перед индукцией анестезии. Период апноэ продолжался после индукции, пока насыщение гемоглобина кислородом не снижалось до 90%. Пациенты с ожирением достигали конечной точки менее чем за 3 мин, в то время как у пациентов с нормальным ИМТ это занимало 6 мин. Методы по предотвращению образования ателектазов и десатурации во время индукции анестезии у больных с ожирением включают применение CPAP во время преоксигенации и использование положительного давления в конце выдоха во время масочной и механической вентиляции после индукции анестезии. Использование CPAP на уровне 10 см вод. ст. во время преоксигенации в положении лежа приводило к более высокому PaO2 после интубации и снижению количества развившихся ателектазов. Комбинация СРАР во время преоксигенации и ПДКВ после интубации значительно увеличивали продолжительность апноэ без гипоксии, с 2 до 3 мин, по сравнению с контрольной группой, пациенты которой не получали СРАР или ПДКВ. Однако использование 10 см вод. ст. СРАР в течение 3 мин преоксигенации в положении на спине не изменяло времени, в течение которого насыщение гемоглобина кислородом у больных с ожирением снижалось до 90%. Преоксигенация с подъемом тела и головы на 25 градусов, в отличие от положении на спине, без СРАР увеличило время, необходимое для десатурации до 92% у анестезированных пациентов с апное. РаО2, измеренный после преоксигенации, непосредственно перед индукцией анестезии, был выше у пациентов, находившихся в положении с приподнятым головным концом. Нарушения газообмена, связанные с ожирением, зависят от соотношения талии и бедер, индекса распределения жировой ткани вокруг грудной клетки. Это исследование также продемонстрировало худший легочный газообмен у мужчин с морбидным ожирением, чем у женщин с такой же патологией. В исследовании, проведенном для оценки взаимосвязи между положением пациента и развитием гипоксемии у пациентов с ожирением во время апноэ после индукции анестезии и интубации, пациентов вентилировали 50% смесью кислорода в воздухе в течение 5 мин, после чего дыхательный контур рассоединяли. Вентиляция возобновлялась после того, как SpO2 снижалось до 92%. Пациенты в горизонтальном положении достигали конечной точки через 2 мин, поднятие головного конца операционного стола на 30° увеличивало это время на 30 с, а обратное положение Тренделенбурга под углом в 30° увеличивало это же время на 1 мин. У пациентов с ожирением, которым выполнялись бариатрические операции, использование обратного положения Тренделенбурга в 30° по сравнению с горизонтальным положением на спине продемонстрировало снижение альвеоло-артериальной разницы по кислороду, а также увеличение общей податливости легких и уменьшение пикового давления и давления плато в дыхательных путях. У пациентов с ожирением жизненная емкость во время общей анестезии также снижается в большей степени, чем у пациентов с нормальным весом.
В исследованиях изучалось большое количество способов и маневров, направленных на поддержание оксигенации и легочных объемов во время операции. Постепенное увеличение дыхательного объема с 13 до 22 мл/кг у больных с ожирением под общей анестезией не улучшает газообмен, но увеличивает давление в дыхательных путях. Использование ПДКВ 10 см вод. ст. во время общей анестезии с нейромышечной блокадой у пациентов с ожирением в большей степени способствует улучшению механики дыхания, повышению РаО, а также уменьшению альвеоло-артериальной разницы по кислороду, чем у пациентов с нормальной массой тела. Пневмоперитонеум при лапароскопических вмешательствах увеличивает сопротивление легких и снижает их динамическую податливость. Во время пневмоперитонеума у пациентов с ожирением изменения положения тела, дыхательного объема и частоты дыхания не оказывают никакого влияния на альвеоло-артериальную разницу крови по кислороду. Во время пневмоперитонеума при лапароскопических бариатрических операциях раскрытие альвеол, достигаемое за счет многократного повышения и удержания давления в легких до 50 см вод. ст. с последующей ИВЛ с ПДКВ 12 см вод. ст, способствовало интраоперационному увеличению РаО, но при этом отмечалась артериальная гипотензия, требующая использования вазопрессоров. С целью оптимизации ПДКВ у пациентов с ожирением, которым выполнялось лапароскопическое бандажирование желудка, нормальная функциональная остаточная емкость легких поддерживалась при помощи ПДКВ на уровне 15±1 см вод. ст. При этом для предотвращения изменений гемодинамики активно использовалась инфузионная терапия.
Резюмируя, наиболее благоприятное положение пациента или оптимальное значение ПДКВ во время преоксигенации, индукции анестезии или во время операции для пациентов с ожирением до настоящего времени все еще не определены. Более того, применение неинвазивных способов вентиляции для поддержания оксигенации и вентиляции у пациентов с ожирением, включая поддержку давлением и двухуровневую поддержку давлением с маской во время преоксигенации, индукции и поддержания анестезии, изучено недостаточно. Идеальное положение пациента, использование ПДКВ, а также специальные режимы вентиляции для поддержания функции легких и газообмена непосредственно перед пробуждением и экстубацией также не были определены. В настоящее время отсутствуют опубликованные рекомендации, касающиеся вопросов респираторной механики и поддержания оксигенации у пациентов с ожирением во время анестезии. Соответственно, с учетом описанных выше нюансов обеспечения проходимости дыхательных путей, а также проблем оксигенации, легочных объемов и вентиляции у лиц, страдающих ожирением, анестезиологу следует укладывать пациента таким образом, чтобы одновременно создавались оптимальные условия и для интубации, и для поддержания оксигенации и легочной механики.
По общепринятому алгоритму пациенты с ожирением до преоксигенации изначально укладываются при помощи валиков в приподнятое положение, а затем при необходимости в обратное положение Тренделенбурга, для достижения 25-30° наклона грудной клетки. Затем пациентов преоксигенируют от 3 до 5 мин 100% кислородом под положительным давлением. Для пациентов, использующих СРАР в домашних условиях для лечения СОАС, применяют СРАР или вентиляцию с поддержкой давлением через лицевую маску на уровне, идентичном СРАР, используемому пациентом дома. В противном случае целесообразно применять СРАР от 8 до 10 см вод. ст. После индукции анестезии во время операции разумно поддерживать ПДКВ 10-12 см вод. ст, при этом необходимо соблюдать осторожность и активно лечить возможную артериальную гипотензию. Наконец, если во время операции положение пациента было изменено, то перед пробуждением и экстубацией необходимо вернуть пациента назад в положение с приподнятым головным концом.
В рамках подготовки к пробуждению нервно-мышечная блокада должна быть полностью реверсирована до экстубации. Учитывая, что режим вентиляции поддержки давлением существует во многих новых моделях наркозно-дыхательных аппаратов, пациент с ожирением может быть переведен на этот режим вентиляции на этапе пробуждения до экстубации, как только восстановилась спонтанная вентиляция. После восстановлении адекватной мышечной силы, что должно быть подтверждено данными нейромышечного мониторинга и выполнением теста на поднятие и удержание головы в течение 5 с, пациент, который адекватно реагирует на команды, может быть безопасно экстубирован. Поддержка давлением или СРАР может быть использована сразу при помощи лицевой маски, так же, как это делается во время преоксигенации перед индукцией анестезии. Существуют разнообразные устройства для обеспечения СРАР во время транспортировки пациента из операционной. Чаще всего используют СРАР в палате пробуждения, особенно у пациентов, которые используют СРАР для лечения СОАС.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания











Комментарии