Синдром малого сердечного выброса: лечение, диагностика
Причинами малого сердечного выброса могут быть ухудшение функции миокарда и нарушение распределения потоков крови при нормальном выбросе из желудочка.
Дисфункция миокарда является обычным феноменом после первой стадии реконструкции у пациентов со СГЛОС. Она обусловлена сочетанием многих факторов, часть из которых присуща этой группе больных, а другие являются следствием сердечной хирургии. Искусственное кровообращение и связанные с ним действия приводят к нарушению метаболизма и электролитного баланса, повреждению эндотелия, активации каскада коагуляции, выделения множества эндогенных вазоактивных веществ и воспалительных медиаторов, к микроэмболии и стрессорной реакции всего организма. Патофизиологическими последствиями этих факторов являются увеличение порозности капиллярных стенок и выпотевание жидкости в интерстициальное пространство, нарушение нормальной вазоактивной обратной связи, глобальная воспалительная реакция и нарушение водно-электролитного и метаболического гомеостаза. Вследствие этого у пациента могут развиться отек миокарда, нарушение эндотелиальной функции коронарных артерий, трансмембранного тока кальция и калия, повреждение миоцитов ишемией и реперфузией, микроэмболия коронарных артерий, склонность к аритмогенезу и другие изменения, связанные с воспалением. Снижение совокупного сердечного выброса в течение первых суток после операции пропорционально продолжительности искусственного кровообращения. Оно проявляется снижением системной венозной сатурации и увеличением артериовенозной разницы по кислороду и является фактором риска летального исхода. Повышение постнагрузки после искусственного кровообращения также существенно снижает функцию миокарда и суживает буферную зону миокардиального резерва. Кровотечение и другие осложнения, такие, как инфекция, сопровождаются абсолютной или относительной гиповолемией и усиливают желудочковую дисфункцию.
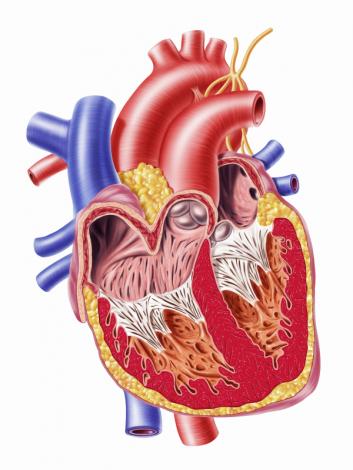
Ряд факторов, специфичных для СГЛОС, предрасполагают к дисфункции миокарда и низкому сердечному выбросу. У этих больных — функционально единственный морфологически правый желудочек. Структура правого желудочка во многом отличается от левого желудочка, что снижает механическую способность нагнетать кровь в системный бассейн с высоким сосудистым сопротивлением. Кроме того, поскольку имеется единственный функциональный желудочек, его механика не поддерживается взаимодействием двух нормально развитых желудочков. Исследования показали значение этого фактора у старших пациентов с функционально одножелудочковым сердцем с доминирующим левым желудочком. Очевидно, что при инверсном положении этот механизм также существует. Наличие маленького гипертрофированного и плохорастяжимого левого желудочка, который не обеспечивает существенного систолического выброса, может ухудшить диастолическую функцию правого желудочка при СГЛОС. Важность этих факторов до конца на доказана, но они могут играть роль в снижении базового миокардиального резерва.
Второй анатомической причиной снижения желудочковой функции является недостаточность коронарного кровотока вследствие обструкции в месте проксимального анастомоза аорты и легочной артерии. Причиной недостаточного коронарного кровотока служит также крайне узкая восходящая аорта у некоторых пациентов. Кроме того, у больных с атрезией аорты и митральным стенозом может быть аномальное коронарное кровообращение, как у пациентов с легочной атрезией и интактной межжелудочковой перегородкой.
Ишемия миокарда во время пережатия аорты и остановки кровообращения также снижает послеоперационную функцию желудочка, что подтверждено гистологическими исследованиями. Ишемия миокарда в дооперационном периоде чаще наблюдается при атрезии аорты и позднем поступлении в хирургическую клинику, когда проток частично закрыт. Защиту миокарда у этих пациентов можно улучшить, если физиологический контур АИК заполнять профильтрованной свежей цельной кровью.
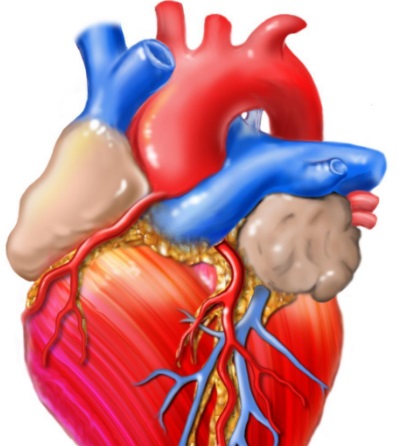
У пациентов со СГЛОС после операции коронарный резерв снижен при увеличенном потреблении кислорода миокардом, снижении содержания кислорода в системной крови и снижении коронарного кровотока на единицу массы миокарда или объема, что является результатом анатомической обструкции кровотоку, недостаточной плотности коронарных капилляров, дисфункции эндотелия коронарных артерий или снижения индекса «диастолическое давление—время». Пациенты со СГЛОС после операции страдают от повышенной потребности миокарда в кислороде, обусловленной увеличенной нагрузкой на единственный желудочек, нагнетающий кровь в системный и легочный сосудистые бассейны, и от сниженной доставки кислорода вследствие относительной гипоксемии и сочетания вышеупомянутых факторов, ведущих к уменьшению коронарного кровотока.
Энергетические потребности миокарда повышены в условиях дисфункции желудочка, вызванной дилатацией, снижением диастолического комплайнса и конечно-систолической способности желудочка возвращаться к диастолическому объему при различных уровнях преднагрузки. Аритмии также ухудшают эффективность использования энергии миокарда за счет укорочения времени диастолического наполнения, ухудшения атриовентрикулярного взаимодействия и неэффективного сокращения после нормального.
Значение распределения кровотока
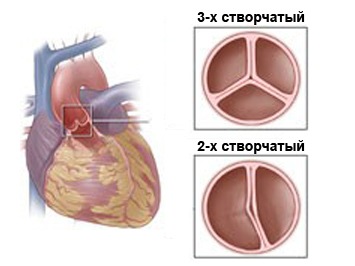
Другим важным фактором системной перфузии является неравномерное распределение сердечного выброса. Это происходит при гиперперфузии легких и недостаточности клапанов. Хотя небольшая недостаточность трехстворчатого и неоаортального клапанов наблюдается часто, выраженная регургитация встречается относительно редко. У трети пациентов со СГЛОС трехстворчатый клапан, который работает как системный AV-клапан, морфологически аномальный, что является предпосылкой для регургитации. Компетентность клапана может ухудшиться, особенно у пациентов с выраженной дисфункцией желудочка и его дилатацией. В отличие от митрального клапана, папиллярно-хордальный аппарат трехстворчатого клапана прикрепляется к межжелудочковой перегородке. Дилатация желудочка приводит к ухудшению смыкания створок даже при отсутствии морфологических изменений клапана. Так у пациентов, которые в предоперационном периоде были в состоянии выраженного метаболического ацидоза, часто имеется недостаточность трехстворчатого клапана, которая может сохраниться в послеоперационном периоде.
Лечение малого сердечного выброса
Лечение является комплексным и включает:
-
применение положительных инотропных средств;
-
нормализацию рН крови;
-
снижение постнагрузки;
-
снижение потребности в кислороде путем релаксации, седирования, устранение аритмий.
При гематокрите ниже 40% оптимизируют кислородную емкость крови трансфузией эритроцитарной массы.
У пациентов с потенциально обратимой дисфункцией миокарда, связанной с аритмиями, дискретным ухудшением коронарной перфузии или спровоцированной системно-легочным артериальным шунтом, показана механическая поддержка кровообращения с помощью ЭКМО.
Если системный кровоток снижен вследствие увеличенной объемной нагрузки, снижают системную постнагрузку повышением дозы милринона, инфузией нитропруссида, вентиляцией с положительным давлением на выдохе, гипоксией или гиперкарбией. При обнаружении анатомической причины прибегают к хирургическому вмешательству — ревизии шунта, дренированию перикарда.
Гипоксемия
-
Патофизиология послеоперационной гипоксемии.
Сатурация системной артериальной крови определяется тремя факторами: содержанием кислорода в легочных венах, содержанием кислорода в системных венах и соотношением Qл/Qс. Снижение одного из этих показателей приводит к гипоксемии. Низкое содержание кислорода в легочных венах нередко наблюдается после операции. Потенциальными причинами обеднения кислородом крови, оттекающей из легких, могут быть:
-
внутрилегочное шунтирование;
-
снижение газообмена вследствие обструктивной болезни легочных артерий или отека;
-
уменьшение эффективного объема легких вследствие пневмоторакса или выраженной экссудации.
Снижение насыщения кислородом системных вен обычно обусловлено низким сердечным выбросом, а также малой кислородной емкостью или высоким потреблением кислорода. Последнее может быть результатом недостаточного седирования или релаксации, нарушением терморегуляции, возникнуть из-за инфекции или усиленного обмена веществ.
Наиболее частыми причинами снижения легочного кровотока являются уменьшение совокупного сердечного выброса и проходимости системно-легочного шунта. Легочно-сосудистое сопротивление у новорожденных в раннем послеоперационном периоде лабильно при аномалиях с исходно высоким легочным кровотоком и с обструкцией легочного венозного оттока. Гиперреактивность легочных сосудов является сложным феноменом, обусловленным эндотелиальной дисфункцией вследствие дооперационного и послеоперационного нарушения напряжения сдвига в легочном кровообращении, а также повреждающего действия на легочные сосуды искусственного кровообращения. Повышенное ЛСС редко является единственным фактором, ответственным за выраженную гипоксемию. Снижение легочного кровотока скорее обусловлено недостаточностью кровотока по шунту.
После первой стадии паллиативного хирургического лечения СГЛОС оптимальное соотношение Qл/Qс равно 1. При этом сатурация кислородом системной артериальной крови, согласно уравнению Фика приблизительно равна 75%.
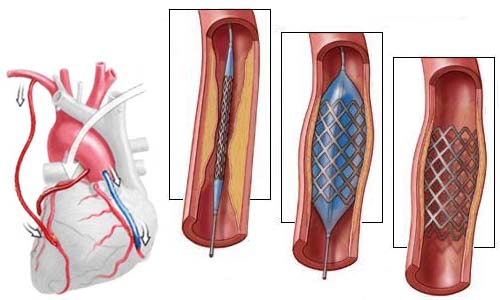
-
Лечение послеоперационной гипоксемии.
Если снижение легочного венозного насыщения вызвано наружным сдавлением легкого плевральным экссудатом или пневмотораксом, плевральную полость дренируют тонким катетером. Патологию легочной паренхимы устраняют подбором режима вентиляции и соответствующей медикаментозной терапией. Увеличение положительного давления на выдохе может разрешить участки ателектаза и нормализовать вентиляционно-перфузионное соотношение, а также уменьшить отек легкого. Увеличение фракции вдыхаемого кислорода способствует повышению насыщения легочной венозной крови.
Лечение гипоксемии, обусловленной системной венозной десатурацией вследствие низкого системного выброса, осуществляют следующим образом. Пациентам с нормальным сердечным выбросом, но увеличенным потреблением кислорода, вызванным возбуждением и болью, проводят седацию и релаксацию. Инфекция и гипертермия сопровождаются повышенным потреблением кислорода. Обычными методами лечения являются применение антибиотиков, антипиретиков и поверхностного охлаждения.
Недостаточность межартериального шунта корригируют увеличением переливания жидкостей, поддержанием высокого артериального давления, обеспечением адекватной седации и повышением содержания кислорода во вдыхаемой газовой смеси. Обтурированный шунт требует хирургического вмешательства или интервенционной катетеризации. При остром ухудшении осуществляют реанимацию с использованием ЭКМО.
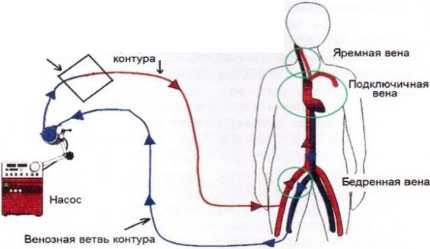
Заключение
Целями послеоперационного лечения в течение первых 24 ч являются:
-
поддержание совокупного сердечного выброса путем использования инотропных средств и снижения системной постнагрузки;
-
минимизация потребности в кислороде путем седирования и релаксации;
-
ограничение стрессовых процедур, увеличивающих потребление кислорода, сопротивление легочных и системных сосудов;
-
устранение боли и неспецифических осложнений.
Недостатками этой лечебной стратегии являются необходимость в постоянных инвазивных катетерах, механической вентиляции и применении потенциально токсичных медикаментов. При стабилизации функции миокарда и сопротивления легочных и системных сосудов важно раннее удаление катетеров и трубок и отлучение от фармакологической поддержки — активная «деинтенсификация». При неосложненном раннем послеоперационном периоде эту программу начинают осуществлять через 16-20 ч после операции. Эта стратегия позволяет снизить ятрогенные осложнения, не жертвуя качеством ухода во время раннего послеоперационного периода. Вентиляцию легких постепенно уменьшают и пациента экстубируют через 24-48 ч после операции. Энтеральное питание начинают после отлучения от инотропной поддержки. Оптимальное время пребывания в отделении интенсивной терапии — 4-5 дней.
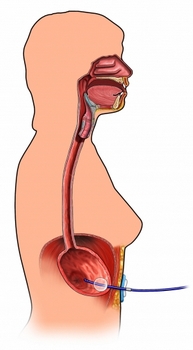
Питание и некротический энтероколит
Энтеральное питание начинают с назогастрального введения пищи с постепенным увеличением объема. Большинству пациентов назначают ранитидин. Парентеральное питание постепенно уменьшают. Оральное питание начинают постепенно. У больных со СГЛОС оромоторная и глоточная координация и поведение питания часто нарушены. Важно оценить роль левой голосовой связки при возникновении кашля или респираторного дистресса при оральном питании, поэтому до 25% новорожденных при выписке из стационара находятся на дополнительном режиме назогастрального питания. Обычная продолжительность дополнительного назогастрального питания в домашних условиях составляет 1-2 нед, редко — более 2 мес.
Одним из наиболее важных оснований для раннего начала энтерального питания является возможность развития некротического энтероколита. Более 3% больных с различными тяжелыми ВПС поступают в хирургический стационар с признаками некротического энтероколита, его наблюдают у 7,6% пациентов со СГЛОС. Факторами высокого риска развития некротического энтероколита и послеоперационной летальности являются более молодой гестационный возраст при рождении и эпизоды низкой системной перфузии. Если у больного имеются симптомы некротического энтероколита, питание прекращают, эвакуируют содержимое желудка, осуществляют парентеральное питание и начинают медикаментозное внутривенное лечение антибиотиками и ранитидином. Больные хорошо переносят I-II стадию некротического энтероколита. Хирургический некротического энтероколит III стадии сопровождается крайне высокой летальностью. Раннее начало лечения при подозрении на некротический энтероколит является жизнеспасающим.
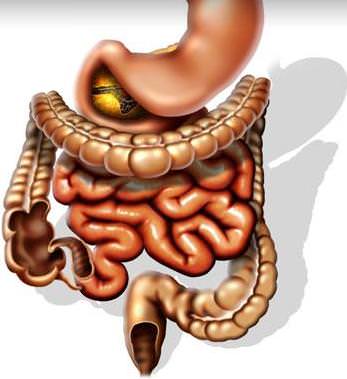
Ведение в постгоспитальном периоде
Из отделения интенсивной терапии пациента выписывают домой или переводят в лечебное учреждение по месту жительства. Родителей инструктируют о признаках низкого сердечного выброса, целях лечения энтеральными медикаментами, важности адекватного питания — орального или дополнительного назогастрального. Обычно назначают фуросемид в дозе 1-2 мг/кг в день и аспирин 40 мг в день. В отдельных случаях при значительной трикуспидальной недостаточности, дисфункции желудочка и аритмиях назначают дигоксин и ингибиторы ангиотензин-превращающих ферментов.
Последующие этапы хирургического лечения — создание одножелудочкового кровообращения по Fontan — начинают с операции hemi-Fontan или двунаправленного кавопульмонального анастомоза в 3-4-месячном возрасте.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания








Комментарии