Робот-хирург. Робот системы в современной хирургии
Впервые слово «робот» было использовано чешским писателем Карелом Чапеком в пьесе «Универсальные роботы Россума» «R.U.R» в 1921 г. «Robota» по-чешски означало «каторга», «вынужденный труд». Первые роботы были разработаны Национальным агентством по аэронавтике и исследованиям космического пространства для исследования космоса. Эти устройства, или телеманипуляторы, были способны выполнять работу на борту космического корабля или в открытом космосе. Они контролировались из центра управления на Земле или на борту космического корабля. Телеманипуляторы интенсивно использовались во время миссий кораблей-челноков 1983-1997 гг. Исследования в области траекторий и систем точного наведения ракет привели к разработке точнейшего механизма прицеливания. Высокая точность была необходима для наблюдения за Землей и звездами во время работы телескопа, установленного на станции Spacelab. Tакие телеманипуляторы, как Instrument Pointing System, были специально сконструированы для точности наведения до +1, ученые исследовательского центра Эймса занимались разработкой виртуальной реальности. Объединение виртуального языка программирования и Dataglove дало возможность взаимодействовать с виртуальными трехмерными объектами. Тем не менее, только интеграция роботоинженерии и виртуальной реальности дало возможность создать телеманипулятор, способный накладывать анастомозы на нервы и сосуды во время операций на ладони.
Министерству обороны США стало понятно, что виртуальная реальность и так называемое телеприсутствие могут быть полезны для оказания медицинской помощи раненым на поле боя. Используя виртуальную реальность, хирург может находиться непосредственно около раненого пациента; эта идея была выражена термином «телеприсутствие». Данные о потерях во время войны во Вьетнаме показали, что из всех раненых солдат 1/3 умирала от массивных поражений и ран головы, а другая 1/3 погибала от профузных кровотечений, но потенциально они смогли бы выжить при своевременном оказании медицинской помощи. Министерство обороны постаралось обеспечить более эффективное присутствие медицинской помощи на поле боя, учитывая, что 1/3 погибших, можно было бы спасти. Телеприсутствие должно было позволять хирургу, находящемуся на борту авианосца, при помощи телеманипулятора оперировать раненого, находящегося на поле боя. Руководствуясь этой идеей, Министерство обороны финансировало разработки телеманипуляторов для мобильных операционных с возможностью телеприсутствия.
Дополнительный импульс развитию роботохирургии придали ограниченные возможности лапароскопических вмешательств. В 1987 г. Mouret провел первую лапароскопическую холецистэктомию в Лионе. В 1988 г. Perissat и колл. представили новую технологию на конгрессе Американского общества гастроэнтерологической эндоскопической хирургии, что послужило началом стремительного распространения лапараскопической хирургии. Несмотря на то, что лапароскопическая хирургия привнесла большие преимущества для пациентов, эта методика имеет свои ограничения, такие как потеря трехмерного видения, нарушение тактильной чувствительности, неловкость манипуляций в связи с большой длиной инструментов и эффектом рычага. Эффект точки опоры выражен в том, что кончик инструмента, опираясь на точку опоры на уровне кожного разреза, движется в противоположном направлении. В связи с этим хирург должен овладевать новыми навыками. Попытки превозмочь неудобства лапараскопических операций придали импульс развитию роботосистем, позволяющих улучшить хирургические приемы и лучше контролировать движения инструментов.
Первые роботоприборы появились в 1980-х гг. и использовались при стереотаксических операциях на головном мозге.
В 1992 г. ROBODOC была использована для обработки кости с целью создания необходимого пространства для протезирования тазобедренного сустава. К середине 1990-х гг. стали применяться позиционные роботы. Совместно с лапароскопической роботосистемой для отведения органов была разработана автоматизированная эндоскопическая система оптимизации положения с контролируемым голосом оптимальным направлением камеры. В начале 1990-х гг. была разработана концепция телеманипулятора для медицинского использования по типу мастер/помощник. Первый манипулятор такого типа для медицинских целей был разработан Stanford Research Institute в 1991 г., с компьютерным алгоритмом, переводящим движения рук хирурга в движения удаленного на расстояние исполнительного инструмента. В ранних модификациях было заложено только четыре степени свободы, но в 1992 г. специалистами из Германии был разработан прототип с шестью степенями свободы. В 1994 г. компания Intuitive Surgical приобрела технологические права у Stanford Research Institute и в 1997 г. представляла прототип робота Da Vinci.
Для инженеров было понятно, что расстояние между хирургом и пациентом является лимитирующим фактором в возможности точного и аккуратного контроля хирургических инструментов. Запаздывание – это время от отправки сигнала от руки хирурга к инструменту до получения хирургом изображения этого движения на экране. Интервал времени от отправки до получения сигнала обратно с Земли до геосинхронизированного орбитального спутника на расстояние 22 300 миль равняется 1,2 с. Такая отсрочка в передаче сигнала делает хирургическую операцию невозможной на практике. Человек может компенсировать задержку сигнала до 200 мс, удлинение времени нарушает точность хирургического вмешательства. Во время операции ткань отводится хирургом, и он не способен достаточно быстро заметить данное движение, что может привести к хирургическому разрезу в нежелательном месте.
Наиболее оптимистичный результат в хирургической операции на расстоянии был достигнут при применении широкополосного оптоволоконного кабеля. Сокращение интервала запаздывания до 155 мс позволило хирургу Maresaux и соавт. успешно выполнить холицистэктомию на расстоянии между Нью-Йорком и Страсбургом. В 2003 г. в Канаде была установлена телероботизированная хирургическая система между университетским и районным госпиталями на расстоянии 250 миль друг от друга. Целью было создать канал, по которому хирург-эксперт ассистировал бы хирургу, непосредственно выполняющему операцию. Выполнялись такие лапароскопические операции, как фундопликация по Ниссену, правосторонняя гемиколонэктомия, сигмоидэктомия/передняя резекция прямой кишки и устранение паховой грыжи.
В последние годы происходит всплеск роботохирургии. В 2000 г. было проведено 1500 робот-операций, а в 2004 более 20 000, 8000 из которых принадлежат проведенным урологами простатэктомии.
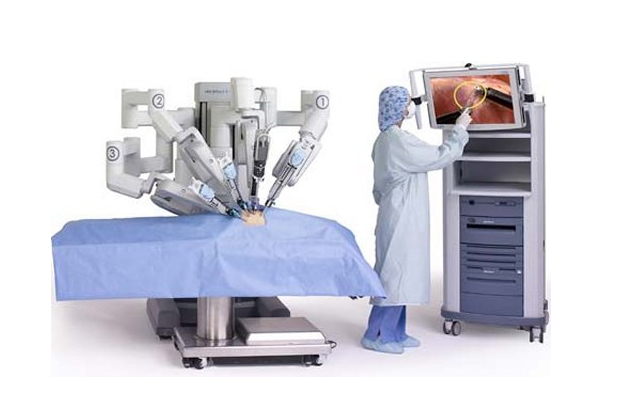
Робот системы
Слово «робот» - очень распространенный термин, описывающий автономный аппарат, способный выполнять различные задания. Промышленные роботы выполняют высоко точные повторяющиеся задания на сборочных линиях. Роботы перепрограммируются в режиме оффлайн и выполняют задания в ответ на запрос. В ортопедической и нейрохирургии такие задачи, как сверление и установка датчиков, основаны на регистрации. Регистрация - это математический процесс определения и трехмерной анатомической ориентации на основе предварительного КТ- или ЯМР-сканирования.
Вторым типом роботов стали системы AESOP, контролирующие положение и направление инструмента. Третий тип роботов, телеманипулятор, также находится под постоянным контролем оператора. Эти устройства полностью или с максимально возможной точностью повторяют движения рук оператора. На сегодняшний день в мире существует несколько типов таких устройств. Система Da Vinchi утверждена FDA для лапароскопии, торакоскопии, внутрисердечных клапаносохраняющих операций на митральном клапане. Параллельно разрабатывалась и была одобрена для применения в общей и лапароскопической хирургии система Zeus. Обе системы были очень схожи, с небольшими отличиями. Вскоре Zeus была приобретена их конкурентами – Intuitive Surgical, производящими роботизированную систему Da Vinchi, которая описана в данной статье, как наиболее современная роботизированная хирургическая система.
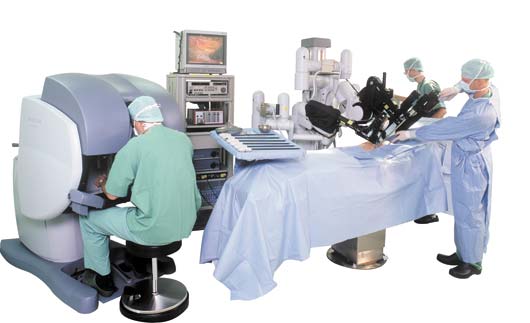
Система Da Vinchi состоит из трех компонентов:
-
консоли;
-
трехмерного оптического блока;
-
хирургического блока.
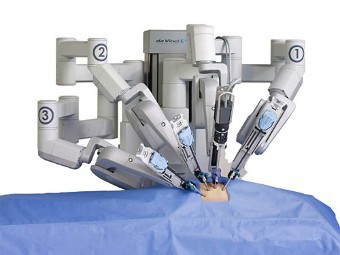
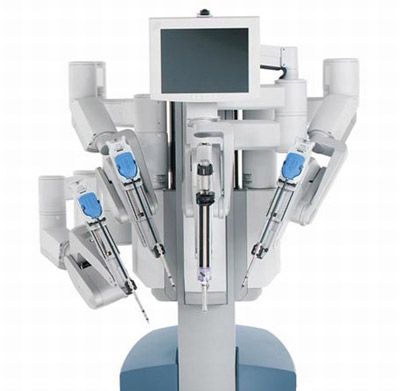
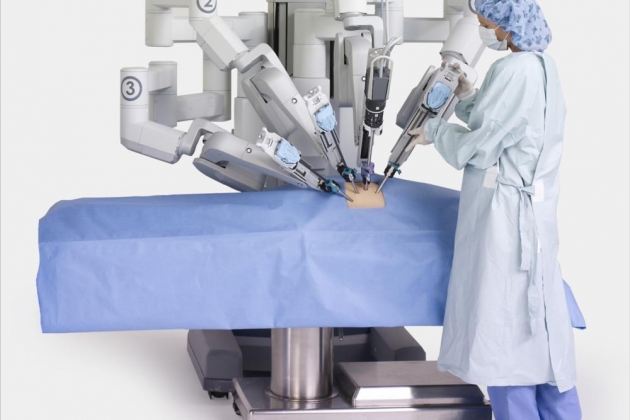
Четыре манипулятора хирургического блока управляются хирургом в режиме реального времени с помощью компьютерной системы контроля. Первые два манипулятора управляются правой и левой руками хирурга, они держат инструменты. Манипулятор номер 3 определяет позицию эндоскопа. Добавочный 4 манипулятор дает возможность хирургу держать еще один инструмент или выполнять дополнительные хирургические приемы, такие как отведение органа, накладывание непрерывного шва. Наличие 4 манипуляторов дает возможность оперировать без второго хирурга-ассистента. Описанная система позволяет хирургу физически не находиться у операционного стола с пациентом.
Семь степеней свободы были заложены в дизайн системы для того, чтобы повторить движения человеческой руки. Они включают три вида движения предплечья:
-
внутрь-изнутри;
-
вверх-вниз;
-
из стороны в сторону;
и три движения кисти:
-
слева направо;
-
подача предмета вверх-вниз;
-
вращение.
Седьмая степень свободы – это захват или разрез. В систему включен фильтр частоты колебаний рук с пределом в 6 Гц, для исключения дрожи рук хирурга. Также применяется система пропорционального движения в максимальном отношении 5:1, что позволяет работать в миниатюрных масштабах. Оптическая консоль состоит из двух независимых компьютерных оптических систем для каждого глаза хирурга. Каналы виртуально объединены для воссоздания виртуального трехмерного изображения.
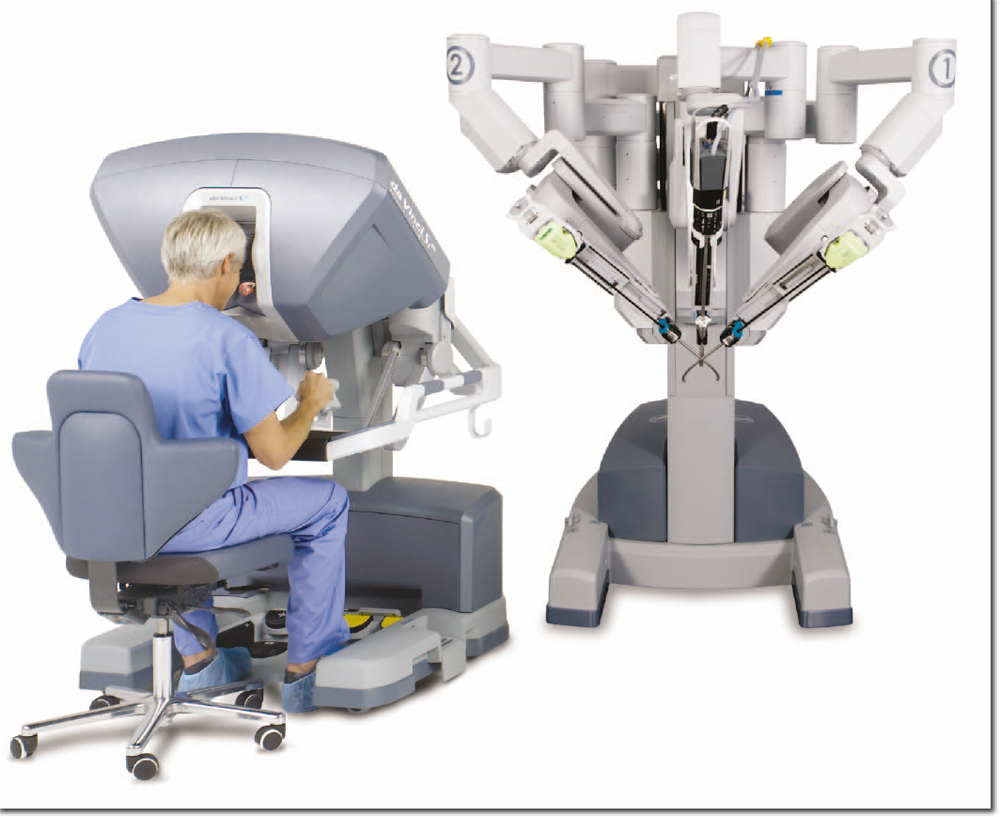
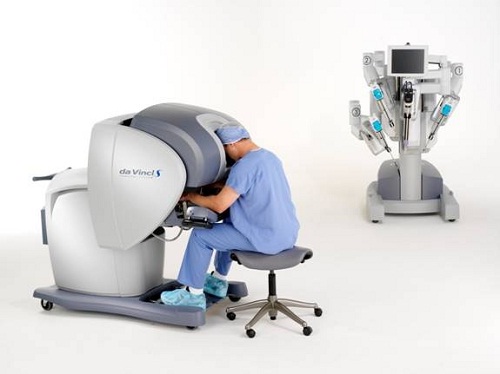
Хирург располагается у консоли управления и работает телескопической рукой и тремя манипуляторами-руками робота у экрана-визора, похожего на микроскоп с двумя окулярами. Каждый окуляр зеркально отражает монитор компьютера. Каждый монитор проецирует один канал стереоэндоскопа, в целом создавая трехмерное изображение операционного поля.
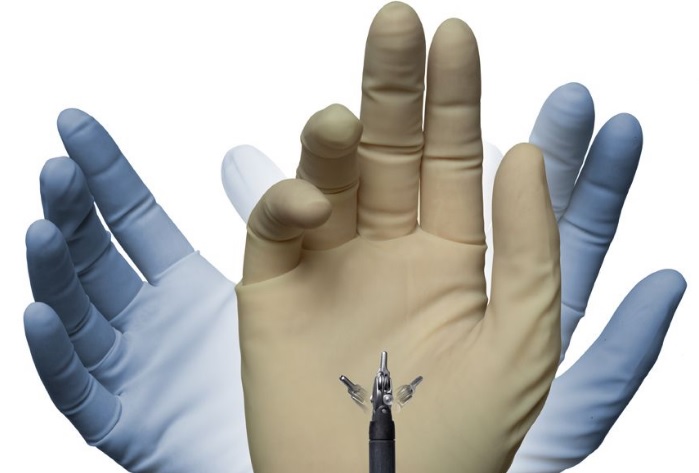
Хирург работает манипуляторами с помощью двух рычагов управления, в которые он вдевает указательные и большие пальцы обеих рук. Движения кистей рук воспроизводят движения рук робота с инструментами. Ножная педаль на консоли выключает движения руки робота, вторая педаль обеспечивает дополнительную настройку камеры эндоскопа, и третья педаль управляет электрокоагулятором.
Сама тележка с руками-манипуляторами, управляемыми сидящим за консолью хирургом, чрезвычайно тяжела и громоздка. Эта конструкция пододвигается к пациенту на колесах и фиксируется в нужном месте тормозами. В связи с непосредственной близостью тележки к пациенту, последний должен быть защищен или огражден от непреднамеренного контакта с движущимися манипуляторами робота. Еще более важно то, что после введения рук манипуляторов в тело пациента положение пациента не должно меняться, пока манипуляторы не будут полностью извлечены из операционного поля и отключены. Даже небольшое движение пациента в связи с недостаточной миорелаксацией может привести к катастрофе. Кнопки сцепления дают возможность предварительной установки рук манипуляторов без движения в троакарах или портах доступа. Функция сцепления позволяет ассистентам хирурга менять инструменты в манипуляторе. В оптическом блоке установлен компьютер, обеспечивающий стереоэффект путем объединения левого и правого оптических каналов, а также пакет программ, обеспечивающих кинематику манипуляторов робота. Движения рук хирурга переводятся компьютером в цифровой код, управляющий движениями рычагов, моторов и кабелей, полностью повторяя движения рук хирурга.
Находящиеся в теле пациента инструменты должны быть стерильны, в то время как их соединения с манипуляторами – нет. Для каждого типа инструментов характерны своя шкала подвижности и приложения усилия, в соответствии с хирургической задачей, что, в свою очередь, требует специального программного обеспечения. Привлечение дополнительного персонала необходимо для смены инструментов на необходимые во время операции. Мониторы установлены так, чтобы каждый присутствующий в операционной мог наблюдать за тем, что происходит в операционном поле.
В дальнейшем более углубленно должен быть рассмотрен вопрос тактильной чувствительности, так как обратная связь от робота до рук хирурга пока оставляет желать лучшего.
Робот в какой-то мере обладает чувствительностью, но приложенная к тканям сила недостаточно хорошо коррелирует с силой, приложенной к роботу. Эта сила варьирует в зависимости от типа инструмента и зависит от приложенных к нему сил натяжения или давления. Хирург-оператор должен уметь оценить давление на орган, основываясь на визуальной оценке изменения формы органа или ткани.
Хирургическая система ZEUS являет собой еще один пример телеманипулятора по принципу мастер/ помощник, где для визуализации применяется вспомогательная система AESOP Robotic System. Данная система визуализации представляет собой отдельный механический телеманипулятор с эндоскопической камерой, вводимой в оперируемую область, управляемой педалями или голосовой программой компьютера, что позволяет хирургу устанавливать камеру, не прерывая операции. Система ЗЕВС крепится к столу по типу AESOP Robotic System и снабжена антитреморным фильтром и шкалой манипуляций в разбросе соотношений от 2:1 к 10:1.
Общая хирургия
Робототехнология была изначально предназначена для проведения лапароскопических вмешательств в брюшной полости. Первая операция по удалению желчного пузыря с применением лапароскопического робота-телеманипулятора была проведена в Брюсселе в 1997 г. Робот-ассистируемые хирургические технологии позволяют хирургам делать минимально возможные разрезы с наименьшим хирургическим стрессом. Данные технологии позволяют хирургам производить тонкие хирургические вмешательства в маленьком оперативном пространстве. Практически все операции в брюшной полости могут быть безопасно выполнены с применением данной технологии. Наиболее часто выполняемые операции включают в себя:
-
фундопликацию;
-
кардиомиотомию Геллера;
-
холецистэктомию;
-
колэктомию;
-
бариартрические вмешательства.
По сравнению с обычными лапароскопическими операциями робот-ассистируемая хирургия обладает рядом преимуществ, таких как трехмерное изображение, фильтр тремора и ненужных движений, оценка соотношения движений, обеспечивая при этом комфортное и эргономическое положение хирурга. К другим преимуществам относятся быстрая обучаемость, лучшее качество операций с одновременным упрощением последних на пациентах с высокой степенью ожирения, т.к. жесткость телеманипуляторов и инструментов позволяют противостоять натяжению и давлению массивных тканей. Хорошие отзывы от пациентов и их удовлетворенность результатами являются характерными чертами роботохирургии. В связи с тем, что отдаленные результаты операций с использованием роботов еще отсутствуют, то высокая цена подобных вмешательств может являться лимитирующим фактором для некоторых центров.
Особенности анестезиологического обеспечения
Во время операции осуществляется следующий мониторинг:
-
ЭКГ;
-
пульсоксиметрия;
-
температура;
-
непрямое измерение артериального давления.
Вследствие неудобного доступа к левой руке, венозные катетеры устанавливаются на обеих руках. Обычно выполняется ингаляционный наркоз. Мышечная релаксация крайне важна для обездвиживания пациента в то время, когда инструменты находятся внутри брюшной полости. Также производится катетеризация мочевого пузыря и устанавливается желудочный зонд. Конвекционный обогрев пациента обеспечивается принудительным обдувом теплым воздухом.
Пациент укладывается на спину, брюшная стенка стерильно обрабатывается, и через троакар в брюшную полость нагнетается углекислый газ до давления, не превышающего 20 мм рт. ст.
Вручную устанавливается троакар для камеры. Тележка с роботом устанавливается у головы пациента, для введения троакаров под контролем камеры. В связи с очень близким расположением к пациенту робот ограничивает доступ к воздуховодным путям и шее пациента.18,19 Голова пациента также должна быть защищена от случайной травмы движущимся манипулятором робота. После введения манипуляторов положение больного на столе не может меняться. Хирургическая бригада должна обладать навыками максимально возможно быстрого удаления манипуляторов из тела пациента в случае неотложной ситуации с воздуховодными путями или другой анестезиологической экстренностью. Как и при любой подобной лапароскопической операции с нагнетанием СО2 в брюшную полость, должны быть проведены соответствующие изменения в режиме вентиляции для удаления избыточного СО2.
По мнению хирургов, преимущества постановки катетера прямого артериального давления не всегда превышают риск. Данный вопрос должен обсуждаться для каждого конкретного пациента на основе оценки рисков и преимуществ.
Предоперационное исследование функции внешнего дыхания показано пациентам со значительной легочной патологией. Плохие результаты исследования ФВД могут являться противопоказанием к робот-ассистируемому вмешательству, в связи с плохой переносимостью однолегочной вентиляции. Роботохирургия может потребовать продленной однолегочной вентиляции на пределе нашего понимания ее физиологии. Чреспищеводная эхокардиография стала стандартным методом мониторинга и завоевала прочное место для безопасного выполнения некоторых робот-ассистируемых процедур.
Операции на митральном клапане и их анестезиологическое обеспечение
В 1997 г. две группы независимо друг от друга впервые опубликовали данные о робот-ассистируемых операциях на митральном клапане. В ноябре 2002 г. FDA утвердило данную процедуру для клапаносохраняющих операций на митральном клапане. Восстановительные операции на митральном клапане, изначально проводимые через миниторакотомию, могут быть проведены с полностью закрытой грудной клеткой. Тем не менее, при протезировании митрального клапана небольшая торакотомия продолжает оставаться необходимой для имплантации самого протеза.
Робот-ассистируемые операции на митральном клапане выполняются в некоторых центрах Европы и США. Первоначально пациентам проводится диагностическая коронарография и вентрикулография для оценки степени стеноза коронарных артерий и функции клапанов сердца. Выраженная митральная недостаточность является механической проблемой, для лечения которой необходимо оперативное вмешательство. Большинству пациентов с гипертонической болезнью проводится медикаментозное снижение постнагрузки такими препаратами, как ингибиторы АПФ. Увеличенные размеры левого предсердия часто приводят к фибрилляции предсердий. Пациенты с хронической фибрилляцией предсердий могут принимать антикоагулянты совместно с препаратами, контролирующими частоту сердечных сокращений. При наличии легочной гипертензии может развиться хронически повышенное давление в левом предсердии, ухудшающееся также при обструктивном заболевании легких. Больные с выраженной легочной гипертензией считаются неподходящими для робот-ассистируемого хирургического вмешательства.
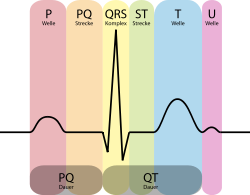
Прежде всего, устанавливается периферический венозный катетер большого калибра. Перед установкой двусторонних артериальных катетеров проводится легкая седация мидазоламом в сочетании с местным обезболиванием. Проводится двухканальный ЭКГ-мониторинг во II и V5 отведениях, пульсоксиметрия, артериальное давление измеряется через катетер в правой лучевой артерии для исключения неправильной позиции эндоартериального баллона. Современные ЭКГ-мониторы могут автоматически проводить анализ интервала ST для определения ишемии миокарда. После адекватной преоксигенации пациент вводится в наркоз комбинацией фентанила, мидазолама, изофлурана и мышечного релаксанта.
Трахея интубируется двухпросветной эндотрахеальной трубкой, правильное положение которой верифицируется бронхоскопом. После этого устанавливается датчик чреспищеводной эхокардиографии для контроля установки центрального венозного катетера и оценки функции сердца и клапанов. Датчик ЧПЭхоКГ устанавливается в средне-пищеводной позиции с углом кристаллов в 90° для выведения двухкамерной проекции при установке канюли в верхнюю полую вену. По технике Сельдингера устанавливается интродьюсер калибра 9 Fr, с последующим проведением катетера Свана-Ганца калибра 8 Fr в легочную артерию. Затем по методу Сельдингера через правую яремную вену устанавливается 17 Fr канюля Biomedicus, что подтверждается ТЭЭ. Как показывает опыт, для предотвращения перегиба и случайного передавливания зажимом для окклюзии аорты лучше использовать армированный венозный катетер. Во время введения канюли она промывается 5000 единицами гепарина для обеспечения проходимости. Канюля укрепляется кисетным швом на шее с последующим прибинтовыванием бинтом Керликса к голове пациента.
Пациент укладывается в положение на спине с наклоном правого плеча на 30° в левую сторону. Накладываются наружные пластины для электрокардиостимуляции и дефибрилляции. В зависимости от телосложения хирург определяет оптимальное положение для портов.
После выделения правых бедренных сосудов и начала левосторонней однолегочной вентиляции производится правосторонняя миниторакотомия.
Сердце выделяется после вскрытия перикардиальной сумки. Перикард фиксируется к наружной стенке грудной клетки двумя провизорными швами.
После гепаринизации по существующему протоколу АСТ канюлируются бедренная вена и артерия для подготовки к феморально-феморальному искусственному кровообращению. Сначала канюлируется бедренная вена, и под контролем ЧП ЭхоКГ венозная канюля калибра 21 Fr устанавливается по проводнику на уровне впадения нижней полой вены в правое предсердие. Одно торцевое и 12 боковых отверстий препятствуют спадению стенок канюли при высоком отрицательном давлении, создаваемом усиленными венозными роторными насосами. По такому же принципу канюлируется бедренная артерия канюлей 24 Fr, и начинается искусственное кровообращение с венозным дренажом из бедренной и яремной вен. Также устанавливаются канюли для антеградной и ретроградной кардиоплегии. В некоторых центрах предпочитают канюлировать восходящую аорту, используя канюлю Heartport Staright-Shot. Трансторакальный зажим проводится к восходящей аорте через правую аксиллярную область. Манипуляторы робота проводятся через соответствующие боковые троакары, в то время как камера проводится непосредственно через торакотомный надрез. Левое предсердие доступно для восстановления или замены митрального клапана.
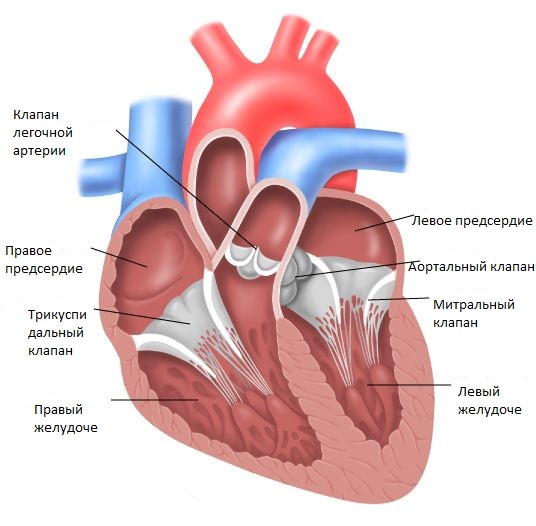
Перед окончанием искусственного кровообращения при помощи ЧП ЭхоКГ оценивается функция митрального клапана, степень остаточной митральной регургитации и подтверждается полная эвакуация воздуха из полостей сердца. Также оценивается передняя створка митрального клапана для проверки систолического захлестывания створки в выходной отдел левого желудочка.
Для оптимальных результатов очень важен отбор пациентов.
Устранение дефектов межпредсердной перегородки
Операции по устранению дефектов межпредсердной перегородки похожи на операции на митральном клапане, за исключением отсутствия необходимости в миниторакотомии. Операцию возможно выполнить при закрытой грудной клетке. Так же как и при других типах торакальной хирургии с использованием роботов, во время операции необходимо обеспечить однолегочную вентиляцию. Восстановление дефектов межпредсердной перегородки также требует изоляции сердца из кровотока, что достигается канюлированием внутренней яремной и бедренной вен и окклюзией путем перетяжки верхней и нижней полых вен. Искусственное кровообращение с кардиоплегией через корень аорты используется для работы на сухом сердце. Методы искусственного кровообращения с эндоваскулярным пережатием аорты описаны в разделе про шунтирование коронарных артерий.
Выделение внутренней грудной артерии
У пациентов осуществляется стандартный для кардиохирургии мониторинг. Центральный венозный и артериальный катетеры устанавливаются на стороне выделения маммарной артерии. Необходимо проводить однолегочную вентиляцию с использованием двухпросветной интубационной трубки, трубки Univent или бронхоблокатора с бронхоскопическим подтверждением положения трубки. Пациент находится на спине с наклоном на 200 вправо с помощью подкладывания валика под левую лопатку. Пластины наружного дефибриллятора наклеиваются на левую сторону спины и правую сторону грудной клетки. Приподнимание левой руки обеспечивает оптимальный доступ и натяжение кожи на стороне операции. Зеркальное отражение положения пациента используется при выделении правой маммарной артерии.
Для улучшения экспозиции и натяжения необходима инсуффляция CO. Нагнетание CO2 в левый гемиторакс отодвигает медиастинальную жировую ткань медиально, немного увеличивая пространство между грудиной и сердцем, улучшая видимость. Нагнетание CO2 в левый гемиторакс достаточно для выделения обеих маммарных артерий, потому что при выделении правой маммарной артерии сердце отклонено влево, улучшая угол доступа. Нагнетание выполняется поэтапно по 2-4 мм рт. ст. Поток нагнетания контролируется автоматически для достижения заданного предела давления. Особенно осторожно нагнетание производится у пациентов с гиповолемией или плохой функцией ЛЖ.
Объем циркулирующей крови должен быть восполнен перед полным нагнетанием CO2, что наряду с однолегочной вентиляцией несколько повышает ЦВД и давление в легочной артерии. Двусторонний пневмоторакс выполняется для выполнения двустороннего выделения маммарных артерий. По данным исследований, большинство пациентов спокойно переносят двусторонний пневмоторакс на протяжении 1 ч.
Аортокоронарное шунтирование
Всем пациентам перед АКШ выполняется ЧП ЭхоКГ для исключения незаращенного овального окна или левостороннего расположения верхней полой вены. Также проводится допплер-сонография подвздошных и бедренных артерий.
Подготовка пациентов к наркозу и мониторинг такие же, как и при операциях на митральном клапане. Обязательна установка артериального катетера в правую лучевую артерию, если планируется использование эндоваскулярного катетера с окклюзионным баллоном. После введения в наркоз мониторируются напряжения кислорода и углекислого газа. ЧП ЭхоКГ является общепринятым стандартным методом для определения функции сердца и подтверждения положения катетеров, так называемым «золотым стандартом». Катетер в легочной артерии используется по необходимости, т.к современные данные указывают на его избыточность при наличии данных ЧП ЭхоКГ.
Если ожидается использование искусственного кровообращения, то левая бедренная артерия канюлируется катетерами для периферического подключения ИК калибра 17 Fr или 21 Fr с баллоном для окклюзии аорты. Катетеры для периферического подключения ИК допускают поток крови около 4-5 л/мин. В них существует отдельный просвет для осуществления кардиоплегии в корень аорты за пределы зоны балонной окклюзии. Под контролем ЧП ЭхоКГ аортальная канюля устанавливается в восходящую аорту в 2 см от аортального клапана. Эндоваскулярный баллон надувается до диаметра, равного диаметру синотубулярного отдела аорты. Давление в баллоне достигает 300 мм рт. ст., и он полностью окклюзирует аорту. Остаточные потоки крови по краям баллона выявляются с помощью ЧП ЭхоКГ с применением цветового допплер-эффекта. Применение двусторонней канюляции лучевых артерий может быть использовано для определения миграции баллона к безымянной артерии. Проксимальная миграция баллона легко диагностируется ЧП ЭхоКГ и предотвращает грыжевое выпячивание баллона через аортальный клапан.
После завершения канюляции и готовности к искусственному кровообращению коллабируется правое легкое и начинается однолегочная вентиляция. Вентилятор настраивается так, чтобы давление CO2 в конце выдоха находилось в пределах 35-40 мм рт. ст. После достижения правостороннего пневмоторакса безопасно вводить порты. CO2 нагнетается в правый гемиторакс с давлением 5-10 мм рт. ст., что позволяет еще более коллабировать легкое и улучшить обзор. Также это может предотвратить смещение средостения в случаях вентиляции большим дыхательным объемом, как, например, у пациентов с эмфиземой легких. Само по себе нагнетание углекислого газа не достаточно для приподнятия грудины над передней поверхностью сердца, поэтому некоторые хирурги используют грудинные ретракторы для увеличения загрудинного пространства и улучшения экспозиции.
Робот-ассистируемое аортокоронарное шунтирование на бьющемся сердце может выполняться при соответствующем отборе пациентов. Шарнирный стабилизатор, проведенный через порт у мечевидного отростка, стабилизирует переднюю стенку сердца, улучшая наложения коронарных шунтов. Двустороннее выделение маммарных артерий также проводится с применением робот-асисстенции.
Хирургия мерцательной аритмии
В клинической практике мерцательная аритмия встречается довольно часто. Процедура лабиринта по Коксу часто является методом выбора при лечении медикаментозно-устойчивых форм фибрилляции предсердий, что дает отличные отдаленные результаты. При этой процедуре право- и левосторонняя атриотомии сочетаются с криоабляцией для разрыва путей обратного проведения импульса и восстановления синусового ритма. Такая процедура традиционно выполнялась в условиях искусственного кровообращения, но по мере эволюции таких технологий, как криотерапия, микроволновых и радиочастотных технологий новые, умещающиеся в руку приборы стали доступны для применения в минимально инвазивной хирургии.
Для минимально инвазивной абляции при фибрилляции предсердий применялись различные подходы. Наиболее часто используемым является метод с роботом Da Vinci с правосторонней миниторакотомией в условиях искусственного кровообращения. Также был описан полный эндоскопический метод на работающем сердце.
Этот раздел описывает метод полной эндоскопии на работающем сердце. Пациент укладывается на спину, в дополнение к стандартным мониторам устанавливаются катетеры для измерения артериального и центрального венозного давлений. Некоторым пациентам при необходимости устанавливается катетер в легочную артерию. После вводного наркоза трахея интубируется двухпросветной эндотрахеальной трубкой с подтверждением позиции последней фибробронхоскопией. Датчик ЧПЭхоКГ устанавливается для мониторинга функции сердца и исключения наличия тромба в ушке левого предсердия. На грудную клетку накладываются пластины наружного дефибриллятора. Проводится односторонняя вентиляция легких, исключая правое легкое, после чего в правый гемиторакс инсуффлируется CO. Выполняются три разреза по 1 см на уровнях 3-го, 4-го и 5-го межреберных промежутков по передне-подмышечной линии для введения портов манипуляторов робота и эндоскопа. После рассечения перикарда выделяется сердце. Микроволновым зондом непрерывно обжигается область вокруг легочных вен. Аритмии в раннем послеоперационном периоде купируются амиоадароном и в-блокаторами.
Установка электрода в левый желудочек
У многих пациентов с сердечной недостаточностью развивается сердечная десинхронизация вследствие запоздалой активации свободной стенки левого желудочка, что вызывает дальнейшее снижение его функции. Также десинхронизация может ухудшать митральную регургитацию и увеличивать смертность. Показано, что желудочковая ресинхронизация улучшает переносимость нагрузок, функцию желудочков и качество жизни в целом. Стандартная двухжелудочковая кардиостимуляция выполняется путем трансвенозного проведения правого предсердного и желудочкового эндокардиальных электродов. Эпикардиальный левожелудочковый электрод устанавливается путем канюлирования коронарного синуса в правом предсердии и дальнейшего проведения электрода на поверхность левого желудочка через впадающие вены. Сложность канюлирования коронарного синуса ведет к невозможности выполнения данной процедуры в 15-20% случаев. Выпадение электрода из стенки левого желудочка добавляет еще 5-10% к неуспеху процедуры. В таких случаях единственным выходом для пациента является установка эпикардиального электрода через миниторакотомный доступ. Некоторые группы применяют робот-ассистируемый подход.

В этой статье описан полный эндоскопический подход. После установки стандартных мониторов и артериального катетера трахея интубируется двухпросветной интубационной трубкой с верификацией позиции фибробронхоскопом. Устанавливаются датчик ЧП ЭхоКГ и катетер в легочную артерию. Пациент укладывается для заднелатеральной торакотомии. Проводится правосторонняя однолегочная вентиляция с выключением левого легкого. CO2 нагнетается в левый гемиторакс с давлением 8-10 мм рт. ст.
Манипуляторы робота вводятся через 5-й и 9-й межреберные промежутки по задне-подмышечной линии, а камера – в 7-м межреберье. Зонд-электрод водителя ритма вводится через рабочий порт и внедряется между первой и второй промежуточными артериями между основанием и верхушкой желудочка. Второй электрод укрепляется около второй промежуточной артерии, затем над электродами закрывается перикард. Оба электрода проводятся в подмышечную зону по тоннелю, и проводится повторное тестирование порога проводимости. Электрод с лучшим порогом проводимости подсоединяется к кардиостимулятору, в то время как второй закрывается колпачком и подшивается под фасцию с целью возможного использования в будущем. Если необходима правосторонняя электрокардистимуляция, то в то же время электрод проводится через вену и подсоединяется к бивентрикулярному водителю ритма. Данный подход обеспечивает надежный доступ в грудную полость для установки левосторонних электродов и доступ к сердцу для выполнения полного картирования.
Торакальная хирургия
Несмотря на то, что видео-ассистируемая торакальная хирургия хорошо отлажена, ее использование ограничено простыми вмешательствами. Немногие центры проводят сложные операции – такие, как лобэктомии и тимомэктомии, используя ВАТХ. Есть надежда, что робот-ассистируемая хирургия сможет превзойти ограничения обычной ВАТХ.
По сравнению с минимально инвазивными операциями, проводимыми на других регионах тела, торакальная хирургия имеет свои сложности. Препятствиями являются как ригидность стенки грудной клетки, так и подвижность сердца, легких и средостения. К анестезиологическим сложностям относятся длительная однолегочная вентиляция и нестабильная гемодинамика в связи с нагнетанием в гемиторакс CO2.
Укладывание пациента в правильную позицию играет основную роль в выведении областей, недоступных по-другому. Так как структуры средостения подвижны и тяжелы, они смещаются под воздействием гравитации. Положение на спине или небольшой боковой уклон 15-30° идеально подходят для патологии переднего средостения. Положение на боку может подойти для иссечения новообразований корня легкого и лобэктомий. Нагнетание CO2 также играет большую роль в адекватном хирургическом доступе, сдвигая средостение и легкое в противоположную сторону. Также оно уменьшает запотевание и задымление от электрокоагуляции; недостатком же является нестабильная гемодинамика.
По мере расширения применения робот-ассистируемой хирургии роль последней в торакальной хирургии также увеличилась. С ее помощью выполняются такие вмешательства, как кардиомиотомия Геллера, резекции новообразований пищевода, эзофагоэктомии, а также тимэктомии и резекции опухолей средостения.
Нейрохирургия
С 1980 по 1993 гг. нейрохирурги исследовали возможность применения роботов для точного установления инструментов в паренхиме мозга, с целью проведения минимально инвазивной операции и защиты окружающих здоровых тканей. Стереотактическая навигация во время нейрохирургических операций предопределила разработку видеонавигационной системы, позволяющей определять местонахождение кончика инструмента в реальном времени.
Система CyberKnife является видеонавигационной безрамочной системой для стереотактической радиохирургии опухолей спинного мозга. Основным преимуществом данной системы является возможность радиохирургического лечения на основе дневного стационара с быстрым вос- становлением. Безрамочная система – стереотактический робот NeuroMate использует данные ЯМР для лечения расстройств движения.
Медицинские роботы еще ждут своего часа, чтобы быть использованными в нейрохирургии. Объединение нескольких дисциплин, таких как роботехника, нанотехнология и точное компьютерное взаимодействие, может революционизировать нейрохирургию.
Урологическая хирургия
Впервые роботы в урологии были использованы в 1980-х гг., когда была разработана роботорама для трансуретральной резекции простаты. Рама была разработана для поддержания шести осей робота Unimate Puma. Безопасность данной рамы основана на стабильности циркулярной рамы, ограничивающей робота при выполнении точной дуги резекции. Операции с применением роботов выполняются быстрее, а поскольку гемостаз осуществляется только единожды, в конце процедуры, то время на абсорбцию ирригационной жидкости сокращается, в результате чего робот Puma может быть использован для безопасной резекции простаты.
Робот для чрескожного доступа PAKY-RCM был разработан в 1996 г., и в дальнейшем вытеснен системой Tracker в 2003 г. Работа этого робота сочетается с флюороскопией или компьютерной томографией для увеличения точности положения иглы для чрескожной нефролитотомии или биопсии тканей. Система AESOP также успешно применяется в лапароскопической хирургии простаты. Наиболее совершенными системами, используемыми в данное время, являются роботы Da Vinci. С их помощью выполняются такие процедуры, как:
-
радикальная простатэктомия;
-
радикальная цистэктомия;
-
радикальная и простая нефрэктомия;
-
нефрэктомия у живого донора;
-
пиелопластика;
-
адреналэктомия.
Радикальная простатэктомия
Guillonneau и Vallancein первыми показали возможности применения и эффективность лапароскопической простатэктомии. С тех пор многие центры успешно применяли робот-ассистированную радикальную простатэктомию, что сделало ее наиболее часто используемой операцией с робот-ассистенцией. С 2000 по 2004 гг. было выполнено 5200, а только в 2005 г. – уже более 8000 подобных операций.
Обучение данной технологии, видимо, происходит быстрее, чем обучение стандартному лапароскопическому доступу. Трансперитонеальный антеградный доступ, разработанный Ficarra и колл. в Vatikutti Institute of Urology в Детройте, является наиболее распространенным для РАРП. Такие показатели, как частота переливания крови, пределы здоровых тканей, восстановление удержания мочи, эректильная функция, говорят о преимуществе РАРП по сравнению с лапараскопическим или традиционным ретропубикальным доступами. Время операции также сравнимо с традиционным доступом за лонной костью после того, как хирург обучится РАРП.
После вводного наркоза устанавливается артериальный катетер для частого забора крови. Дополнительный большепросветный венозный катетер устанавливается, если потенциально возможна большая кровопотеря. Пациент укладывается на спину в литотомическое положение Тренделенбурга с наклоном 30°. Бедра максимально разводятся для помещения робота. Пациенты с ростом менее 180 см не укладываются в литотомное положение, а, напротив, ноги отводятся согнутыми в коленях. Долгое нахождение в положении Тренделенбурга относительно противопоказано пациентам после инсульта или с аневризмой мозговой артерии. Так как операция достаточно продолжительная, то все области, где тело пациента подвержено сдавлению, прокладываются гелевыми подушечками. Некоторые хирурги предпочитают укладку рук пациента с «пеленанием» до наркоза, для наибольшего комфорта и избегания сдавления нервов. Обработка и накрывание операционного поля проводится после установки мочевого катетера Фолея калибра 14 Fr. Пневмоперитонеум осуществляется через надрез в пупке до максимального давления 15 мм рт. ст. Троакары вставляются по стандартному протоколу Heilbronn – пять штук в полулунном порядке и один в над- пупочной области. Операция выполняется по модифицированной методике Montsouris.
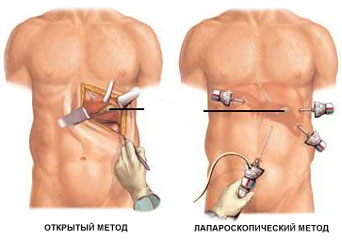
Радикальная цистэктомия
Уменьшение операционной кровопотери, времени госпитализации, послеоперационной боли являются преимуществами лапароскопического доступа. Недостатками данного метода являются его техническая сложность, требующая от хирурга виртуозности. В то же время данные о долговременных онкологических результатах являются недостаточными. Робот-ассистирумый доступ может стать промежуточным вариантом между открытым и лапароскопическим методами. Первые данные о серии подобных операций были представлены в 2003 г., и с того времени продолжают публиковаться отдельные наблюдения и маленькие серии.
В зависимости от сопутствующих заболеваний решается вопрос о постановке артериального катетера. Трахея интубируется однопросветной трубкой. Венозные катетеры большого диаметра вводятся, если предвидится массивная кровопотеря. Наркоз поддерживается летучими анестетиками. Предельно важно обеспечение полной мышечной релаксации, с целью избежания травмы от внедренных в брюшную полость робото-манипуляторов в случае непроизвольного движения пациента. В дополнение устанавливаются катетер в мочевой пузырь, желудочный зонд, и осуществляется согревание пациента обдуванием теплым воздухом. Пациент укладывается в литотомическое положение с наклоном головного конца стола вниз на 45°. Силиконовые гелевые защитные подушки на места сдавления применяются для предотвращения пролежней в связи с длительностью операции.
Робот системы в ортопедической хирургии
Система «Да Винчи» с шестиразрезным доступом применяется для выполнения тазовой лимфаденэктомии и цистопростатэктомии. Удаленный орган извлекается через разрез в 5-6 см над лонным сочленением. Через этот же разрез выводится наружу кишка и формируется новый мочевой пузырь, а затем накладывается уретронеовезикальный анастомоз с помощью робота. В целом отмечается уменьшение кровопотери и времени госпитализации при робот-ассистируемом вмешательстве по сравнению с открытым доступом.
Во время этой процедуры бедренный имплант вставляется в проксимальный отдел центрального канала бедренной кости с тугой фиксацией путем вдавливания или приклеивания в канале. Результаты отсроченного рентген-контроля после замены тазобедренного сустава показали растрескивание клея, приводящее к ослаблению крепления с последующим разрушением костной ткани, что приводило к неудаче операции. Современные импланты обладают пористой структурой, для прорастания костной ткани внутрь, продлевая положительный эффект операции. Именно по этой причине необходима тугая фиксация импланта в канале бедренной кости.
Канал в бедренной кости, формируемый роботом, в 10 раз более точен, чем выполненный вручную под контролем глаза. Робот использует данные ЯМР и КТ для определения визуальных точек координат. Точное трехпространственное позиционирование координат бедренной кости необходимо для фрезерования прецизионного канала для внедрения хирургического протеза. Для этого нога пациента обследуется на КТ, и компьютер создает трехмерные модели самой кости и точек крепления.
В операционной хирург обычно удаляет головку бедренной кости и вставляет суставную чашечку вручную. Бедренная кость жестко укрепляется фиксатором робота. Робот распознает три титановых позиционных датчика и сопоставляет их позицию с позицией, полученной на компьютерном томографе. Таким образом, робот точно определяет, как расположена бедренная кость в трехмерном пространстве для выполнения сверхточного фрезерования канала. Остальные этапы операции заканчиваются вручную.
В данное время существует 4 робот системы для ортопедической хирургии, включая Acrobot system, ROBODOC system, P1 Galileo Nav system и CASPER system. Первое рандомизированное многоцентровое исследование сравнивало систему ROBODOC и установку штифта протеза вручную. Результаты показали меньший зазор и отсутствие интраоперационных переломов кости при применении робот системы. Кровопотеря и время операции, однако, также были значительно большими в случаях использования ROBODOC. В 2001 г. FDA утвердила еще одно многоцентровое исследование ROBODOC с бесскрепочной системой. Целью данного исследования было доказать эффективность данной системы, уменьшить время операции и снизить кровопотерю во время ROBODOC-асисстируемых операций. Было продемонстрировано снижение кровопотери и сокращение времени операции по сравнению с первым многоцентровым исследованием.

Более позднее исследование показало увеличение частоты дислокации суставов и необходимости повторного хирургического вмешательства при использовании ROBODOC-ассистируемой технологии при первичной имплантации тазобедренных суставов по сравнению с ручным методом. Предполагалось, что эти осложнения возникали в связи с повреждением приводящих мышц. Описанные осложнения были отнесены к человеческой ошибке, так как в проходящем сейчас исследовании они не отмечены.
Замена коленного сустава
Большинство полных замен коленных суставов зависит от установки позиции пилы, которая устанавливается под визуальным контролем экспозиции кости хирургом. Неточности провоцируют надколенно-феморальную боль и ограничение суставной подвижности у 40% пациентов при обычных операциях. Неточность в 2,5 мм может привести к 20% нарушению амплитуды подвижности сустава.
Робот системы были разработаны для увеличения точности выравнивания суставного протеза. Роботу необходимо распознать ориентиры, для этого фиксируется положение таза и лодыжки на операционном столе, так как костный материал сохраняет форму и с меньшей вероятностью деформируется под давлением. Небольшие исследования показали улучшение точности операций при использовании роботосистем в хирургии коленного сустава.
Высочайшая точность необходима, поскольку сосуды глаза находятся на расстоянии 25 мкм от сетчатки. Сотрудничество лаборатории реактивных двигателей NASA и Charles привели к разработке робот-ассистируемой микрохирургической системы, способной проводить хирургические вмешательства с точностью до 10 мкм. Простой человеческий глаз может различать расстояния только до 200 мкм. Робот системы снабжены стабилизационно-трекинговой системой для отслеживания движения глаз с частотой 200 Гц, что позволяет получать неподвижное изображение оперируемого глаза. Также данная система увеличивает изображение в масштабе 100:1 и позволяет различать расстояние в 10 мкм. Тремор отфильтровывается в пределах частот от 8 до 14 Гц, для удаления неточности движений.
Проводить операции с такой или большей точностью – явное преимущество роботосистем, без которых подобные операции были бы немыслимы.
Использование роботов в хирургии с большой вероятностью будет расширяться, в связи с их высоким уровнем точности и контролируемости. Так как робот-ассистируемые операции являются минимально инвазивными, стресс, общая болезненность, тканевая травма и время госпитализации сокращаются. Также улучшаются послеоперационное восстановление и косметические результаты.
Анестезиологи должны быть в курсе изменений этой быстро развивающейся области и знать, как это влияет на проведение наркоза. Изначально техника торакальных операций с использованием робота увеличила продолжительность требуемой общей анестезии. Длительность однолегочной вентиляции была доведена до предела в связи с глубоким пониманием особенностей ее физиологии. По мере накопления опыта хирургами ожидается, что время операций будет значительно сокращаться до времени обычных открытых операций. Необходимость полной неподвижности пациента во время роботохирургии и невозможность использовать физиологию гравитации для воздействия на внутрисердечное давление принуждает к более частому использованию фармакологических препаратов.
Анестезиологи научились работать на удалении от воздухоносных путей пациента и должны быть готовы к применению роботосистем на верхней половине тела. Системы удаленного мониторинга необходимы для обеспечения практически безопасного наркоза. Вероятно, что «миниинвазивная» революция потребует более быстрого восстановления больного, что усилит роль регионарной анестезии. Уменьшение хирургического стресса приведет к практическому уменьшению воспалительного ответа организма.
Началась новая эра практического применения роботов в хирургии и улучшения качества помощи. В будущем робот станет менее механической и более информационной системой, взаимодействующей с другими системами. Последним достижением в робот системах явилась возможность наложения компьютерно-сканированных изображений на хирургическое поле в реальном масштабе времени во время операции. Анатомические структуры выглядят прозрачными, и жизненно-важные структуры могут выделяться для лучшего обзора. Предоперационная имидж-диагностика в комбинации с виртуальной реальностью позволят хирургу отрабатывать сложные операции на тренажерах перед самой операцией с целью избегания повреждения жизненно важных тканей во время самой операции. Сейчас разрабатываются системы, улучшающие визуализацию подвижных органов, таких как сокращающееся сердце, что позволит видеть сердце как неподвижное. Технология использует синхронизированный с сердечным ритмом стробоскоп, что позволяет получить неподвижное или виртуально неподвижное изображение сердца.
Нанотехнология – еще одна область, где применяются медицинские роботы. В наши дни размеры самого маленького автономного робота достигают всего 250х100 мкм. В будущем нанороботы будут ипользоваться для доставки агентов для целевой генной или химиотерапии в любые участки тела. Как и всегда, однако, все новшества должны восприниматься с известной долей осторожности.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания







Комментарии