Повреждение сосудов при операции на конечностях. Диагностика и оперативное лечение повреждений нервов
Если мобилизация тыльной плюсневой артерии обычно не вызывает затруднений, то подошвенная – требует при своем выделении особой осторожности, поскольку всегда проходит под головкой I плюсневой кости в непосредственной близости от сухожилия длинного сгибателя большого пальца, отдавая при этом весьма короткие ветви к окружающим тканям.
У детей с отсутствием тыльной артерии стопы и преимущественным развитием системы задней большеберцовой артерии выделение начинают от области развилки пальцевой артерии в проксимальном направлении, при этом длина сосудистой ножки ограничивается размерами плюсневых костей.
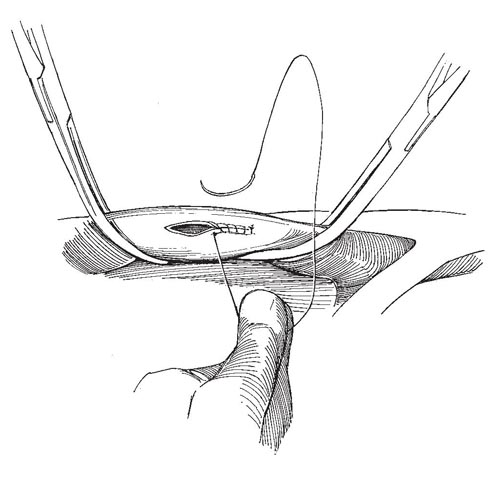
Одновременно с мобилизацией артерий выделяют подошвенные пальцевые нервы. Последние расщепляют интрафасцикулярно в области общепальцевых стволов и заимствуют, как с наружной, так и с внутренней стороны трансплантата.
На тыле стопы пересекают сухожилия разгибателей II пальца, на подошвенной поверхности после рассечения подошвенного апоневроза выделяют сухожилия сгибателей, причем поверхностные – отсекают у места входа в трансплантат, глубокие – максимально проксимально.
Если палец, используемый для пересадки, необходимо взять лишь на уровне фаланг, то производят капсулотомию плюснефалангового сустава, при заимствовании трансплантата вместе с плюсневой костью выполняют ее остеотомию на необходимом уровне.
После проведенных манипуляций палец остается связанным со стопой лишь сосудистой ножкой. Далее снимают жгут и оценивают кровоснабжение трансплантата. При отсутствии технических погрешностей во время заимствования он обычно в течение 1-2 мин приобретает нормальные цвет и температуру.
Выделение и подготовку для пересадки блока II-III пальцев стопы проводят идентичным образом, выделяя лишь двойное количество сухожилий и нервов.
Палец оставляют связанным со стопой, вплоть до момента полной подготовки реципиентной зоны на кисти, что позволяет уменьшить время ишемии трансплантата до минимума.
-
Подготовка реципиентной зоны на кисти.
На кисти разрезы проводят в области планируемого для реконструкции пальца, начиная от его кончика и далее по тылу и ладонной поверхности в проксимальном направлении.
При наличии культи основной фаланги или пястной кости обнажают их дистальный конец, сухожилия фиксируют на держалки, нервы маркируют или фиксируют к боковым поверхностям разреза.
В области анатомической табакерки или на передней поверхности предплечья выделяют лучевую артерию и V. cefalica или V. basilica. Иногда в качестве питающих сосудов выделяют ладонные общепальцевые артерии или ладонную артериальную дугу.
После снятия жгута производят тщательный гемостаз и приступают к следующему этапу оперативного вмешательства.
После полной подготовки реципиентного участка сосуды трансплантата на стопе перевязывают и пересекают, палец переносят на кисть, помещают в позицию планируемого для реконструкции сегмента и фиксируют одной осевой спицей.
После этого на ладонной поверхности сшивают сухожилия сгибателей, пальцевые нервы, используя эпиневральные швы. На тыле проводят восстановление целости сухожилий разгибателей, после чего приступают к сосудистому этапу вмешательства.
При наличии замкнутой ладонной артериальной дуги, в области анатомической табакерки перевязывают дистальные концы лучевой артерии и головной вены, накладывают анастомозы конец в конец между их проксимальными фрагментами и сосудами трансплантатов. Диаметр сшиваемых сосудов в данной зоне, в зависимости от возраста ребенка и вида патологического состояния, составляет 0,7-1,8 мм.
После снятия клипс с артерии и вены и восстановления кровотока послойно зашивают раны на кисти и стопе, используя при необходимости различные варианты кожной пластики.
Указанным образом можно поступать при пересадке II или блока II-III пальцев стопы. При раздельной пересадке пальцев обеих стоп требуется подключение двойного количества сосудов в операционной ране.
В отношении восстановления вен особых трудностей не возникает, поскольку на кисти они, даже при самых тяжелых степенях недоразвития, могут быть обнаружены в необходимом количестве на уровне лучезапястного сустава или дистальной трети предплечья.
Что касается восстановления артериального кровотока, то могут быть использованы следующие основные варианты данного этапа операции.
В первом из них во время выделения артерии на стопе, на одном из пальцев максимально возможно мобилизуют фрагмент глубокой подошвенной ветви, уходящей на подошвенную поверхность стопы у основания первого межплюсневого промежутка. Ее перевязывают и пересекают, включая в состав сосудистой ножки. Артерию второго трансплантата заимствуют обычным путем.
После переноса на кисть артерию первого трансплантата подключают к проксимальному концу лучевой артерии, а второго – к фрагменту глубокой подошвенной артерии первого трансплантата. В результате оба трансплантата кровоснабжаются из одного ствола.
Вместе с тем при указанном способе у значительной части больных отмечается так называемый синдром обкрадывания, когда при малейшем затруднении кровотока в одном трансплантате происходит его перераспределение с развитием ишемических нарушений в данном сегменте. В связи с этим мы в последние годы используем другой вариант подключения сосудов, при выполнении которого основным условием является наличие замкнутой артериальной дуги.
Лучевую артерию выделяют в области анатомической табакерки, после ее пересечения к проксимальному концу подключают артерию одного, к дистальному – другого трансплантата. Тем самым добиваются раздельного питания пересаженных сегментов из бассейна лучевой артерии и через ладонную дугу – локтевой артерии.
При наличии сохранившегося остатка основной фаланги или головки пястной кости, трансплантат берут со стопы после капсулотомии плюснефалангового сустава, причем отмечены хорошие функциональные исходы при сопоставлении головки пястной кости и суставной поверхности основной фаланги пальца стопы. Подобное комбинированное формирование сустава уже в ближайшие месяцы после операции обеспечивает значительный объем активных и пассивных движений.
При значительном укорочении пястных костей трансплантат заимствуют вместе с плюснефаланговым суставом и дистальным концом плюсневой кости, что дает несколько худшие функциональные исходы и вместе с тем обеспечивает вполне приемлемый косметический результат.
Визуально линейные размеры перенесенных на кисть сегментов превышают их длину на стопе. Подобные результаты объясняются тем, что на стопе межпальцевая складка находится на уровне дистальной трети основной фаланги или проксимального межфалангового сустава, маскируя истинную, костную длину сегмента, проявляющуюся после устранения базальной синдактилии на кисти.
В послеоперационном периоде применяют инфузионную терапию, включающую в себя антикоагулянты, ингибиторы сосудисто-тромбоцитарного гемостоза, препараты, расширяющие периферические сосуды, а также улучшающие микроциркуляцию и реологические свойства крови. Многие хирурги вообще не применяют медикаментозное лечение в послеоперационном периоде. Однако в детской хирургии применение данных средств оправданно, что связано с особенностями детского организма.
При гладком течении послеоперационного периода после выполнения микрохирургических пересадок пальцев стопы на кисть иммобилизацию прекращают через 3-4 недели, после чего назначают курс восстановительного лечения, включающий в себя ЛФК, массаж, ФТЛ.
-
Крайние варианты использования аутотрансплантации пальцев стоп.
Крайние уровни отчленения, т. е. 1-й уровень и 5-й требуют взвешивания всех факторов «за» и «против», на основании чего выбирается метод реконструкции сегментов кисти.
Функция кисти при 1-м уровне ампутации пальца практически не нарушается. В данном случае имеется преимущественно косметический дефект, в основном связанный с отсутствием ногтевой пластинки. В большинстве случаев данный дефект не нуждается в оперативном лечении.
Выделение сосудисто-нервного пучка дистального фрагмента пальца стопы связано с некоторыми техническими трудностями и риск возникновения сосудистых нарушений в послеоперационном периоде повышается.
Несмотря на это, некоторые пациенты настаивают па реконструкции ногтевой фаланги пальца.
Наименее благоприятным для реконструкции функционирующего пальца является 5-й уровень отчленения – полная травматическая ампутация луча.
В случае отсутствия большого пальца основным недостатком является повреждение основного сустава, играющего важную роль в его подвижности, а также группы мышц тенара, что снижает возможности активной функции восстанавливаемого сегмента. В таких случаях сохранение полноценных четырех или трех лучей кисти является показанием к поллицизации. Однако при восстановлении кисти с дефектами трех и более лучей отдают предпочтение микрохирургической аутотрансплантации пальца стопы. При этом трансплантат выделяют вместе с плюсневой костью.
Полное отсутствие луча обычно является показанием для косметического протезирования, так как пересадка пальца стопы малоудовлетворительна в косметическом отношении из-за разницы как в длине, так и во внешнем виде пальцев стопы и кисти. Однако при значительных повреждениях или отчленениях нескольких пальцев кисти пересадка пальцев стопы является единственным вариантом восстановления функции кисти.
Таким образом, аутотрансплантацию пальцев стопы необходимо производить по определенным показаниям, после всесторонней оценки степени повреждения сегментов и функциональных структур кисти и предплечья. Однако даже при крайних вариантах отчленения пальцев кисти данный метод реконструкции является более эффективным по сравнению с другими.
Примеры использования аутотрансплантации пальцев стоп при крайних вариантах посттравматических культей пальцев кисти.
-
Девочка 14 лет, поступила на отделение реконструктивной микрохирургии с диагнозом: ампутационные культи II-III пальцев правой кисти на уровне дистальных межфаланговых суставов. И родители, и сама пациентка настаивали на восстановлении ногтевых фаланг, отказываясь от косметического протезирования. Произведена свободная пересадка ногтевых и частично средних фаланг II пальцев с обеих стоп. Через полгода произведена завершающая косметическая кожно-пластическая операция.
-
Мальчик 11 лет, поступил с диагнозом: «последствие взрывной травмы левой кисти, ампутационные культи I, II, V пальцев на уровне основных фаланг, полная ампутация III-IV лучей кисти». По функциональным и косметическим соображениям решено восстановить III-IV лучи кисти методом пересадки II пальцев обеих стоп вместе с плюсневыми костями. Через 6 месяцев после операции ребенку поэтапно производили удлинение основных фаланг I и II, V пальцев кисти. Таким образом, удалось восстановить вес пальцы кисти, необходимой для функции длины.
Ошибки и осложнения при микрохирургической пересадке пальцев на кисть.
Критический анализ ошибок и осложнений серии достаточно однотипных оперативных вмешательств всегда полезен для улучшения исходов лечения и совершенствования используемых методик. В микрохирургии данный вопрос является чрезвычайно актуальным, поскольку пересадки кровоснабжаемых комплексов тканей образно характеризуют как методы, приводящие либо к блестящей победе, либо к сокрушительному поражению при весьма ограниченном числе промежуточных вариантов.
Считаем целесообразным разделять все имеющиеся осложнения на три основные группы:
1) ближайшие, которые возникли в ходе оперативного вмешательства и первые два часа послеоперационного периода;
2) ранние, наступившие в первые 3 суток после хирургического вмешательства;
3) поздние, развившиеся на 4-15-е сутки после операции.
При рассмотрении первой группы осложнений целесообразно выделять следующие, наиболее типичные, погрешности хирургических вмешательств.
Возможные повреждения сосудов при выделении трансплантатов, что отмечается при сложных анатомических взаимоотношениях во время заимствования пальцев стопы, причем наиболее часто это происходит на уровне входа в ткани трансплантата, где диаметр сосуда не превышает 0,3-0,5 мм. Одной из причин подобного может быть чрезмерное обескровливание конечности, затрудняющее идентификацию артерии, а также ее совершенно атипичное положение.
Стойкие спазмы артерий после снятия жгута могут возникнуть при травматическом выделении сосудов, коагуляции мелких ветвей в непосредственной близости от стенки магистрального ствола, взятии артерии без определенного количества паравазальных тканей, служащих как бы буфером от непосредственного воздействия на адвентицию. Кроме того, следует отметить склонность к спазму у детей младшего возраста, который довольно быстро приобретает стойкий характер и с трудом поддается ликвидации.
Неправильный выбор магистрального ствола артерии при недостаточно тщательной оценке взаимоотношений тыльной и подошвенной плюсневых артерий и взятие трансплантата лишь на одной из них могут привести к недостаточности артериального кровотока с развитием ишемических нарушений в планируемом к переносу пальце.
Наиболее типичной ошибкой при подготовке реципиентной зоны на кисти является неадекватный выбор артерии и вены. Иногда подготовка сосудов в типичных местах и последующее их анастомозирование с сосудами трансплантата могут не обеспечить адекватной перфузии тканей по причине малого объемного кровотока. Это особенно часто наблюдается, когда перемещаемый комплекс тканей по своей массе приближается к объему сохранившихся сегментов кисти.
Тромбозы артериального и венозного анастомозов в ближайшие 2 ч. после операции отмечаются крайне редко и связаны, в основном, с техническими погрешностями.
Ранние осложнения, наступающие в ближайшие сроки после операции, имеют совершенно четкий временной промежуток – конец 2-х – начало 3- х суток послеоперационного периода, так называемые «тромбозы третьих суток». Их появление вполне объяснимо, поскольку к этому периоду на кисти наступает пик отека, и при максимальном сдавлении мягких тканей, прежде всего, начинаются нарушения венозного оттока.
При несвоевременной диагностике данного осложнения у детей довольно быстро присоединяются нарушения артериального кровотока. Палец первоначально имеет цианотичный оттенок, затем становится пятнистым, участки багрово-фиолетового цвета чередуются с мраморными.
При выжидательной тактике уже в ближайший час после развития осложнения превалирует прекращение артериального кровоснабжения с выраженным поведением пальца и резким снижением его температуры.
Помимо отека тканей, причиной развития данной ситуации может быть гематома в области анастомозов, возникшая вследствие недостаточно тщательного гемостаза в процессе операции, которая, естественно, увеличивает механическое давление в данной зоне. Следует отметить, что эта группа осложнений является наиболее частой в клинической практике пересадок пальцев стопы.
К поздним осложнениям, которые отмечаются весьма редко, могут быть отнесены нагноения послеоперационных ран и эрозивные кровотечения.
Нагноения являются следствием многократных повторных хирургических вмешательств для восстановления кровотока в пересаженных комплексах тканей, причем они могут развиваться, несмотря на интенсивное применение антибиотиков широкого спектра действия.
Источником эрозивных кровотечений могут быть области сосудистых анастомозов, причем данный вид неблагоприятного течения послеоперационного периода является казуистикой.
-
Повторные хирургические вмешательства.
При рассмотрении повторных хирургических вмешательств, проводимых по поводу перечисленных выше осложнений, следует обратить внимание на следующее.
Профилактикой спазма сосудов являются аккуратные манипуляции с ними, минимально возможное время обескровливания конечности, адекватное анестезиологическое обеспечение, местное применение спазмолитиков. К сожалению, в ряде случаев спазм артерий бывает настолько значительным, что его не удается преодолеть даже гидравлической и механической дилатацией, тогда участок сосуда приходится резецировать и использовать венозную вставку.
Наиболее сложной является борьба с осложнениями, наступающими на 2-3-и сутки послеоперационного периода. Основным условием профилактики последних является предупреждение натяжения мягких тканей. Зашивание раны с натяжением должно быть предупреждено использованием различных вариантов кожной пластики. Натяжение тканей па пике отека может привести к сдавлению сосудов трансплантата с развитием вначале признаков венозного тромбоза. В данной ситуации бывает вполне достаточным снятие части кожных швов, ликвидация напряжения тканей с весьма быстрой компенсацией кровотока. Также очень эффективно применение трудотерапии.

Если неоперативные мероприятия безуспешны, то приходится осуществлять повторное хирургическое вмешательство, во время которого используют следующую последовательность действий.
Обнажают области артериального и венозного анастомозов, тщательно прослеживают путь сосудов до места их входа в трансплантат, при необходимости ликвидируются гематомы.
Снимают несколько швов с венозного анастомоза, после чего восстанавливают проходимость артерии. Контроль за восстановлением кровообращения осуществляют по появлению венозной крови, и повторно шов на вену накладывают только при получении адекватной перфузии трансплантата.
Вместе с тем у значительного числа больных этой группы диагностируют так называемый синдром блокады венозного оттока, при котором артерия клинически проходима до области входа в трансплантат, а последний остается обескровленным и из вены не получают ни капли крови. Данное состояние обусловлено тромбообразованием на уровне артериол и капилляров, с которым редко удается справиться медикаментозными средствами и физическим воздействием на сосуды трансплантата. Одним из вариантов борьбы с этим осложнением является переключение кровотока на вторую собственную пальцевую артерию. В ряде случаев получают довольно быстрый клинический эффект со стабильным восстановлением кровотока. По всей вероятности в данном случае речь идет о включении в работу дополнительных, ранее не задействованных артериовенозных шунтов. При безуспешности всех перечисленных мероприятий последним и единственным шансом является применение тромболитиков.
Если кровообращение в трансплантате не восстанавливается, то единственно возможным способом его сохранения является следующий. С пересаженного сегмента удаляют кожу, подкожную жировую клетчатку, фасции, оставляя лишь костно-суставно-сухожильный трансплантат. В области груди формируют острый стебель по Блохину-Конверсу, в свободный конец которого погружают обработанный палец.
Подводя итог всему сказанному, можно отметить, что наиболее надежной профилактикой осложнений при микрохирургической пересадке пальцев стопы на кисть являются четкое знание анатомии донорского и реципиентного участков, предельно аккуратное взятие трансплантата, надежный гемостаз на кисти, тщательное наложение сосудистых анастомозов, постоянный контроль в послеоперационном периоде и, при необходимости, раннее повторное хирургическое вмешательство.
Диагностика и оперативное лечение повреждений нервов
По этиологии:
Механические повреждения:
-
открытые повреждения – огнестрельные, резаные, колотые, рубленые, рвано-ушибленные и др.;
-
закрытые повреждения – ушиб, тракция, сдавление; хроническая травма нерва, вывих нерва.
Термические повреждения: ожоги, электроожоги.
Химические повреждения: инъекции лекарственных и других веществ.
По степени повреждения:
-
полное нарушение проводимости;
-
частичное нарушение проводимости.
По локализации: сторона повреждения.
Сочетанные повреждения:
-
с сухожилиями, мышцами, сосудами, костями, суставами;
-
повреждения нерва при травме различных органов, при травме головного и спинного мозга.
Комбинированные повреждения:
-
повреждение нерва и лучевая болезнь;
-
повреждение нерва и поражения боевыми отравляющими веществами;
-
повреждение нерва и ожоговая болезнь.
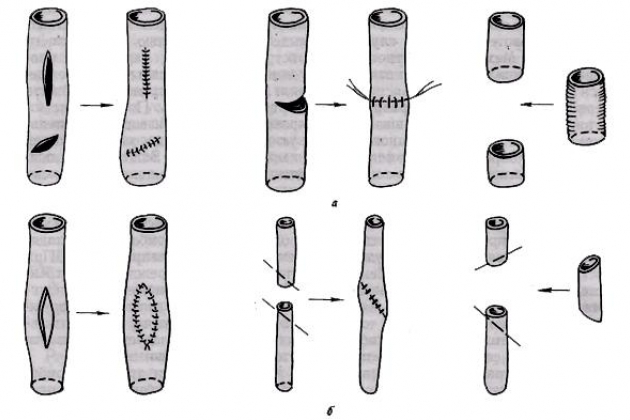
Показания к наложению шва на нерв и невролизу при открытых повреждениях. При резаных, колотых, рубленых, рваных ранениях конечности и полном нарушении проводимости нерва показано наложение шва па нервный ствол. При частичном нарушении проводимости нерва в этих случаях показана ревизия нерва с уточнением объема операции после осмотра нерва в ране и проведения электродиагностики на обнаженном нервном стволе. При наличии грубых внутриствольных изменений производят резекцию измененного участка нерва с последующим наложением шва. В остром периоде травмы на операции чаще находят анатомический перерыв части нерва. В таких случаях неповрежденные пучки нерва сохраняют, поврежденные экономно освежают и накладывают межпучковый шов, используя при этом микрохирургическую технику. Через несколько недель или месяцев после травмы частичное нарушение проводимости нерва не всегда является показанием для операции. При нарушении проводимости нерва, когда сила иннервируемых им мышц и чувствительность оцениваются в 4 балла, показано неоперативное лечение. Если нарушение проводимости нерва более глубокое, то следует провести интенсивные курсы неоперативного лечения в течение 1-2 мес. При неэффективности его показано оперативное вмешательство. Объем операции уточняют в ходе самой операции.

Так, если при осмотре и пальпации не находят грубых внутриствольных изменений, электропроводимость нерва сохранена – показан внешний невролиз. Если при осмотре и пальпации находят боковую неврому, захватывающую часть пучков нерва, то показана резекция измененной части нерва с последующим наложением межпучкового шва с использованием микрохирургической техники. Если при осмотре и пальпации находят неврому, захватывающую весь поперечник нерва, то возможны два тактических варианта: при отсутствии электропроводимости нерва производят резекцию измененного участка нерва н наложение шва, при наличии хотя бы минимальной электропроводимости операцию можно закончить внешним невролизом и подвести электроды для стимуляции.
При огнестрельных ранениях нервов тактика лечения складывается совершенно по-особому, что связано со смешанным механизмом воздействия на нервные стволы и обширностью поражения. При ПХО раны необходимо накладывать шов на полностью прерванные нервные стволы. Однако в связи с тем, что у некоторых пациентов с огнестрельным ранением нарушение проводимости нервов связано с сотрясением, которое обусловлено высокой кинетической энергией ранящего снаряда, резекция неповрежденных нервов при ПХО не показана. Показания к повторному оперативному вмешательству на таких нервах обычно выясняются спустя 2-4 мес. после ранения и позже, когда исчезнут явления, вызванные сотрясением нервного ствола, и останутся стойкие неврологические выпадения, обусловленные тяжелыми морфологическими внутриствольными изменениями. Если спустя 1-2 мес. после огнестрельного ранения неврологическое и инструментальное исследование выявляет синдром полного нарушения проводимости нерва или выявляется синдром глубокого нарушения проводимости нерва при полной неэффективности активно проводимого неоперативного лечениям, показана ревизия поврежденного нерва. При ревизии обязательно использование микрохирургической техники и оптического увеличения, при этом производят осмотр нерва, пальпацию его для определения внутриствольного уплотнения, проведение электродиагностики обнаженного нервного ствола. При обнаружении отчетливых изменений в нерве, при отсутствии электропроводимости его показана резекция измененного участка нерва с последующим наложением шва. При отсутствии отчетливых изменений в нерве при наличии даже минимальных признаков проводимости обнаженного нерва показано проведение невролиза и подведение к нерву электродов или введение их субэпиневрально для длительной электростимуляции в послеоперационном периоде в течение 2-4 недель.
-
Показания к наложению швов на нерв и невролизу при закрытых повреждениях.
Закрытые повреждения нервных стволов в мирное время встречаются довольно часто, они могут произойти в результате ушиба, тракции или сдавления. Типичным примером ушиба нерва является повреждение локтевого нерва при травме локтевой области, которую в течение жизни испытывает почти каждый человек, при этом пострадавший ощущает как бы удар током в V палец, в область мышц гипотенара с онемением этой зоны. Чувство онеменения в зависимости от тяжести травмы длится от нескольких минут до нескольких часов.
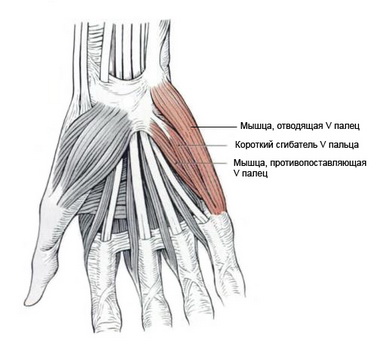
Обычно при ушибах нерва с частичным нарушением проводимости в течение нескольких недель после курса неоперативного лечения наступает восстановление функции нерва. Если ушиб нерва вызвал полное или глубокое нарушение его проводимости со снижением силы иннервируемых мышц и чувствительности до 1-2 баллов, с отсутствием эффекта от неоперативного лечения, то показано оперативное вмешательство – ревизия нерва с проведением электродиагностики на открытом нерве с уточнением объема операции.
Характерным примером тракционного повреждения является повреждение плечевого сплетения при затягивании руки в транспортер. По мнению многих авторов, оперативное вмешательство при закрытых тракционных повреждениях плечевого сплетения, как правило, не показано. При закрытом тракционном повреждении плечевого сплетения оперативное лечение не показано двум группам больных:
-
больные, у которых нарушение проводимости стволов плечевого сплетения частичное и в результате неоперативного лечения идет процесс восстановления проводимости нервов с улучшением полезной функции конечности;
-
больные, у которых имеет место закрытое тракционное повреждение всех стволов плечевого сплетения с полным нарушением проводимости при большом сроке, прошедшем после травмы, при наличии грубой атрофии мышц руки и плечевого пояса, их паралича, полном перерождении мышц, отсутствии электропроводимости стволов плечевого сплетения, анестезии кисти и предплечья, наличии выраженных трофических нарушений; обычно у таких больных оперативное вмешательство не приводит к положительным результатам.
Наиболее тяжелый прогноз при сочетании повреждения плечевого сплетения и подключично-подмышечной артерии со значительным нарушением кровообращения.
Оперативное вмешательство показано больным следующих групп:
1) больные с тракционным повреждением плечевого сплетения с полным нарушением проводимости всех стволов в ранние сроки после травмы; если при ревизии обнаруживается перерыв ствола, то показано его сшивание; при большом дефекте, когда концы нерва сшить не удается, показано сшивание разноименных нервов; в качестве невротизатора можно использовать диафрагмальный нерв, межреберные нервы и др.;
2) больные с тракционным повреждением плечевого сплетения с полным нарушением проводимости одного или нескольких стволов; показана ревизия поврежденного ствола, желательно в первые полгода — год после травмы; при полном перерыве ствола плечевого сплетения показана реконструкция его; если анатомическая целость ствола плечевого сплетения сохранена, то производят тщательный внешний невролиз его и подводят к стволу или вводят субэпиневрально электроды для долгосрочной электростимуляции в послеоперационном периоде;

3) больные с тракционным повреждением плечевого сплетения С частичным нарушением проводимости одного или всех первичных или вторичных стволов; оперативное вмешательство показано, когда проводимое в течение 3-6 мес. неоперативное лечение не дает положительного результата;
4) больные с тракционным повреждением плечевого сплетения, как с полным, так и с частичным нарушением проводимости, сочетанным с переломом ключицы, I ребра, лопатки, когда по рентгенологическим и клиническим признакам можно предполагать сдавление или повреждение отломками костей первичных или вторичных стволов плечевого сплетения; при этом показана ревизия стволов плечевого сплетения, при их анатомической целости проводят невролиз, при перерыве – реконструкцию; необходимо устранить сдавление отломками костей.
Сдавление нервных стволов – своеобразная форма повреждения. Она может наступить от сдавления нервов, сосудов, мышц гипсовой повязкой, жгутом, нарастающей гематомой, в результате отека тканей. Нерв может быть сдавлен отломками костей, костной мозолью, добавочным шейным ребром, в естественных костно-фасциальных каналах и др.
Сдавление гипсовой повязкой – одна из наиболее частых причин сдавления нервного ствола. При данном механизме сдавливаются нервы, мышцы и сосуды, что быстро приводит к некрозу мышц, грубым ишемическим изменениям в нервных стволах, причем повреждения мышц и нервов часто бывают очень тяжелыми и необратимыми. На верхней конечности страдают в основном мышцы и нервы передней поверхности предплечья. Если при наложенной циркулярной гипсовой повязке появляются признаки сдавления и нарушения проводимости нервных стволов, что клинически проявляется болевым синдромом, а затем нарушением чувствительности на пальцах кисти, то необходимо немедленно снять гипсовую повязку. Если при обследовании больного при этом определяется полное нарушение проводимости нервных стволов и в течение ближайших 2-3 ч после снятия повязки анестезия не исчезает, то показано срочное оперативное вмешательство с широким рассечением фасций для устранения отека и сдавления мышц и нервов в плотных фасциальных влагалищах. Эта операция в некоторых случаях может предотвратить некроз мышц и нервов. Если гипсовую повязку снимают поздно, то в последующем развивается контрактура Фолькманна. Рациональный способ лечения ишемической контрактуры заключается в иссечении некротизированных мышц, пересадке сухожилий и восстановлении нервов. При контрактуре Фолькманна в результате некроза мышц и дальнейшего их рубцового перерождения кисть и пальцы находятся в согнутом положении, кроме того, имеет место полное или частичное нарушение проводимости срединного и локтевого нервов. При этой форме поражения нервов оперативное вмешательство показано и в отдаленные сроки после повреждения.
Операция должна заключаться в полном иссечении некротизированных мышц. Затем производят реконструкцию сухожилий. Заканчивают операцию широкой ревизией пострадавших нервных стволов. Если произошел некроз нервного ствола, то необходимо произвести широкую мобилизацию его отрезков и после «освежения» концов нерва наложить шов. Если нерв изменен, но некроз его не наступил и при электродиагностике определяется, что проводимость обнаженного нерва, хотя и снижена, но сохранена, вмешательство на нерве заканчивается внешним невролизом.
Сдавление нерва жгутом – своеобразная форма повреждения. Наиболее часто поражается лучевой нерв. Следует помнить, что поражение лучевого нерва может наступить уже спустя полчаса после наложения жгута. При внутрикостной и внутривенной анестезии в травматологических стационарах вместо жгута для профилактики осложнений со стороны нервов предпочтительнее использовать пневматическую манжету. Следует отметить, что это не спасает больных от осложнений. Тактика лечения при поражении лучевого нерва в результате наложения жгута должна быть следующая.
При синдроме частичного нарушения проводимости лечение, как правило, только неоперативное. Оно во всех случаях заканчивается выздоровлением пациентов в ближайшие полгода. Оперативное вмешательство бывает показано лишь в редких случаях, когда имеет место синдром глубокого нарушения проводимости лучевого нерва после наложения жгута, приводящего к отсутствию электропроводимости лучевого нерва, полной реакции перерождения разгибателей кисти и пальцев, если в течение 3-4 мес. энергичное неоперативное лечение не дает положительного эффекта. В таких случаях показаны невролиз лучевого нерва и подведение электродов к нему для длительной электростимуляции в послеоперационном периоде.
Оперативное вмешательство показано пациентам со жгутовым повреждением лучевого нерва при наличии синдрома полного нарушения его проводимости:
-
атрофия и паралич мышц;
-
отсутствие электропроводимости нерва;
-
полная реакция перерождения мышц;
-
если энергичное неоперативное лечение в течение 4-6 мес. не даст положительного эффекта.
В практике нейрохирурга и невролога изредка встречаются пациенты, у которых жгут вынуждены были держать на конечности в течение нескольких часов. В этих случаях страдают все нервы конечности дистальнее жгута, и часто в последующем возникает контрактура типа фолькманновской в связи с длительной ишемией мышц. Так, при пребывании в течение нескольких часов жгута на плече страдают все нервы предплечья: лучевой, локтевой, срединный, а затем развивается сгибательная контрактура кисти и пальцев. План лечения таких больных должен быть таким же, как и при контрактуре Фолькманна, возникающей в результате сдавления конечности гипсовой повязкой.

Сдавление нервных стволов гематомой – редкая форма повреждения. Она возникает при колотом ранении артерии, когда продолжающееся кровотечение приводит к возникновению нарастающей гематомы, которая и сдавливает нервные стволы. Клинически это проявляется нарастанием признаков нарушения проводимости нервных стволов. Чаще эта форма повреждения встречается при повреждении подключичной, подмышечной и плечевой артерии. Таким больным показано срочное оперативное вмешательство: эвакуация гематомы и остановка кровотечения. Одновременно необходимо произвести ревизию нервов. Чаще операция заканчивается невролизом.
Сдавление нервов отломками костей
Повреждения нервов при переломах костей обусловлены тремя группами причин: первая относится к моменту перелома кости, и связана с прямым воздействием силы на кости и нерв; вторая — вторичные изменения тканей в области перелома; третья — проведение лечебных мероприятий по поводу перелома. Существуют 3 варианта сдавления нервов:
-
у больного с переломом кости сразу после перелома нет признаков повреждения нерва; затем при транспортировке или в процессе лечения при неэффективности иммобилизации костных отломков происходит их смещение, они сдавливают нерв, в результате чего происходит нарушение его проводимости; если отломок имеет острый край, то может произойти даже полный анатомический перерыв нерва; такому пациенту необходима срочная помощь травматолога и нейрохирурга в следующих случаях:
-
при наличии частичного неглубокого нарушения проводимости нерва можно произвести закрытую репозицию отломков кости без ревизии нерва; если же травматолог считает показанной открытую репозицию отломков, то нейрохирург может одновременно произвести осмотр нерва во время оперативного вмешательства; если он обнаружит при этом разрыв эпиневрия без разрыва пучков нерва, надрыв эпинев- ральной оболочки следует зашить; при обнаружении свежей субэпннев- ральной гематомы ее следует эвакуировать; при разрыве части пучков нервного ствола необходимо наложить частичный шов;
-
при наличии полного или глубокого нарушения проводимости нерва целесообразно произвести ревизию нерва с уточнением объема оперативного вмешательства па нем в зависимости от результатов осмотра, пальпации нерва и данных электродиагностики на обнаженном нерве;
-
у больного с переломом кости сразу после перелома нет признаков повреждения нервных стволов; признаки повреждения нерва появляются после закрытой репозиции отломков; важнейшим приемом для предотвращения повреждения нерва при закрытой репозиции отломков является тщательное выполнение классических рекомендаций; нерв, попавший между отломками, выскальзывает из-под них и не повреждается в момент репозиции, если отломки кости предварительно несколько растянуть в разные стороны вдоль их продольной оси; если повреждение нерва произошло, то тактика в отношении пациентов этой группы такая же, как и в отношении пациентов первой группы;
-
повреждение нерва отломками кости при открытой репозиции, как правило, свидетельствует о низкой квалификации хирурга и слабой ориентировке его в топографической анатомии; если повреждение нерва выявлено в процессе операции, то решение о тактике лечения принять обычно несложно после осмотра нерва, пальпации его и проведения электродиагностики на обнаженном нерве; обнаружение признаков нарушения проводимости нерва уже после оперативного вмешательства значительно усложняет положение врача и больного; надежным способом избежать повреждения нервов при оперативном вмешательстве является выделение нерва до вмешательства на костях и отведение его на резиновых держалках в сторону от отломков костей.
Сдавление нервов добавочными шейными ребрами описано анатомами давно. Наличие шейных ребер – довольно распространенное явление, однако сдавление сосудов и нервов они вызывают только у 10% пациентов, и чаще обнаруживается у женщин. Шейные ребра могут быть у V, VI, VII шейных позвонков. Практическое значение для хирургов имеют ребра VII шейного позвонка, так как они могут сдавливать стволы плечевого сплетения. При появлении признаков сдавления стволов плечевого сплетения добавочными шейными ребрами показано оперативное вмешательство. В типичных случаях оно должно заключаться в резекции шейного ребра и невролизе вовлеченных в патологический процесс стволов плечевого сплетения. Если имеются признаки нарушения кровообращения, то производят ангиолиз подключичной артерии. При выявлении во время операции сдавления нервов и сосудов передней лестничной мышцей необходимо произвести скаленотомию. Если нервы или сосуд сдавливаются фиброзными тяжами, то их также необходимо рассечь. Оперативное вмешательство целесообразно проводить в начальной стадии заболевания при появлении болевого синдрома и парестезии. Не следует проводить неоперативное лечение до появления атрофии мыши.

Сдавление нервов в результате отека тканей – весьма редкая форма повреждения нервного ствола. Причинами быстрого и выраженного отека тканей конечности, приводящего к сдавлению нервов, могут быть тупая травма, случайные инъекции различных веществ, например эфира, бензина, спирта и т. п., подкожно или внутримышечно и некоторые другие причины. В результате быстро возникающего и нарастающего отека тканей происходит сдавление мышц и нервных стволов в плотных малоподатливых фасциальных влагалищах. При этом механизм повреждения сходен с таковым при сдавлении конечности гипсовой повязкой. В результате выраженного отека тканей сдавливаются мелкие сосуды, нарушается кровообращение в мышцах и нервных стволах. Клинически это проявляется болевым синдромом, нарушением движений и чувствительности. При нарастающих расстройствах чувствительности пальцев показано срочное оперативное вмешательство – широкое рассечение плотных фасций и невролиз пострадавших нервных стволов для предотвращения некроза мышц и нервов и гибели их от ишемии. Если такую операцию не предпринимают, то исходом этого вида повреждения обычно является контрактура Фолькманна разной выраженности. Лечебные, мероприятия при ней описаны выше.
Сдавление нервов в естественных костно-фасциальных каналах можно расценивать как разновидность хронической травмы нерва. При этом нерв подвергается сдавлению, хронической травматизации и ишемии, что приводит к постепенному снижению его проводимости и нарушению функции. Протекают эти симптомокомплексы хронически с обострениями и ремиссиями под влиянием внешних и внутренних факторов. Этот вид повреждения обычно связывают с изменением обменных процессов в организме, что вызывает дегенеративные изменения связочно-фасциального аппарата. Провоцирующим фактором в ряде случаев может быть большая нагрузка па определенные группы мышц, связанная с особенностями трудовой деятельности. Наиболее часто встречаются синдром канала запястья с поражением срединного нерва и синдром передней лестничной мышцы с поражением стволов плечевого сплетения. Кроме того, стволы плечевого сплетения могут страдать под малой грудной мышцей с развитием гиперабдукционного синдрома. Локтевой нерв может поражаться в канале под связкой между гороховидной и крючковидной костями, а также в локтевой бороздке под треугольной связкой локтевого сустава. Лучевой нерв может быть сдавлен в спиральном канале на плечевой кости. Задний межкостный нерв, являющийся ветвью лучевого, может хронически ущемляться, под апоневротическим краем короткого лучевого разгибателя кисти.
Лечение туннельных синдромов в начальных стадиях заболевания обычно неоперативное. При отсутствии эффекта от него следует, как можно раньше прибегать к оперативному вмешательству, которое состоит в рассечении, а чаще в иссечении измененных связок и стенок сухожильно-фасциальных влагалищ и проведении внешнего невролиза.
Хроническая травма нерва – сравнительно редкая и очень своеобразная форма повреждения. Чаще всего она относится к локтевому нерву и возникает обычно спустя несколько лет после перелома костей, формирующих локтевой сустав. Кроме того, эта форма повреждения нерва формируется при хондроматозе локтевого сустава и очень редко после тяжелых ожогов области локтевого сустава.
Клинически она проявляется тем, что спустя несколько лет после перелома, появления хондроматоза или ожога области локтевого сустава у пациента выявляются признаки постепенно и очень медленно развивающегося нарушения проводимости локтевого нерва. Это проявляется медленно нарастающей атрофией мышц кисти, иннервируемых локтевым нервом, их парезом, а затем параличом. Параллельно нарушаются чувствительность и потоотделение в зоне иннервации локтевого нерва. Процесс развивается медленно, однако в течение нескольких лет приводит к полному параличу мышц кисти, иннервируемых локтевым нервом. Электродиагностика рано выявляет снижение электровозбудимости мышц, а затем частичную и полную реакцию перерождения. Появление первых симптомов нарушения проводимости нерва после старых переломов является показанием для оперативного вмешательства – невролиза и перемещения локтевого нерва в новое ложе. Чаще всего нерв перемещают в локтевую ямку с обязательным сохранением его ветвей к сгибателям кисти и пальцев. Оперативное вмешательство необходимо проводить с использованием микрохирургической техники на этапе мобилизации ветвей нерва.
Вывих нерва из своего ложа
Чаще встречается вывих локтевого нерва. Развитие заболевания обычно связывают с врожденной слабостью связочного аппарата и, в частности, треугольной связки локтевого сустава, которая удерживает локтевой нерв в бороздке. Провоцирующим фактором является травма локтевого сустава, а в последующем даже сгибание в локтевом суставе приводит к вывиху нерва. С течением времени развивается атрофия мышц предплечья и кисти, иннервируемых локтевым нервом, возникает преходящее, а затем постоянное чувство онемения в V пальце и в области гипотенара.
В травматологии предложены операции по укреплению стенок, удерживающих локтевой нерв в локтевой борозде, однако отдаленные результаты этих операций неблагоприятны. Это связано с тем, что с возрастом у больных развивается синдром сдавления локтевого нерва с усугублением неврологической симптоматики. Поэтому рекомендуется сразу по выявлении вывиха локтевого нерва производить оперативное вмешательство – перемещение нерва в локтевую ямку. Чем раньше производится эта операция, тем лучше отдаленные результаты. Применение микрохирургической техники способствует улучшению результатов этой операции, так как дает возможность тщательно выделить и полностью сохранить ветви нерва к мышцам сгибателей кисти и пальцев.
-
Показания к повторному шву нерва.
Необходимо помнить, что наложение повторных швов на нерв значительно ухудшает результаты лечения, поэтому следует принимать все меры для соблюдения условий, необходимых для качественного наложения первичного или отсроченного шва. Если нет условий для наложения первичного или раннего отсроченного шва, то лучше отложить оперативное вмешательство на некоторое время, так как операция, выполненная без соответствующего оснащения, редко заканчивается хорошим результатом. По данным В.Т. Горбуновой, после первичного шва нерва, наложенного в общехирургических и травматологических стационарах, хороший и отличный результаты были получены только у 8% больных, при наложении первичного шва на нерв в специализированном стационаре хороший и отличный результаты получен у 84,5% пациентов. Разумная отсрочка операции не дает такого резкого снижения результатов лечения. Анализ показывает, что отсроченный шов дает 72% хороших и отличных результатов и 20% – удовлетворительных. При повторном наложении шва получены только 42% хороших результатов и 36% удовлетворительных. Такое значительное ухудшение результатов вызвано, прежде всего, тем, что при повторной операции резко увеличивается диастаз между отрезками нерва и возрастает его натяжение, что и отягощает прогноз операции.
Основным показанием для повторного наложения шва является отсутствие клинических и электрофизиологических признаков регенерации нервного ствола после ранее произведенной операции. При этом необходимо, чтобы после операции прошло время, достаточное для появления первых признаков регенерации. При решении вопроса о выполнении повторных операций можно ориентироваться на следующие сроки:
1) верхний первичный ствол плечевого сплетения – 4-6 мес.;
2) средний и нижний первичные стволы плечевого сплетения – 6-9 мес.;
3) вторичные стволы плечевого сплетения – 9-12 мес.;
4) ранение и шов нервов па плече в верхней трети – 6-9 мес.;
5) ранение и шов нервов в верхней и средней третях предплечья – не менее 6 мес.;
6) ранение и шов нервов в нижней трети предплечья – 4-6 мес.;
7) ранение и шов нервов на кисти – не менее 3 мес.
Все названные сроки являются сугубо ориентировочными. Они в значительной степени могут меняться при большом дефекте нерва, при наличии сочетанного повреждения сосудов, костей, грубого повреждения большого массива мышц, большого количества сухожилий, недостаточно проводившегося в послеоперационном периоде неоперативного лечения и от многих других причин. В то же время повторный шов нерва может быть наложен и значительно раньше указанных сроков, если:
1) быстро формируется отчетливо пальпируемая неврома;
2) по медицинской документации, представленной больным, выявлены грубые ошибки, допущенные па предыдущем этапе лечения;
3) явно недостаточная регенерация нерва после ранее наложенного шва, по прошествии достаточного времени для данного конкретного нерва, уровня повреждения, величины дефекта, степени освежения отрезков нерва и т. д.
Если при полном отсутствии клинических и электрофизиологических признаков регенерации нерва принять решение о повторной операции обычно достаточно просто, то при наличии признаков недостаточно полноценно протекающей регенерации ранее сшитого нерва принять решение о производстве повторной операции обычно всегда нелегко. Такие повторные операции нецелесообразно предпринимать, если хирург не имеет достаточного опыта лечения повреждений нервных стволов, и нет необходимой аппаратуры для производства подробного электрофизиологического обследования.
Обычно окончательное решение о наложении повторного шва принимают уже в ходе самой операции после тщательного осмотра, пальпации уровня шва нерва и проведения электродиагностики на операционном столе, а при необходимости и исследования вызванных мышечных потенциалов с обнаженного нерва. Если при осмотре в ране ранее сшитого нерва выявляется плотная на ощупь внутриствольная неврома, нет электропроводимости нерва дистальнее невромы, то необходимо иссечь измененный участок нерва до картины нормального строения пучков на срезах центрального и периферического отрезков и наложить повторный шов. Если на операции не выявляется грубых анатомических изменений нерва на уровне ранее наложенного шва и имеются признаки электропроводимости нерва дистальнее уровня повреждения, то оперативное вмешательство чаще всего заканчивают тщательным внешним невролизом. При обнаружении грубых технических ошибок, допущенных при предыдущей операции, показания к повторному шву нерва обычно бесспорны.
Показания к операциям на нервах в зависимости от сроков с момента повреждения
-
Шов нерва.
Большинство авторов, изучавших результаты наложения швов на нерв, считают, что наибольшее число хороших и отличных результатов можно получить у пострадавших, оперированных в первые 3-6 мес. после травмы. Однако опыт показывает, что даже отсрочка в 9-12 мес. часто существенно не ухудшает результаты лечения. Наилучшие результаты дает первичный шов нерва, однако для его выполнения необходим целый ряд условий. Таким образом, при наличии показаний к наложению шва или к другой реконструктивной операции на нерве оперативное вмешательство надо стремиться выполнить как можно раньше после травмы. Однако если по каким-либо причинам реконструктивная операция на нерве была отложена, то противопоказаний для наложения шва на нерв нет в любые сроки, даже спустя много лет после травмы, так как даже небольшое улучшение движений, чувствительности и трофики очень важны.
-
Невролиз.
Срочные показания для невролиза могут возникнуть при сдавлении нерва нарастающей гематомой, при сдавлении нервных стволов выраженным и быстро нарастающим отеком конечности, при сдавлении нерва отломками кости, при сдавлении нервных стволов и других тканей конечности гипсовой повязкой. В остальных случаях невролиз производят в плановом порядке при возникновении показаний к этой операции. Во всех случаях это оперативное вмешательство также следует выполнять без особой отсрочки.
-
Тактика при больших дефектах нервных стволов.
При выявлении во время операции большого дефекта нерва необходимо учитывать ряд обстоятельств и придерживаться следующей тактики. Во-первых, возможности нерва для натяжения не безграничны, и потому необходимо ограничить себя при попытке сшить нерв при максимальном натяжении. Это связано с тем, что большое натяжение приводит к ишемизации нервного ствола и значительно ухудшает условия для регенерации. Наибольший дефект нерва, при котором может быть получен удовлетворительный результат, колеблется для различных нервов от 8 до 13 см. Во-вторых, необдуманное «освежение нерва» приводит к искусственному увеличению диастаза между отрезками, что, в свою очередь, отягощает прогноз повторной операции. Поэтому необходимо придерживаться следующей тактики: еще не обработанные концы нерва нужно взять на держалки и попытаться сопоставить отрезки на уровне предполагаемого «освежения», если возникают сомнения в состоятельности шва при данном натяжении, то используют ряд приемов для сближения концов поврежденного нерва.
К.А. Григорович предлагает следующие приемы:
1) придание конечности определенного положения, обычно с укорочением пути прохождения нерва путем сгибания конечности в суставах;
2) мобилизация центрального и периферического отрезков нерва на значительном протяжении;
3) соединение разноименных нервов;
4) этапное наложение швов на нерв, включающее в себя наложение предварительного провизорного шва без освежения концов нерва за неврому и периферический участок, второй этап операции проводится через 1-2 мес. после постепенного растяжения нерва путем осторожной разработки в суставах;
5) перемещение нерва в новое ложе по более короткому пути;
6) укорочение конечности путем резекции части кости.
Если отсутствует возможность устранить дефект с помощью указанных приемов, то необходимо ставить вопрос о возможности пластики нерва. В настоящее время общепризнанно, что в качестве трансплантата следует использовать только нервные стволы этого же больного. В качестве аутотрансплантатов можно использовать один из непоправимо поврежденных и лежащих рядом нервов или нервы, менее ценные в функциональном отношении, к таковым обычно относим кожные нервы конечностей. При этом следует помнить, что кожные нервы тоньше основного сшиваемого ствола, поэтому для трансплантата необходимо заготавливать более длинные участки, чтобы была возможность уложить их в 2-3 ряда в зависимости от толщины основного ствола.
Пластику нервных стволов следует применять только при наличии соответствующей увеличительной аппаратуры, микрохирургического инструментария и хирурга, владеющего микрохирургической техникой и хорошо знающего топографическую анатомию с учетом вариабельности строения нервных стволов.
Сочетание повреждения сухожилии и нервных стволов. Повреждение сухожилий на предплечье, кисти и пальцах, особенно при резаных ранах, расположенных поперечно, часто сочетается с повреждением нервов. Повреждения периферических нервов кисти проявляются нарушением движений и чувствительности. Различают осязательную, тактильную, тепловую, болевую и глубокую чувствительность.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания








Комментарии