Дыхательная система детей. Дыхательная недостаточность
Возрастные изменения дыхательной системы: структурное и функциональное развитие.
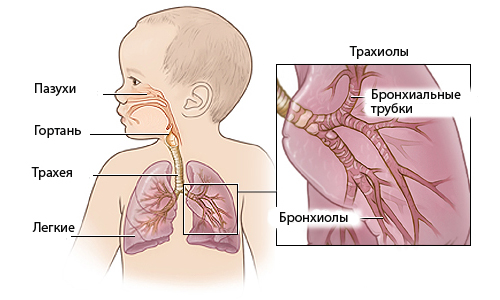
Дыхательные пути и альвеолы
Формирование легких происходит на 4-8 неделе беременности. В это время зачатки легких делятся на главные бронхи, на 6 неделе уже присутствуют все субсегментарные бронхи, и к 16 неделе строение бронхиального дерева аналогично таковому у взрослых. Когда развитие дыхательных путей завершено, конечные отделы бронхов реконструируются и делятся с формированием больших мешочков, или предшественников альвеол, которые могут поддерживать газообмен. Настоящие альвеолы образуются непосредственно до и после рождения; во время постнатального роста альвеолы тонкие и септированные.
У новорожденных детей имеется около 24 млн альвеол; к 8 годам их число увеличивается до 300 млн. После этого дальнейший рост легких, прежде всего, является результатом увеличения размеров альвеол.
Ткани легких новорожденных менее эластичны, чем у взрослых, эластин имеется только на альвеолярном канале. К 18-летнему возрасту эластин распространяется на альвеолы и его содержание становится максимальным. Затем он медленно уменьшается в течение следующих 50 лет. Растяжимость легких неразрывно связана с количеством эластина, поэтому пик растяжимости отмечается в пубертатном возрасте. Она снижена у маленьких детей и очень старых людей. Примерно до 5 лет происходят колебания дыхательных объемов.
Кровоснабжение легких
На 14 неделе гестации уже присутствуют главные артерии в легких. К 20 неделе картина ветвления аналогична таковой у взрослых, и также имеются дополнительные коллатеральные сосуды. Во время внутриутробной жизни дополнительные артерии развиваются одновременно с дыхательными путями и мешочками. Бронхиальные артерии появляются между 9-й и 12-й неделями беременности. Артериальная стенка развивается в виде тонкой эластичной пластинки на 12 неделе гестации, и мышечные клетки присутствуют уже на 14 неделе беременности. К 19 неделе эластичная ткань достигает седьмого порядка артериального ветвления, и мышечная ткань распространяется дистальнее. У плода мышечный слой артерий заканчивается на более проксимальном уровне, чем у детей и у взрослых. Мышечный слой артерий более толстый, чем у артерий аналогичного размера у взрослых. Легочные артерии сильно сужены до второй половины беременности. У плода ягненка легочный кровоток составляет всего 3,5% от общего объема желудочков во втором триместре и составляет всего 7% перед рождением. Сразу после рождения легочный кровоток увеличивается почти до уровней взрослого человека. Развитие легочной венозной системы является зеркальным отражением развития артериальной.
Легочные артерии продолжают развиваться после рождения, образование артерий сопутствует ветвлению дыхательных путей вплоть до 19-месячного возраста, а коллатеральные артерии продолжают развиваться до 8 лет. При увеличении альвеолярного размера картина ветвления ацинусов становится более обширной и сложной. Артериальная структура также претерпевает изменения, такие как увеличение размеров имеющихся артерий, толщина мышечного слоя артерий снижается до уровней взрослого человека в течение первого года жизни.
Биохимическое развитие
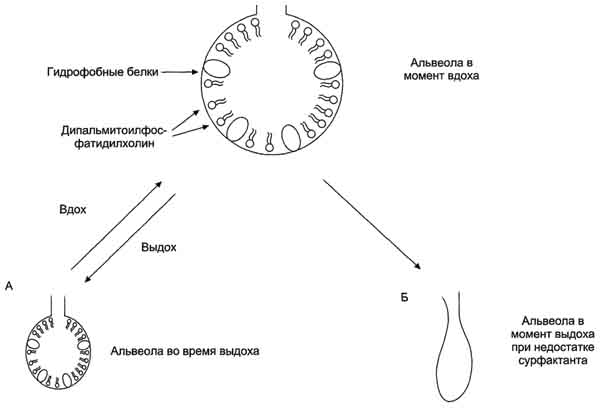
На 24 неделе беременности кубический альвеолярный эпителий увеличивается в объеме и пневмоциты I типа становятся выстилающими и опорными клетками альвеол. В это время также развиваются большие клетки II типа, производящие и накапливающие сурфактант. У человека сурфактант появляется на 23-24 неделе гестации, и его концентрация увеличивается в течение последних 10 недель внутриутробной жизни. Сурфактант высвобождается в альвеолы приблизительно на 36 неделе гестации, что делает возможной нормальную внеутробную жизнь.
Переход дыхания: от плацентарного к легочному
Примерно на 24 неделе гестации легкие способны на газообмен вне матки. Тем не менее, сразу после рождения должен произойти ряд важных циркуляторных и механических изменений для обеспечения адекватного газообмена в легких.
Вентиляция начинает соответствовать перфузии в первые часы жизни. Вначале появляется внутрилегочное шунтирование справа налево через ателектатические участки легкого, а также шунтирование слева направо через артериальный проток и, незначительно, справа налево через овальное окно. РаО2 в пределах 50-70 мм рт. ст., что в три раза больше нормы взрослых, указывает на шунт справа налево.
Переход от фетального к неонатальному дыханию и циркуляции является динамичным. Постнатально легочное сосудистое русло остается суженным при воздействии ацидоза, холода или гипоксии. При сужении легочной артерии увеличивается шунтирование не насыщенной кислородом крови справа налево через открытое овальное окно и артериальный проток, и, следовательно, снижается легочный кровоток. Наличие такой активной легочной вазоконстрикции называется персистирующей легочной гипертензией новорожденных или персистирующим фетальным кровообращением. Она также встречается у пациентов с врожденной диафрагмальной грыжей, аспирацией мекония и сепсисом.
Биомеханика дыхания детей
Для вентиляции легких дыхательные мышцы должны преодолеть статико-эластические и динамические силы сопротивления. Изменения в этих противостоящих силах во время постнатального развития влияют на объем легких, характер и работу дыхания.
Растяжимость легких в зависимости от возраста
Растяжимость легких с возрастом меняется из-за изменений альвеолярной структуры, количества эластина и сурфактанта. При рождении растяжимость является низкой, поскольку предшественники альвеол имеют толстые стенки и сниженное количество эластина. Дефицит сурфактанта (например, при болезни гиалиновых мембран) еще больше снижает растяжимость легких. В результате дальнейшего развития альвеол и эластина растяжимость легких улучшается в течение первых лет жизни.
Грудная стенка
У младенцев очень податливая грудная стенка, потому что их ребра представлены хрящевой тканью. Из-за коробчатой конфигурации грудной клетки младенцев ее эластическая тяга меньше, чем эластическая тяга уплощенной в дорсовентральном направлении грудной клетки взрослых. Взрослые имеют значительную долю медленно сокращающихся, устойчивых к утомлению волокон, характеризующихся высоким уровнем аэробного метаболизма, как в диафрагме, так и межреберных мышцах. В то время как у взрослых имеются 65% этих волокон в межреберных мышцах и 60% в диафрагме, новорожденные имеют только от 19% до 46% этих волокон в межреберных мышцах и от 10% до 25% - в диафрагме. Следовательно, дети более склонны к переутомлению мышц и снижению устойчивости грудной стенки. Результатом растяжимости грудной стенки и плохо растяжимых легких является альвеолярный коллапс и снижение дыхательного объема в покое (функциональная остаточная емкость). Несмотря на эту склонность к коллапсу легкого, ребенок сохраняет большую динамическую функциональную остаточную емкость с помощью быстрого темпа дыхания, размыкания гортани и стабилизации грудной стенки с увеличением тонуса межреберных мышц во время выдоха.
Верхние дыхательные пути
Существуют несколько анатомических различий между верхними дыхательными путями у детей и взрослых, которые влияют на способность поддерживать их проходимость. Более переднее и краниальное расположение гортани у детей делает «положение принюхивания» идеально подходящим для масочной вентиляции и интубации трахеи. Чрезмерное разгибание шеи в действительности может привести к обструкции дыхательных путей. Узкая часть дыхательных путей взрослого человека – это область голосовых связок. В возрасте до 5 лет самой узкой частью дыхательных путей ребенка является область перстневидного хряща, так как сзади гортань расположена более краниально, чем спереди, что приводит к тому, что перстневидный хрящ имеет форму эллипса, а не круга. К 5-летнему возрасту задняя часть гортани спускается на уровень взрослого. Эндотрахеальная трубка, которая легко проходит через голосовые связки маленького ребенка, может стать причиной ишемического повреждения дистального отдела гортани. Перстневидное сужение и очень податливый хрящ трахеи обеспечивают адекватную герметизацию вокруг эндотрахеальной трубки без манжетки. Детям в возрасте до 5 лет обычно не требуется эндотрахеальная трубка с манжеткой, однако некоторые практикующие врачи регулярно используют такие трубки у этой возрастной группы пациентов.
Экспираторное закрытие дыхательных путей
Эластические свойства легких тесно коррелируют с экспираторным закрытием дыхательных путей. Экспираторное закрытие дыхательных путей (или объем закрытия легких) – это объем легких, при котором терминальные отделы дыхательных путей закрываются и газ попадает в «ловушку» (за закрытыми дыхательными путями). Большой объем закрытия легких увеличивает вентиляцию мертвого пространства, что приводит к ателектазам и шунтированию крови справа налево. Эластичные ткани помогают поддерживать дыхательные пути открытыми, так что чем больше эластичной стромы в мелких дыхательных путях, тем меньший объем легких приходится на закрытие мелких бесхрящевых дыхательных путей. Объем закрытия легких мал в позднем подростковом возрасте и относительно велик у пожилых и детей. Дети преодолевают осложнения, обусловленные большим объемом закрытия легких и вторичных ателектазов, с помощью учащения дыхания, постоянной активности и плача. Экспираторное закрытие дыхательных путей становится серьезной проблемой у неактивных, седатированных и анестезированных младенцев.
Силы сопротивления
У новорожденных дыхательные пути мелкие с большим сопротивлением или низкой проводимостью. Диаметр мелких дыхательных путей существенно не увеличивается примерно до 5 лет, а значит, маленькие дети имеют повышенное сопротивление дыхательных путей в состоянии покоя и особенно уязвимы для болезней, которые вызывают дальнейшее сужение дыхательных путей (спазм гладкой мускулатуры, отек/воспаление дыхательных путей). Нормальное высокое сопротивление дыхательных путей у новорожденных и детей раннего возраста помогает поддерживать функциональную остаточную емкость.
Регуляция дыхания
У новорожденных – уникальная регуляция дыхания. На начальном этапе гипоксия увеличивает вентиляцию на короткое время. За этим увеличением следует устойчивое снижение вентиляции. У недоношенных детей ответ более выраженный. У доношенных новорожденных он исчезает через несколько недель. Периодическое дыхание также часто встречается у младенцев, особенно у недоношенных, что, вероятно, обусловлено недостаточным развитием мозговых дыхательных центров.
Транспорт кислорода: присоединение и отдача кислорода
Фетальный гемоглобин содержит более низкие уровни 2,3- ДФГ, и давление полунасыщения гемоглобина кислородом составляет от 18 мм рт. ст., что значительно ниже, чем у взрослых (27 мм рт. ст.). Такое низкое давление полунасыщения у плода позволяет хорошо оксигенировать гемоглобин при низком плацентарном напряжении кислорода, но усложняет высвобождение кислорода в тканях. От 3 до 6 месяцев после рождения фетальный гемоглобин заменяется гемоглобином взрослого типа. Повышенная концентрация фетального гемоглобина и увеличенное содержание кислорода в нем для плода являются выгодными, потому что это позволяет 20 мл кислорода, содержащимся в 100 мл крови, быть доставленными к мозгу и к сердцу. Такое содержание кислорода аналогично таковому у взрослых, дышащих комнатным воздухом. Потребность в кислороде у новорожденных при рождении составляет от 6 до 8 мл/кг/мин. Она снижается до 5-6 мл/кг/мин на первом году жизни. Сниженное вентиляционно-перфузионное соотношение, сниженное давление кислорода в фетальном гемоглобине и признаки прогрессирующей анемии новорожденных могут вызывать трудности в доставке достаточного количества кислорода в первые месяцы жизни. Младенцы компенсируют это сердечным выбросом, равным приблизительно 250 мл/ кг/мин в течение первых 4-5 месяцев жизни.
Дыхательная недостаточность ребенка
Дыхательная недостаточность проявляется неспособностью легких адекватно оксигенировать кровь и удалять углекислый газ из артериальной крови легких. Существует много причин дыхательной недостаточности, в том числе низкая концентрация кислорода в окружающей среде, паренхиматозные и сосудистые заболевания легких.
Подробный анамнез тяжести и частоты дыхательных расстройств помогает провести дифференциальную диагностику и выбрать правильный подход к лечению. Должны быть конкретные данные, включающие:
-
историю недоношенности;
-
использование дыхательной аппаратуры;
-
проведение искусственной вентиляции легких;
-
внелегочную органную патологию;
-
семейный анамнез заболеваний дыхательных путей.
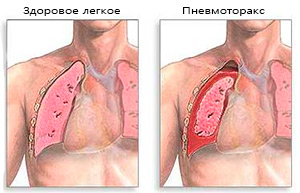
Подробная информация о кормлении и уточненная диаграмма роста могут дать ценную информацию, потому что задержка роста может увеличить потребность в кислороде. Как правило, 1-2% от общего объема потребляемого кислорода используются для дыхания. При дыхательной патологии для дыхания может быть использовано до 50% от общего потребления кислорода. У младенцев и детей с дыхательной недостаточностью часто возникают межреберные и супрастернальные втяжения (признаки увеличения дыхательной работы и потребления кислорода). Большинство младенцев и детей имеют тахипноэ, которое также помогает поддерживать функциональную остаточную емкость легких при помощи сокращения времени выдоха. При частом и неглубоком дыхании требуется меньше энергии, чем при глубоких вдохах. У младенцев с дыхательной недостаточностью часто имеется цианоз губ, кожи и слизистых оболочек. Тем не менее, зачастую бывает трудно распознать изменения цвета кожи, если РО2 не ниже 70 мм рт. ст. Следует отмечать симметричность грудной клетки в акте дыхания. Неравномерное участие грудной клетки в дыхании может указывать на пневмоторакс или обструкцию бронха. Небольшой грудной объем способствует легкой передаче звуков дыхания с одной стороны на другую. Дыхательные шумы могут оставаться нормальными, даже при пневмотораксе. У младенцев и маленьких детей вздутие живота может значительно затруднять дыхание.
Радиологическое исследование носоглотки, шеи и грудной клетки может предоставить значимую информацию относительно причин и тяжести дыхательной дисфункции. Для оценки дыхательных путей и движения диафрагмы у неконтактного ребенка может быть использована рентгеноскопия. Однако для таких обследований ребенка должен сопровождать кто-то, кто способен обеспечить ИВЛ, если он может покинуть отделение интенсивной терапии.
Исследование функции легких помогает оценить дыхательную функцию, но из-за невозможности взаимодействия эти тесты сложно проводить у детей младше 5 лет без седации, которая может быть опасна для неинтубированного ребенка с дыхательной недостаточностью. Большинство исследований легочной функции требуют использования облегающей маски, а это само по себе может быть проблематично. При интубированной трахее можно легко измерить легочные объемы, скорость выдоха, податливость и силу вдоха; в самом деле, большинство механических аппаратов ИВЛ теперь оснащены мониторами, которые позволяют регулярно измерять эти показатели.
Для определения эффективности газообмена используется анализ газов артериальной крови. Измерения РаО2 позволяют определить альвеолярно-артериальный градиент кислорода и шунтирование крови через легкие справа налево.
Еще одним показателем функции легких является элиминация CО2 из артериальной крови. Нарушение удаления CО2 из легочной артериальной крови указывает на неравномерное распределение кровотока в легких и, в частности, говорит об увеличенном мертвом пространстве.
У новорожденных распространена катетеризация пупочной артерии, соответственно, те, кто работают с такими детьми, могут получать артериальную кровь и непрерывно измерять артериальное кровяное давление. Такие катетеры относительно просты в установке и в обслуживании. Кончик катетера в идеале должен быть установлен на уровне или немного выше уровня бифуркации аорты и ниже уровня почечных артерий. При стабилизации состояния ребенка нужно устанавливать периферический катетер и извлекать катетер из пупочной артерии. Все внутриартериальные катетеры потенциально способны приводить к тромбоэмболическим заболеваниям. Необходимо соблюдать осторожность при использовании артериальных катетеров, чтобы предотвратить эмболию сосудов мозга или сердца. При правильной установке и техническом обслуживании серьезные артериальные осложнения редки. Несмотря на то, что артерии, которые катетеризированы в течение длительного периода, могут закупориваться, они имеют способность к реканализации в течение короткого промежутка времени.
Разработаны малоинвазивные методы мониторинга газообмена. Чрескожные электроды точно измеряют уровень кислорода и углекислого газа у младенцев и маленьких детей, но теряют точность при гипоперфузии. Электроды требуют некоторого времени для разогревания, что делает трудным проведение выборочных проверок. Такие мониторы лучше всего использовать у детей старшего возраста и у взрослых. Для ухода за тяжелобольными младенцами и детьми обычно используются пульсоксиметры, потому что они являются точными, не требуют времени для разогрева и требуют небольших умений для их применения. Датчик легко обхватывает всю руку или стопу маленького ребенка. Мониторинг содержания СО2 в конце выдоха позволяет непрерывно измерять элиминацию углекислого газа. Однако эта технология имеет ограниченное применение у маленьких детей, из-за наличия у них увеличенного мертвого пространства и большого веса устройства на конце эндотрахеальной трубки для взятия проб, которое может перегибать эндотрахеальную трубку и привести к случайной экстубации.
Причины дыхательной недостаточности
Причины дыхательной недостаточности в некоторой степени зависят от возраста пациента. Дыхательная недостаточность у новорожденных часто является результатом врожденных аномалий, незрелости легких и легочных кровеносных сосудов.
Врожденные аномалии могут включать в себя:
-
пороки развития дыхательных путей;
-
дисгенез;
-
нарушение функции легких или других органов;
-
аномалии легочных сосудов.
Проявления незрелости могут включать в себя:
-
апноэ недоношенных;
-
болезнь гиалиновых мембран;
-
аномальный синтез;
-
секрецию сурфактанта.
В перинатальном периоде новорожденные подвержены инфекциям и стрессу. Персистирующая легочная гипертензия может осложнить неонатальную легочную и внелегочную патологию. Вне зависимости от причины дыхательная недостаточность может быть классифицирована как гиповентиляционный синдром у пациентов с нормальными легкими, с внутренней альвеолярной и межинтестинальной патологией и с обструктивными заболеваниями дыхательных путей.
Гиповентиляционные синдромы у детей с нормальными легкими
Причинами гиповентиляции являются нервно-мышечные заболевания, центральная гиповентиляция и структурные/анатомические нарушения расправления легких (обструкция верхних дыхательных путей, массивное вздутие живота). Эти состояния характеризуются недостаточным расправлением легких, наличием вторичных ателектазов, внутрилегочным шунтированием справа налево и системной гипоксией. Ателектаз и вторичное сокращение ФОЕ увеличивает работу дыхательных мышц. Это заключается в увеличении ЧДД со сниженным ДО. Характер дыхания в конечном счете увеличивает количество ателектазов и шунтирование. В результате дети с нормальными, по сути, легкими и гиповентиляционным синдромом имеют тахипноэ, сниженный дыхательный объем, повышение работы дыхательных мышц и цианоз. Рентгенограммы грудной клетки выявляют небольшие объемы легких и милиарный или долевой ателектаз. Патологические процессы быстро ликвидируются с помощью вентиляции с положительным давлением и с положительным давлением в конце выдоха (ПДКВ).
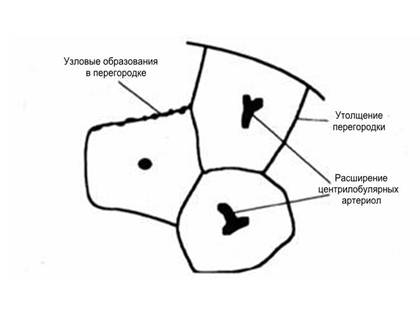
Первично-легочная альвеолярная или интерстициальная патология
Внутренние болезни легких с вовлечением альвеол или легочного интерстиция снижают эластичность легких и уменьшают просвет дыхательных путей, что приводит к ателектазам и увеличению работы дыхания. Эластичность легких снижается вследствие отека или воспаления альвеол, или фиброза интерстиция. Чем «жестче» легкие, тем большее отрицательное внутриплевральное давление требуется для прохождения воздуха, тем самым увеличиваются работа дыхания и риск возникновения пневмоторакса.
Обструктивная болезнь дыхательных путей
Обструкция дыхательных путей может быть наружной или внутренней. Внутренняя обструкция мелких дыхательных путей обычно происходит при бронхиолите, бронхопневмонии, бронхиальной астме и бронхолегочной дисплазии (БЛД). Обструкция дыхательных путей уменьшает проходимость дыхательных путей, увеличивает их сопротивление и работу дыхания. Частичная обструкция препятствует больше выдоху, чем вдоху, и приводит к образованию «ловушки» для газа или очаговой эмфиземе. Полная обструкция дыхательных путей приводит к возникновению ателектазов и шунтированию крови справа налево в легких. У пациентов с заболеваниями мелких дыхательных путей обычно имеется сочетание полной и частичной обструкции, неоднородного коллапса и перераздувания легкого. Коллабированные области вызывают внутрилегочное шунтирование крови справа налево, а перераздуваемые – увеличивают количество мертвого пространства. Если легкое перераздувается, уменьшается его растяжимость и увеличивается работа дыхания. Клиническая и рентгенологическая картина варьируют в связи с различной степенью коллапса и перерастяжения легкого.
Таким образом, все причины дыхательной недостаточности имеют сходную патофизиологию: ателектазы и снижение функциональной остаточной емкости, с внутрилегочным шунтированием крови справа налево, или перерастяжение альвеол, с повышением мертвого пространства и снижением элиминации СО2 (или и тем, и другим). Повышенная работа дыхания, связанная со всеми формами дыхательной патологии, может привести к усталости и такой картине дыхания, которая еще более усложнит начальный процесс. Если повышенная работа дыхания своевременно не обнаружена и не проводится лечение, то это может привести к апноэ, гипоксии и остановке сердца у маленьких детей.
Лечение дыхательной недостаточности
Лечение дыхательной недостаточности включает в себя:
-
обеспечение проходимости дыхательных путей;
-
увеличение концентрации кислорода на вдохе;
-
устранение обструкции дыхательных путей;
-
лечение инфекций;
-
коррекцию перегрузки жидкостью;
-
исправление всех внелегочных аномалий;
-
назначение искусственной вентиляции легких.
В некоторых случаях может оказаться эффективным использование экзогенного сурфактанта, высокочастотной вентиляции легких, тактики механической вентиляции с защитой легких, ингаляций NO, наклонного положения, увлажненной вентиляции и экстракорпоральной мембранной оксигенации (ЭКМО).

Младенцы и маленькие дети часто нуждаются в помощи в поддержании проходимости дыхательных путей. Для предотвращения возникновения аспирации или желудочно-пищеводного рефлюкса и сведения к минимуму последствий вздутия живота необходимо проведение специфических манипуляций, таких как создание полувертикального положения. Как правило, уместно держать голову по средней линии и минимизировать чрезмерное ее сгибание.
Вдыхаемая концентрация кислорода может быть увеличена с помощью облегающей маски. Часто помогают носовые канюли, но они могут вызывать возбуждение у некоторых детей и сводить на нет все полезное действие высоких значений FiO. Направленный поток кислорода, лицевые маски, кислородные палатки менее агрессивны и, в целом, лучше переносятся детьми.
Обструкция верхних дыхательных путей может быть устранена при помощи постановки ларингеальной маски, эндотрахеальной трубки, ротоглоточного или носоглоточного воздуховода или трахеостомии. Часто ингаляционный рацемический адреналин и внутривенные стероиды уменьшают отек подсвязочного пространства, антибиотики снижают инфекционный отек, агонисты бета-рецепторов и ингаляционные антихолинергические препараты расслабляют гладкую мускулатуру бронхов. Больные с пневмонией должны сдать анализы на бактериальные, вирусные или грибковые патогены и лечиться соответствующими антибиотиками. Отек легких лечится путем ограничения потребления жидкости и назначения диуретиков и кардиотонических или вазоактивных препаратов. Хорошее энтеральное или парентеральное питание, жидкостный и электролитный баланс и адекватное функционирование сердечно-сосудистой системы и почек являются частью респираторной поддержки. Искусственная вентиляция легких является основным методом лечения дыхательной недостаточности. Вот несколько внелегочных показаний к искусственной вентиляции легких:
-
Реанимация при сосудистой недостаточности.
В ситуациях, когда сердечно-сосудистая система нестабильна, самым безопасным методом является механическая вентиляция легких. При остановке сердца респираторная поддержка является обязательной, хотя вначале может быть эффективным проведение масочной вентиляции с помощью мешка AMBU. Пациенты редко умирают от отсутствия эндотрахеальной трубки. Смерть пациента обычно происходит вследствие недостатка кислорода, который иногда, в спешке, забывают подсоединить к эндотрахеальной трубке. Искусственная вентиляция легких используется после кардиохирургических вмешательств (для обеспечения адекватного газообмена) до стабилизации кровообращения. Искусственная вентиляция легких также снижает риск развития нежелательной сердечно-сосудистой декомпенсации.
-
Респираторная поддержка.
Иногда для увеличения сосудистого русла у некоторых новорожденных используется проведение преднамеренной гипероксии с целью расширения легких для инициализации других методов лечения. Искусственная вентиляция легких используется также для снижения внутричерепного давления (ВЧД), что происходит благодаря возникновению небольшого дыхательного алкалоза и снижения церебрального объема крови. После этого среднее артериальное давление должно поддерживаться на уровне, предшествовавшем гипервентиляции, или выше, чтобы предотвратить развитие дальнейшей церебральной ишемии. Механическая вентиляция также может потребоваться детям с патологическими состояниями, которые предрасполагают к дыхательной недостаточности (патологическое ожирение, сепсис, истощение и кифосколиоз).
-
Сниженная работа дыхания.
Снижение кислородной емкости при дыхании у искусственно вентилируемых пациентов может улучшить способность некоторых из них переживать основные физиологические ответы. Для сохранения энергии, затрачиваемой на дыхание, и использования этой энергии для роста детям с БЛД может потребоваться долгосрочная ИВЛ.
Вентиляционная терапия
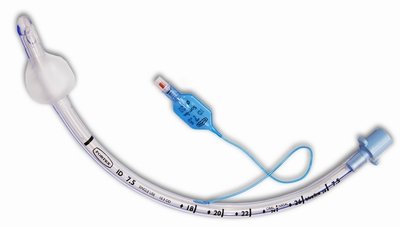
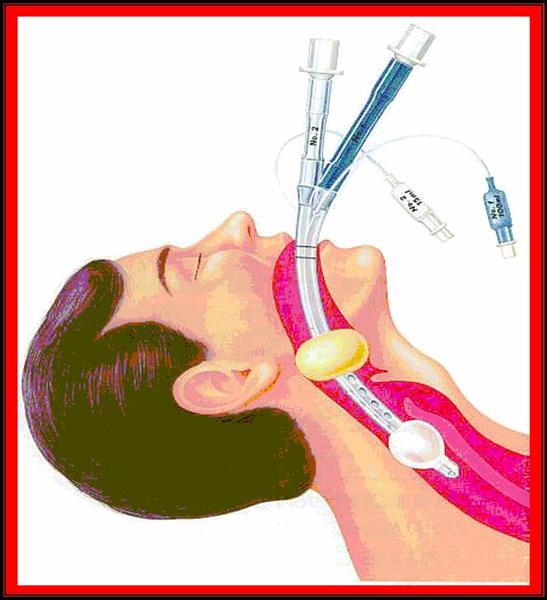
Респираторная поддержка обеспечивается благодаря постоянному положительному давлению в дыхательных путях, вентиляции с прерывистым положительным давлением и вентиляции с отрицательным давлением. Вентиляция с положительным давлением, как правило, применяется через эндотрахеальную трубку или трахеостомию. Вентиляция у некоторых младенцев и детей может быть поддержана с помощью постоянного положительного давления в дыхательных путях через маску, неинвазивной вентиляцией или с помощью носовых канюль с высоким потоком. Рототрахеальные интубации выполнимы легче назотрахеальных, особенно в чрезвычайных ситуациях. Следует тщательно подбирать необходимый размер эндотрахеальной трубки. Существует формула, с помощью которой можно рассчитать необходимый размер трубки детям старше 2 лет: (возраст+16).
Эта формула определяет внутренний диаметр эндотрахеальной трубки подходящего размера. При использовании правильного размера должна происходить небольшая утечка воздуха при применении положительного давления (от 20 до 30 см вод. ст.). При использовании несоразмерно большой эндотрахеальной трубки (ЭТТ), особенно у детей с воспалительными заболеваниями верхних дыхательных путей, такими как ларинготрахеобронхит, могут возникнуть серьезные повреждения гортани и подсвязочной области. Из-за более гибкого хряща трахеи и относительно узкого подсвязочного пространства у детей младше 5 лет ЭТТ без манжетки, как правило, обеспечивает адекватную герметичность. Тем не менее, если у пациента имеется заболевание легких, которое требует высокого давления при вентиляции, целесообразней использовать трубки с манжетками. В отделении интенсивной терапии маленьких детей часто используется ЭТТ небольшого диаметра с манжетой, но в таких случаях следует позаботиться об обеспечении небольшой утечки воздуха от 25 до 30 см вод. ст. Как правило, трубка с манжеткой устраняет утечку воздуха вокруг ЭТТ, а перераздувание манжеты может остановить венозный кровоток и травмировать дыхательные пути. В настоящее время нет данных о долгосрочной безопасности использования у маленьких детей ЭТТ с манжетками.
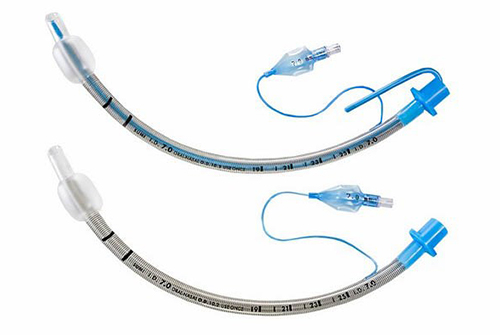
При интубации трахеи важно правильно расположить эндотрахеальную трубку. Если она установлена правильно, то движения грудной клетки симметричны и дыхательные шумы одинаково проводятся с обеих сторон, при выслушивании в подмышечных впадинах. Электронная или колориметрическая система обнаружения CO2 помогает подтвердить то, что ЭТТ находится действительно в трахее, а не в пищеводе. Если двойные линии на ЭТТ находятся на уровне голосовых связок, то это, как правило, указывает на правильное положение ЭТТ. Еще одним способом правильно расположить трубку является продвижение ее в правый главный бронх с последующим выслушиванием дыхательных шумов в левой подмышечной впадине (дыхательные шумы будут уменьшаться). Необходимо медленно выводить ЭТТ. Когда при дыхании слышны звуки слева, нужно дополнительно подтянуть трубку на 1-2 см, в зависимости от размера ребенка. Если дыхательные шумы одинаковые, следует зафиксировать трубку на месте. На рентгенограмме грудной клетки кончик ЭТТ должен располагаться на половине расстояния между голосовыми связками и килем. У маленьких детей расстояние между килем и голосовыми связками очень короткое. Следовательно, можно случайно разместить ЭТТ в главном бронхе. ЭТТ перемещается в дыхательных путях при сгибании головы. Разгибание перемещает ее к голосовым связкам. Поворот головы в сторону может вызвать обструкцию кончика ЭТТ, если он вступает в контакт со стенкой трахеи, что может привести к гиперкапнии и/или гипоксемии.
Обычно эндотрахеальная трубка используется более чем 2 недели до проведения трахеостомии. Это возможно при использовании надлежащего увлажнителя вдыхаемых газов, при проведении улучшенной эндотрахеальной санации, мониторинга (SaO2) и при обеспечении отличного ухода.
Каждый ухаживающий за ребенком должен быть постоянно готов к тому, что ЭЭТ может обтурироваться выделениями, случайно произойдет экстубация или интубация главного бронха. У новорожденных обычно чаще обтурируются выделениями эндотрахеальные трубки с глазком Мерфи, чем без него. Глазок Мерфи расположен очень близко к концу ЭТТ. Как только ЭТТ входит в главный бронх, эффективное дыхание младенца через «глазок» становится невозможным. Поскольку ЭТТ почти такого же размера, что и трахея, для младенца практически невозможно дыхание вокруг трубки. Таким образом, ЭТТ с глазком Мерфи опасны и, вероятно, не должны использоваться у детей раннего возраста. Когда детям на большой промежуток времени требуется создание искусственных дыхательных путей с целью механической вентиляции легких, эндотрахеальной санации или для обхода места обструкции верхних дыхательных путей, проводится трахеостомия. Случайное смещение трахеостомической трубки и ее выход из дыхательных путей могут быть опасны для жизни. Извлечение трахеостомической трубки в течение первых 72 ч после введения может быть очень затруднительным и создать ложные ходы, которые способны сделать невозможной вентиляцию легких или вызвать пневмоторакс.
Постоянное положительное давление в дыхательных путях и положительное давление в конце выдоха (ПДКВ)
При создании постоянного положительного давления (СДППД или CPAP) в дыхательных путях ребенок дышит самостоятельно через систему, которая поддерживает постоянное ПДКВ. При ПДКВ (или PEEP) легкие механически вентилируются при сохранении постоянного давления в конце выдоха.
Постоянное положительное давление в дыхательных путях применяется с эндотрахеальной трубкой, носовыми канюлями или маской. Поскольку большинство новорожденных дышат через нос, часто является эффективным применение постоянного положительного давления в дыхательных путях через нос, даже у недоношенных. Успешность его применения зависит от размера, состояния ребенка и от наличия у последнего дыхания через рот. Плач и дыхание через рот могут уменьшить эффективность использования носового постоянного положительного давления в дыхательных путях, потому что эти действия уменьшают давление в глотке. При использовании постоянного положительного давления в дыхательных путях через носовые канюли или маску возможно вздутие живота. В таком случае требуется постановка желудочного зонда для декомпрессии. В течение коротких периодов эффективно использование лицевой маски у детей и взрослых. Длительное использование маски для постоянного положительного давления в дыхательных путях может привести к некрозу лица и/или глаз вследствие их сдавления. Уровень ПДКВ от низкого до умеренного может сохраняться у детей с ЭТТ без манжеты, но большая утечка газа вокруг трубки приводит к неустойчивости уровня ПДКВ. Эту проблему решает применение трубки большего диаметра или ЭТТ с манжетой.
Трудно определить оптимальный уровень постоянного положительного давления в дыхательных путях или ПДКВ, но, как правило, им является самый низкий уровень давления, который поддерживает нормальное РаО2 без чрезмерного повышения PaCO. Слишком малое давление неэффективно повышает РаО2, в то время как слишком высокое давление перераздувает легкие и увеличивает вентиляцию мертвого пространства. Для всех детей с искусственными дыхательными путями рекомендуется применять низкий уровень постоянного положительного давления в дыхательных путях или ПДКВ (от 2 до 5 см вод. ст.).
Целью является использование самого низкого уровня постоянного положительного давления в дыхательных путях или ПДКВ, который адекватно улучшает оксигенацию при минимальном воздействии на вентиляцию.
-
Первый подход заключается в использовании такого уровня постоянного положительного давления в дыхательных путях или ПДКВ, который улучшает оксигенацию и позволяет быть уменьшенным уровню FiO2 (до 0,6 или менее).
-
Второй подход заключается в увеличении давления в конце выдоха до максимального улучшения ситуации.
Suter и колл. предположили, что лучшим для ПДКВ (или для постоянного положительного давления в дыхательных путях) является такой уровень конечного экспираторного давления, который необходим для максимального транспорта кислорода, являющегося результатом сердечного выброса и артериального содержания кислорода. Для этого требуются повторные измерения сердечного выброса и использование термодилюционного катетера Свана-Ганца, который редко применяется у маленьких детей. Большинство клиницистов приближаются к лучшим уровням постоянного положительного давления в дыхательных путях или ПДКВ с помощью уровней, которые дают адекватные РаО2 и РаСО2, и позволяют снижать FiO.

-
Вентиляция с положительным давлением.
Механические респираторы с положительным давлением классифицируются в соответствии с методом их регуляции, как:
-
с заданным объемом;
-
с заданным давлением;
-
с заданным временем.
Как правило, предварительная установка аппаратов по времени или давлению более удобна для использования у младенцев и маленьких детей (<10 кг), тогда как респиратор с заданным объемом обычно используются у детей старшего возраста (> 10 кг) и взрослых. Установка респираторов с заданным временем и давлением имеет ряд преимуществ у младенцев и маленьких детей. Большинство из этих пациентов интубированы ЭТТ без манжетки, что приводит к утечке газов в разной степени вокруг трубки. Эта утечка, наряду с относительно большим сжатием объема дыхательного контура по сравнению с дыхательным объемом младенцев, делает заданную по объему вентиляцию ненадежной. Основная проблема аппаратов с заданным давлением или временем состоит в том, что поставляемый объем зависит от растяжимости грудной клетки и легких ребенка и от сопротивления дыхательных путей. Высокая растяжимость легких и грудной стенки может привести к чрезмерному раздуванию альвеол и к их разрыву. Однако сниженная растяжимость может привести к гиповентиляции и ателектазам.
Перемежающаяся принудительная вентиляция позволяет ребенку дышать самостоятельно из источника газа при малом сопротивлении, периодически получая дыхательный объем с помощью механического респиратора через заданные временные интервалы. Перемежающаяся принудительная вентиляция производится с помощью непрерывной цепи или с помощью систем клапанов. Непрерывные цепи просты и не требуют дополнительных усилий со стороны пациента при спонтанном дыхании. Системы клапанов могут быть не эффективны у детей, которые имеют относительно высокую частоту дыхания, потому что чувствительность и время отклика клапана не позволяют аппарату ИВЛ работать синхронно с вдохами пациента. При вентиляции с повышенным давлением каждое спонтанное дыхание дополнено поставкой газа в заданном давлении. Пациент определяет темп дыхания и время вдоха, аппарат определяет давление на вдохе. Вентиляция с поддержанием давления увеличивает дыхательный объем, может уменьшить работу дыхания и улучшить комфорт пациента. Такой режим вентиляции обычно используется, чтобы отучить пациента от ИВЛ. Режим поддержания давлением не будет работать, если у пациента имеется аномальный дыхательный водитель ритма.
Лучшее понимание этой патологии привело к таким режимам вентиляции, в которых используют довольно длительные вдохи, высокое положительное давление в конце выдоха и маленький дыхательный объем. Эти режимы вентиляции с защитой легкого приводят к снижению минутной вентиляции и повышению PaCO. Они также уменьшают поперечные силы, действующие на терминальные отделы дыхательных путей, и возвращают в процесс дыхания участки легкого из мертвого пространства. Кислотно-основное состояние может быть относительно нормальным, благодаря метаболическому алкалозу, вызванному задержкой бикарбоната в почках и назначением бикарбоната натрия или трисбуфера (трисаминометан).
Оптимальным образцом вентиляции для больных с обструктивным заболеванием дыхательных путей является более высокая скорость и меньшая продолжительность вдоха, и более длительный выдох, для улучшения вентиляции относительно нормального легкого и выведения газа из обструктированной части легких. Фармакологическая бронходилатация является основой лечения болезни мелких дыхательных путей. При проведении ИВЛ таким пациентам обычно происходят баротравма и альвеолярный разрыв.
-
Начало искусственной вентиляции.
Соотношение вдоха к выдоху 1-1,5:1 и относительно медленный темп вентиляции (<24 циклов/мин у младенцев и <16 циклов/ мин у детей) являются отправной точкой для многих пациентов. Параметры вентиляции изменяются на основании показателей газов крови, рН и сатурации.
Важными критериями для определения адекватности вентиляции являются расширение грудной клетки, аускультация легких и достаточность альвеолярной вентиляции (определяется по PaCO2). Нужно измерять максимальное давление в дыхательных путях, по возможности часто и как можно ближе к ЭТТ.
Следует начинать использование ПДКВ от уровня 3-4 см вод. ст. и увеличивать его постепенно на 2 см, пока не станет адекватной SaO. Некоторые дети нуждаются в давлении в конце выдоха более 20 см вод. ст.
Инициирование вентиляции с положительным давлением может привести к системной артериальной гипотензии, которая обычно купируется инфузией 10-20 мл/кг кристаллоидов, коллоидов или препаратов крови. Необходимо измерять ЦВД при значении ПДКВ более 10 см вод. ст. Измерение внутрисосудистого артериального давления и ЦВД позволяет обнаруживать вредное действие ИВЛ и положительного давления в дыхательных путях на сердечно-сосудистую систему.
Вспомогательная фармакологическая терапия: аналгетики и седативные препараты. Для того, чтобы помочь детям в сознании синхронизировать с механической вентиляцией, часто требуется седация. Количество необходимой седации зависит от возраста ребенка, его размера, основного заболевания и от количества необходимой дыхательной поддержки. Некоторые младенцы достаточно спокойны и не требуют применения седативных препаратов. Седация позволяет пациентам дышать синхронно с респиратором, который снижает пиковое давление в дыхательных путях, устраняет кашель и напряжение, которые могут привести к утечке газа из легких. Непрерывная инфузия фентанила (1-2 мкг/кг/ч) обеспечивает обезболивающий и седативный эффекты. Однако это может привести к необходимости увеличить объем введения фентанила в последующие дни, для сохранения того же уровня седации. Другие препараты, такие как лоразепам (0,1-0,2 мг/кг внутривенно каждые 4-6 ч) или мидазолам (0,05-0,2 мг/кг/ч), могут быть полезным дополнением к опиоидам. Обычно у этих препаратов отмечается минимальный сердечно-сосудистый эффект при достаточном объеме сосудистого русла. Однако назначение лоразепама недоношенным новорожденным в течение нескольких дней может привести к гипотензии, чувствительной к стероидам, в результате накопления препарата в организме. У недоношенных новорожденных период полувыведения лоразепама составляет около 72 ч. Введение препарата каждые 4-6 ч приводит к его накоплению в крови и тканях.
Миорелаксанты увеличивают растяжимость грудной стенки, снижают потребление кислорода и облегчают искусственную вентиляцию легких. При их использовании терапию нужно дополнять препаратами, вызывающими амнезию, седацию и обезболивание.
Панкуроний и векуроний являются наиболее часто используемыми миорелаксантами в ПОИТ. Стандартная доза панкурония – 0,1 мг/кг внутривенно каждые 1-1,5 ч или 40-100 мкг/кг/ч в виде инфузии. Тахикардия, связанная с панкуронием, является нежелательным побочным эффектом у взрослых, но, как правило, желательным у младенцев и детей, потому что она помогает поддерживать сердечный выброс на нормальном уровне. Векуроний (0,08-0,2 мг/кг, с последующей инфузией 60-150 мкг/кг/ч) меньше вызывает тахикардию, чем панкуроний; часто целесообразно использование цисатракурия (0,1-0,2 мг/кг, с последующей инфузией 60-120 мкг/кг/ч), потому что его элиминация не зависит от функционального состояния почек или печени. Если эти препараты назначаются более одного дня, следует рассматривать способ избегания их накопления в плазме и длительного паралича, в виде проведения регулярных «выходных дней» от них.
-
Отмена ИВЛ.
Критерии для отмены ИВЛ плохо определены. В общем, отмена респираторной поддержки начинается, когда сердечно-сосудистая система стабильна, ребенок бодрый и внимательный. Не следует отменять механическую вентиляцию, если имеется значительный риск острой сердечной декомпенсации. До начала отмены лучше откорректировать тяжелую анемию, гипогликемию или гипергликемию, гипернатриемию, гипохлоремию или истощение, поскольку эти метаболические расстройства у ребенка нарушают его способность отвыкания от ИВЛ. До рассмотрения отмены ребенок должен быть способен производить давление в дыхательных путях (сила вдоха) как минимум – 20 см вод. ст. и вдыхать не менее 10 мл/кг газа с максимальным усилием (жизненная емкость легких).
Шунтирование крови через невентилируемые области легких, приводящее к гипоксемии и тканевой гипоксии быть уменьшено при улучшении растяжимости легких, потому что в противном случае может произойти пневмоторакс и/или пневмомедиастинум.
Режим работы аппарата ИВЛ обычно не снижают до стабилизации показателей газов артериальной крови, вдыхаемой концентрации кислорода меньше 0,6, ПДКВ меньше 10 см вод. ст. и пикового давления в дыхательных путях ниже 30-35 см вод. ст.
Не должно быть никаких остаточных явлений от миорелаксантов, а уровень седации должен быть минимальным. Нервно-мышечная блокада может быть ликвидирована внутривенным введением неостигмина (0,050,07 мг/кг) и гликопирролата (0,01 мг/кг); приемлемая нервно-мышечная функция должна быть подтверждена с помощью стимулятора периферических нервов. Когда все эти показатели в порядке, в течение нескольких часов или дней постепенно уменьшают режим работы респиратора.
Отмена должна продолжаться до тех пор, пока газы артериальной крови не будут оставаться в допустимых пределах и пока клиническое состояние ребенка не стабилизируется. При усилении произвольной вентиляции увеличенная работа дыхания может ухудшить состояние ребенка. Признаками опасности являются тахикардия, гипертония или гипотония, тахипноэ, повышение работы дыхания и тревога. При появлении этих симптомов необходимо прекратить отмену и усилить респираторную поддержку. На протяжении отмены необходима частая оценка газов артериальной крови и клинического состояния ребенка. Если у ребенка имеется остаточное заболевание легких и снижение растяжимости легких, дальнейшее снижение функциональной остаточной емкости и увеличение гипоксемии могут отсрочить отмену. Риск возникновения этих потенциальных проблем можно свести к минимуму с помощью умеренных уровней постоянного положительного давления в дыхательных путях или ПДКВ (от 5 до 10 см вод. ст.) в течение отмены. Функциональная остаточная емкость аналогична таковой у новорожденных на искусственной вентиляции легких с ПДКВ 2 см вод. ст., как после экстубации трахеи.
Экстубация трахеи должна выполняться специалистом, так как может потребоваться повторная интубация. После экстубации трахеи FiO2 обычно увеличивается на 20%. Взрослым пациентам рекомендуется глубоко дышать, кашлять, освобождаться от секрета из дыхательных путей как можно чаще. Принудительная спирометрия, ранняя мобилизация и физиотерапия на грудную клетку являются важными составляющими при восстановлении после дыхательной недостаточности.
Перед экстубацией необходимо оценить качество и объем выделений из трахеи; пациенту будет трудно санировать большие объемы густого секрета после экстубации. Как правило, экстубацию трахеи лучше проводить, когда доступны весь медперсонал для внимательного наблюдения за ребенком и проведение рентгенографии грудной клетки. Если отмена ИВЛ и экстубация трахеи были тщательно продуманы и выполнены, то реинтубация бывает сравнительно редко.
-
Высокочастотная вентиляция.
Высокочастотная вентиляция обеспечивает меньший дыхательный объем, чем анатомическое мертвое пространство при высокой интенсивности дыхания (от 150 до 3000 вдохов/мин). Эффективным является применение нескольких различных типов аппаратов ИВЛ, таких как высокочастотный струйный респиратор, высокочастотный осциллирующий респиратор и прерыватели потока. Каждый из них отличается техническим дизайном и областью клинического применения; они могут дифференцироваться по механизму газообмена.
Высокочастотный осциллирующий респиратор обычно используется для новорожденных и детей с тяжелыми заболеваниями легких и дыхательной недостаточностью. Его использование сократило число младенцев, требующих проведения экстракорпоральной мембранной оксигенации (ЭКМО). Высокочастотная осциллирующая вентиляция также успешно применяется при лечении детей с острыми гомогенными интерстициальными и альвеолярными заболеваниями. Из-за физических ограничений оборудования эта форма вентиляции менее результативна в лечении старших детей и взрослых. Струйная вентиляция используется для лечения дыхательной недостаточности от многих причин, хотя основным показанием к ее использованию является лечение баротравмы или бронхоплеврального свища.
Экзогенный сурфактант
Терапия экзогенным сурфактантом стала в настоящее время стандартным лечением недостатка собственного сурфактанта у недоношенных детей с увеличением их выживаемости при снижении потребности в механической вентиляции и ЭКМО. Применение экзогенного сурфактанта у детей более старшего возраста и взрослых не эффективно, потому что причины заболевания разные. Пожилые пациенты чаще имеют нарушения функции сурфактанта, чем его количества.
Экстракорпоральная мембранная оксигенация (ЭКМО)
ЭКМО является стандартом лечения детей старше 34 недель жизни с острой дыхательной недостаточностью, которая не отвечает на стандартную терапию. Более 24000 младенцев, с прогнозируемой смертностью от 80% до 85% при обычном ведении, были пролечены с помощью ЭКМО, и более 80% этих пациентов выжили. Около 30% детей с поражением сердца (особенно миокарда) спасены благодаря ЭКМО. Большинство ЭКМО были вено-артериальными, где кровь забирается из венозной системы и возвращается в восходящую аорту. Веноартериальная ЭКМО поддерживает дыхательную и сердечную функции. Вено-венозная ЭКМО менее эффективна, но она сохраняет легочный кровоток и позволяет избежать катетеризации крупных артерий. Вено-венозная ЭКМО менее эффективна у пациентов с дисфункцией миокарда. Однако она стремительно набирает популярность и используется так же или чаще, чем вено-артериальная ЭКМО. Популяция новорожденных с показаниями для ЭКМО также меняется. Экзогенный сурфактант, ингаляционный NO и применение высокочастотного осциллирующего респиратора значительно сократили необходимость в экстракорпоральной мембранной оксигенации и перевели ее использование, в большей степени, для пациентов с сепсисом и полиорганной недостаточностью. Сегодняшние кандидаты для ЭКМО – это больные в более тяжелом состоянии, и, в основном, имеют сепсис и полиорганную недостаточность. ЭКМО для старших детей и взрослых с ОДН продолжает исследоваться. Было зарегистрировано примерно 7000 педиатрических пациентов с проведенной ЭКМО во всем мире. Это были пациенты, которым в 80% прогнозировался летальный исход. Около 50% пациентов с ЭКМО выжили. Причина этого различия в исходах двух возрастных групп связана с выраженной неоднородностью по возрасту, диагнозам, особенностям ведения, а также критериями для проведения ЭКМО. Кроме того, у новорожденных имеется немного причин ОДН, и большинство из них обратимы. Более взрослые пациенты имеют больше причин ОДН, которые не всегда обратимы.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания











Комментарии