Паразитарные заболевания печени: симптомы, течение, лечение
Эхинококкоз – один из самых широко распространённых по всему миру зоонозов. ВОЗ поставила задачу разработки стратегии, которая позволит контролировать заболевание. Наиболее часто встречается в Центральной и Южной Америке, Северной Африке, Азиатском и Средиземноморском регионах среди населения, занятого в животноводстве, особенно там, где жизнь домашних животных и людей тесно связана. Альвеококкоз встречается только в Северном полушарии, наиболее подвержен риску контингент, контактирующий с дикими животными (например, обработка шкурок) В природных очагах. Для РФ областями, неблагополучными по гельминтозам, являются, прежде всего, регионы Сибири и Дальнего Востока. Заболеваемость описторхозом неравномерна: 2/3 мирового ареала приходится на территорию РФ. Самым обширным и интенсивным очагом описторхоза является Обь-Иртышский регион, включающий 15 краёв и областей России и Казахстана. Наибольшее распространение описторхоз имеет в ХМАО-Югре (поражённость населения 85-95%), следующий по величине – очаг в бассейне Днепра и его притоков. Из-за миграции населения в последнее время часто типичные природноочаговые заболевания регистрируется вне эпидемических очагов.
В практике российских хирургов наибольшее значение имеют эхинококкоз и описторхоз.
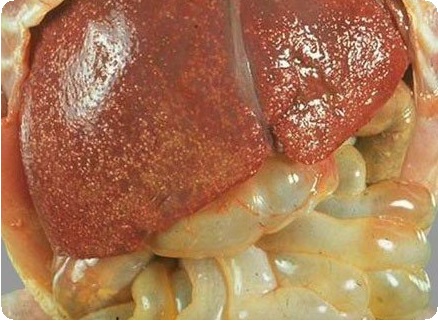
Эхинококкоз
Известно 4 возбудителя эхинококкоза:
-
echinococcus granulosus – эхинококкоз цистный (гидатидозный или однокамерный);
-
echinococcus multilocularis – альвеококкоз, альвеолярный эхинококкоз;
-
е. vogeli;
-
е. oligarthrus – редко встречаемые варианты.
Эхинококкоз – хронически протекаемое паразитарное заболевание человека и животных, развиваемое в результате проникновения в организм и развития в нём личиночной (ларвальной) стадии ленточного червя Е. granulosus.
Этиология
Половозрелые черви Е. granulosus паразитируют в кишечнике плотоядных рода Canidae (окончательный хозяин) – шакалов, волков, лис, но наибольшее эпидемиологическое значение имеет контакт людей с заражёнными домашними собаками. Червь длиной 2-7 мм состоит из головки (сколекса) с четырьмя присосками и крючьями и 3-4 члеников (проглотид). Последний из них содержит матку с яйцами паразита. Яйца эхинококков, имеющие плотную хитиновую оболочку, выделяются в окружающую среду, поедаются свиньями, овцами, коровами, верблюдами (промежуточный хозяин), где развивается личиночная стадия паразита (лавроциста) – кистозная. Далее окончательный хозяин поедает поражённые органы промежуточного хозяина. Человек заражается случайно при поедании яиц паразита и является биологическим тупиком для паразита. под влиянием желудочного сока хитиновая оболочка яйца растворяется, личинка внедряется в стенку желудка или кишки, таким образом, попадает в кровоток и далее в капилляры печени, где в 80% задерживается и начинает развиваться. Сначала формируется пузыревидная личинка – циста, по мере созревания в кисте развиваются оболочки, выводковые капсулы, сколексы и ацефалоцисты. Наиболее часто эхинококкоз наблюдается в печени (70-80%), лёгких (20%) и реже в головном мозге, селезёнке, почке, костях и спорадически в других органах.
Основные черты патологии
Пузырь эхинококка заполнен прозрачной жидкостью со сколексами различной степени зрелости и имеет трёхслойную стенку. Внутренняя стенка материнского пузыря (герминативная, зародышевая оболочка) имеет ростковый слой, далее он покрыт хитиновой оболочкой (белого цвета). Снаружи пузырь покрыт фиброзной капсулой — результат попытки хозяина отграничиться от эхинококка. Рост паразитарной кисты происходит аппозиционно – раздвигая ткани. Внутрь пузыря отпочковываются дочерние пузыри и сколексы (головки паразита). 1 л жидкости пузыря содержит до 2-3 см3 эхинококкового «песка», содержащего до 1 млн сколексов. Ацефалоцисты – стерильный эхинококковый пузырь без выводковых капсул и сколексов. В поражённом органе может развиваться одна киста – солитарное поражение, или несколько – множественный эхинококкоз.
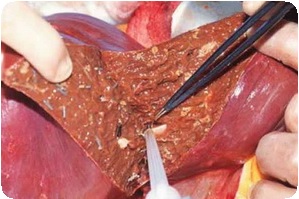
Классификация
В мире для сравнения результатов и стандартизации методов лечения наиболее часто используют классификацию эхинококкоза, основанную на ультразвуковой картине, которая учитывает активность процесса. Она утверждена рабочей группой ВОЗ по эхинококкозу (World Health Organization-Informal Working Groupon Echinococcosis) В 2001 Г.
Клиническая симптоматика
Поскольку развитие эхинококковой кисты происходит медленно, в течение десятков лет от начального размера в несколько миллиметров до кисты, содержащей несколько литров жидкости, то выделяют раннюю (бессимптомную), неосложнённую и осложнённую стадии.
На ранней стадии киста, как правило, не оказывает существенного давления на окружающие органы, и её чаще всего выявляют случайно во время профилактического УЗИ.
На неосложнённой стадии эхинококкоза печени из-за её увеличения за счёт растущей кисты появляется чувство тяжести в правом боку, боли в этой зоне и эпигастрии. При преимущественной локализации в правой доле – боли напоминают холецистит, в случае локализации в левой доле чаще возникают жалобы на тошноту и тяжесть в эпигастрии. При больших размерах кисты и локализации в передних и поверхностных отделах печени могут пальпироваться увеличенная печень или сферические образования с гладкой поверхностью. Длительность второго периода может быть несколько лет, а прогрессирование заболевания связано с ростом паразита, что приводит к появлению гепатоспленомегалии, желтухи, асцита.
Переход в осложнённую стадию предопределяется как трансформациями самой кисты, так и изменениями пораженного органа. Из-за сдавления желчных протоков развивается билиарная гипертензия, а компрессия воротной вены может приводить к признакам портальной гипертензии. К наиболее тяжёлым осложнениям, связанным с эхинококковой кистой, относят нагноение (асептический некроз или инфицирование), разрыв кисты (травматический или спонтанный), опорожнение кисты в просвет желчных протоков. Клиническая картина разрыва кисты зависит от иммунной реакции организма И может варьировать от крапивницы до анафилактического шока, кроме того, при прорыве кисты в свободную брюшную полость возникает риск диссеминации эхинококка.
Диагностика
Эпидемиологический анамнез – в эндемичных очагах все кисты печени следует первично рассматривать как эхинококковые. Серологическая диагностика основывается на выявлении антител к паразиту в крови пациентов. Осуществляется с помощью реакции непрямой гемагглютинации и иммуноферментного анализа. Серологические исследования используют не только для первичной диагностики эхинококкоза, но и для оценки результатов лечения. Рекомендуют проводить исследования через 3, 6 и 12 мес. после операции и далее 1 раз в год в течение 5 лет. Четырехкратное увеличение титра может свидетельствовать о рецидиве заболевания. Инструментальные методы – высокоинформативным методом диагностики эхинококкоза печени является УЗИ, которое позволяет установить локализацию, количество и качественные характеристики кист. КТ и МРТ носят уточняющий характер, позволяют оценить поражение других органов (лёгкие, головной мозг и т. д.). При подозрении на прорыв кисты в жёлчные протоки применяют ЭРПХГ.
Принципы лечения
Используют:
-
противопаразитарную химиотерапию;
-
пункционные методики;
-
хирургическое лечение.
Лекарственная терапия
Для лекарственной терапии эхинококкоза применяют препараты бензимидазола (альбендазол или мебендазол). Из-за меньшей токсичности предпочтение отдают альбендазолу, который назначают в дозе 10-15 мг/кг 2 раза в день, за 7 дней до оперативного лечения и далее несколько одномесячных курсов, разделённых 14-дневными интервалами. Обычно проводят от трёх до шести курсов.
Показания к лекарственной терапии:
-
предоперационная терапия и противорецидивная терапия после любого вида оперативного вмешательства;
-
спонтанный или травматический разрыв кисты. Лечение назначают в максимально короткие сроки от разрыва;
-
множественные кисты в одном или нескольких органах размером не более 3,5 см;
-
в случаях невозможности или противопоказаний к оперативному лечению.
При поражении сердца или головного мозга химиотерапию проводят только после удаления кист, вне зависимости от их размера.
Неблагоприятные последствия химиотерапии бензимидазолами:
-
гепатотоксичность (транзиторное повышение аминотрансфераз);
-
нейтропения;
-
тромбоцитопения;
-
алопеция;
-
эмбриотоксичность.
Пункционно-дренажные методики
Метод PAIR (Puncture, Aspiration, Injection, Re-aspiration – пункция, аспирация, инжекция, реаспирация).
Показания для PAIR:
-
анэхогенное поражение диаметром больше или равно 5 см (CE1);
-
киста с дочерними цистами (CE2) и/или с определяемой мембраной (CE3);
-
многокамерная киста, доступная для пункции;
-
инфицированная киста.
Дополнительные показания: беременные; дети старше 3 лет; пациенты, не демонстрирующие ответ на химиотерапию, а также те, которым хирургическое лечение противопоказано или которые отказались от хирургического лечения; рецидив после хирургического лечения.
Противопоказания для PAIR:
-
отсутствие безопасной траектории для пункции или рискованная локализация;
-
кисты, локализуемые в спинном мозге, головном мозге, сердце;
-
неактивная стадия и кальцинированная киста;
-
киста, связанная с жёлчными протоками;
-
киста, прорвавшаяся в брюшную полость, бронхи или мочевыводящий тракт.
Преимущества PAIR:
-
минимально-инвазивная процедура;
-
меньше рисков по сравнению с хирургическим вмешательством;
-
подтверждение диагноза;
-
удаление большого количества сколексов при аспирации жидкости кисты;
-
увеличивает эффективность лекарственной терапии, назначаемой до- или после пункции (возможно, из-за увеличения проницаемости для антигельминтных препаратов);
-
уменьшение продолжительности госпитализации;
-
стоимость пункции и химиотерапии обычно меньше затрат на хирургическое лечение или химиотерапию.
Осложнения ириски PAIR:
-
осложнения, свойственные любой пункции (кровотечения, механическое повреждение тканей, инфицирование);
-
анафилактический шок или другие аллергические реакции;
-
риск обсеменения из-за попадания содержимого кисты в свободную брюшную полость;
-
химический (склерозирующий) холангит, если киста имеет связь с жёлчными протоками;
-
быстрая декомпрессия кисты, может приводить к формированию цистобилиарных фистул;
-
выживание дочерних кист;
-
системная токсическая реакция от вводимых гермицидов (особенно при необходимости введения больших их объёмов).
Хирургическое лечение
Принципы хирургического лечения подразумевают эрадикацию паразита, предупреждение обсеменения окружающих тканей, закрытие остаточной полости. В качестве гермицида для обработки полости кисты рекомендуется 80-100% раствор глицерина или 30% раствор хлористого натрия. Независимо от доступа (открытый или лапароскопический) принципы должны быть соблюдены. Объём оперативного лечения определяют размер, количество, локализация кист и активность процесса. Виды хирургического лечения.
Радикальное:
-
перицистэктомия – удаление паразита вместе с фиброзной оболочкой;
-
цистэктомия, эхинококкэктомия – удаление элементов эхинококковой кисты без фиброзной оболочки;
-
резекция органа.
Консервативное:
-
наружное дренирование;
-
фенестрация;
-
марсупилизация;
-
частичная цисто-перицистэктомия.
Альвеококкоз
Отличительной эпидемиологической особенностью альвеококкоза (Echinococcusmultilocularis) от гидатидозного эхинококкоза (Echinococcus granulosus) является циркуляция в природных очагах между дикими плотоядными животными (окончательный хозяин) и мышевидными грызунами (промежуточный хозяин).
Основные черты патологии
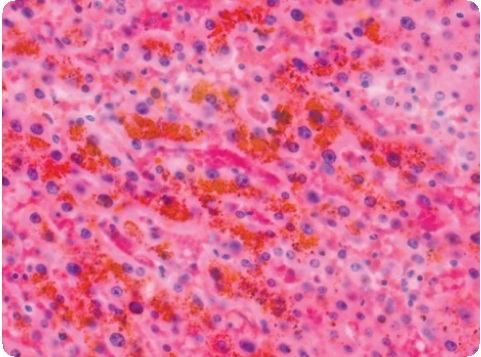
Заражение человека происходит при контакте с плотоядными животными или при обработке их шкур. Тяжёлое течение и плохой прогноз альвеококкоза при несвоевременной диагностике предопределяет инфильтративный характер роста «паразитарной опухоли», состоящей из множества мелких пузырьков, окружённых фиброзной капсулой. В подавляющем большинстве случаев органом-мишенью для альвеококка является печень человека, а поражение других органов (лёгкие, головной мозг, почки, селезёнка, мышцы, брюшина, брыжейка) осуществляется путём инфильтративного роста (паразит выделяет гиалуронидазу, растворяющую окружающие ткани) или метастазирования. Образовавшиеся в печени узлы представляют собой очаги продуктивно-некротического воспаления беловатого цвета, диаметром от 0,5 до 30 см и более, с прорастанием поверхности печени и соседних органов.
К специфическим осложнениям следует отнести холангиты, абсцессы печени, нагноением распад узлов, а также цирроз печени. При прорастании желчных протоков развивается механическая желтуха. При некрозе паразитарного узла в его центральных отделах формируются полости с ихорозным или гнойным содержимым.
Клиническая симптоматика
Отличительная особенность альвеококкоза – длительно протекающий бессимптомный период заболевания (доклиническая стадия), что связано с медленным ростом паразита и особенностями иммунитета коренного населения в эндемических очагах. В развитии заболевания выделяют раннюю неосложнённую стадию, стадию осложнений и терминальную стадию. При ранней стадии заболевания общее состояние удовлетворительное, трудоспособность сохранена, однако отмечаются периодические ноющие боли в печени, а также ощущения тяжести в правом подреберье и в эпигастральной области. Печень на 2-3 см выступает из-под края правой рёберной дуги, при пальпации могут определяться участки каменистой плотности (симптом Любимова).
В стадии развития осложнений отмечаются механическая желтуха и гнойный холангит с абсцедированием, а при сдавлении ворот печени – признаки ПГ. Тогда же появляются признаки функциональных нарушений печени. Наиболее яркую клиническую картину наблюдают при нарушении целостности и прорыве содержимого полости распада в брюшную или плевральную полость с развитием явлений перитонита или эмпиемы плевры. Наиболее тяжёлые осложнения альвеококкоза связаны с метастазированием возбудителя в головной мозг и лёгкие. В терминальной стадии болезни развиваются необратимые обменные нарушения и кахексия.
Диагностика основывается на эпидемиологических данных, результатах серологических исследований, УЗИ и КТ брюшной полости.
Лечение
Основной метод лечения альвеококкоза – хирургический. Возможности оперативного лечения в основном зависят от степени вовлечения печёночной ткани в патологический процесс. Все оперативные вмешательства можно разделить на 4 группы:
-
радикальные оперативные вмешательства, при которых выполняют резекции печени с удалением паразитарных узлов;
-
условно-радикальные – при этом удаляют основную массу поражённой печёночной ткани, а оставшиеся небольшие поражённые участки обрабатывают химическими противопаразитарными средствами;
-
паллиативные резекции с криообработкой поражённого среза
-
симптоматические вмешательства, направленные на устранение осложнений (желтуха, перитонит).
В комплексном лечении неоперабельных больных используют химиотерапию.
Больные альвеококкозом должны находиться на пожизненной диспансеризации и в случае рецидива – госпитализироваться в стационар.
Описторхоз
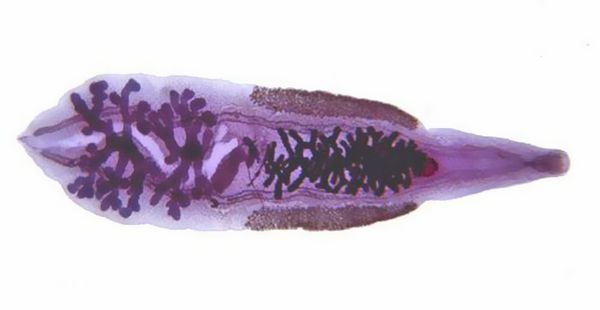
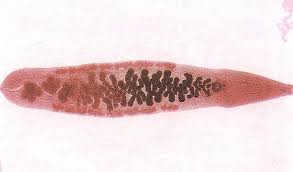
Описторхоз – системное заболевание, возбудителями которого являются трематоды: Opisthorchis felineus и Opisthorchis viverrini, паразитирующие в желчных протоках и поджелудочной железе.
В России зарегистрирован Opisthorchis felineus (кошачья двуустка). Это плоский червь ланцетовидной формы, длиной 3-13 мм и шириной 1-3,5 мм, гермафродит.
Основные черты патологии
В цикле развития кошачьей двуустки необходимо участие трёх хозяев – два промежуточных (моллюски и рыбы) и окончательный (человек, кошки, собаки и др.). При поедании поражённой рыбы личинки (метацеркарии) попадают в желудок, где под действием желудочного сока и желчи освобождаются от соединительнотканной оболочки и, продвигаясь по желудочно-кишечному тракту и протокам желчевыводящей системы (благодаря положительному хемотаксису к желчи), через 3-5 ч достигают желчного пузыря, печени и поджелудочной железы. При этом условия существования метацеркариев в поджелудочной железе менее благоприятны. Описторхисы в печени обнаруживают в 100% случаев инвазий, в желчном пузыре – в 60%, в поджелудочной железе – в 36%.
Классификация
Стадии (фазы) описторхоза:
-
острая – субклиническая или манифестная формы заболевания;
-
латентная;
-
хроническая – субклиническая или манифестная форма кистозной трансформации желчных протоков;
-
фаза исхода (необратимых изменений).
Патогенез и патоморфология описторхоза
Основными патогенетическими факторами являются: механический, аллергический, нейрогенный и вторично-инфекционный. Описторхисы повреждают стенки желчных и панкреатических протоков присосками и шипиками. Образуется множество эрозий, что стимулирует регенеративно-гиперпластическую реакцию эпителия. Наряду с этим скопление в желчных и панкреатических протоках гельминтов, их яиц, слизи, эпителия создаёт препятствие для оттока желчи и секрета, что приводит к развитию билиарной гипертензии. Механическое раздражение интерорецепторов желчных и панкреатических протоков вызывает возникновение патологических нервных импульсов, что влечёт за собой нарушение функций ДПК и желудка, дискинезию желчного пузыря и дисфункцию сфинктеров Люткенса и Одди.
Существенное значение в патогенезе описторхоза и его осложнений имеет вторичная инфекция, проникающая в печень через жёлчные протоки и гематогенным путем. При присоединении инфекции у больных развиваются такие осложнения, как гнойный холангит, холангитические абсцессы, жёлчный перитонит. Однак, ведущим фактором следует признать аллергическую перестройку организма, возникающую в результате сенсибилизации его продуктами обмена и распада описторхов, аутосенсибилизацию продуктами распада собственных тканей.
Клиническая симптоматика
Описторхоз с одинаковой частотой встречается у мужчин и женщин, чаще в возрасте от 20 до 40 лет. Инкубационный период обычно равен 1-6 нед. Затем наступает острый период, который характеризуется общей слабостью, головной болью, лихорадкой неправильного типа, с ознобами, повышенной потливостью, болями в мышцах и суставах, в области печени, характерны диспепсические расстройства, могут наблюдаться кашель, одышка, боль в груди. Условно выделяют четыре клинических варианта острой фазы описторхоза:
-
тифоподобный;
-
гепатохолангитический;
-
гастроэнтерологический;
-
латентный.
Гепатохолангитический вариант встречается наиболее часто. Имеются характерные особенности острого описторхозного холецистохолангита. Во-первых, токсическое воздействие продуктов жизнедеятельности паразитов, сенсибилизация, развитие аллергии, механическое раздражение интерорецепторов билиарного тракта гельминтами, приступы дискинезии желчных путей вызывают функциональные расстройства центральной нервной системы. Больные становятся раздражительными, легковозбудимыми, развиваются головные боли, снижение памяти, потливость, тремор пальцев. Во-вторых, имеется увеличение печени и желчного пузыря у подавляющего числа больных (80%). Жёлчный пузырь при этом может содержать до 0,7-1,0 мл изменённой желчи. В-третьих, на фоне желчной гипертензии нередко возникают пропотной или перфоративный жёлчный перитонит. Пропотевание желчи происходит не только через истончённую и растянутую стенку желчного пузыря, но и через стенки многочисленных субкапсулярных холангиоэктазов, перфорации последних также нередки.
После перенесения острой фазы заболевание переходит в хронический процесс, при котором периоды обострения сменяются периодами затишья. Клиническая картина хронической фазы полиморфна. Можно выделить несколько синдромов, которые встречаются изолированно или вместе: синдром гастродуоденальной диспепсии, ангиохолецистита, панкреатита, цирроза, а может быть бессимптомное течение. Наиболее часто встречается синдром, указывающий на поражение желчного пузыря и желчных путей. Частой жалобой больных являются боли в правом подреберье. Присоединяются диспепсические явления, головная боль, головокружение, бессонница, раздражительность, субфебрильная гипертермия. У 62% пациентов отмечается увеличение печени, у 46% – субиктеричность кожи, у 0,5% – желтуха. Закупорка желчных протоков гельминтами, продуктами их обмена и яйцами, токсико-аллергическое действие описторхов на билиарную систему, присоединение вторичной инфекции, реактивный перихолангиосклероз обусловливают билиарную гипертензию (внутрипечёночный холестаз).
Основой всех хирургических осложнений описторхоза является желчная гипертензия, которая служит пусковым моментом в формировании холангиоэктазий, гнойного холангита, холецистита, холангиогенных абсцессов печени, перфорации субкапсулярных желчных протоков и желчного перитонита. По данным исследователей, у 50% больных определяется обтурационный холецистит, у 40% – рубцовая стриктура дистального отдела холедоха и большого дуоденального сосочка, у 10% – склерозирующий холангит. По вопросу о значении описторхозной инвазии в образовании камней в желчном пузыре единого мнения нет. Большинство исследователей считают, что описторхоз является одним из существенных факторов возникновения первичного рака печени.
Диагностика
Постановка диагноза описторхоза основывается на клинической картине, в которой далеко не часто можно выявить специфические симптомы. Ценные указания на наличие описторхозной инвазии может дать исследование крови, выявляющее эозинофилию. Снижаются пигментная, белковообразовательная функции печени, активность сывороточных ферментов. Наиболее выраженные отклонения обнаруживают в ранней фазе описторхоза, и в совокупности с клиническими симптомами и патоморфологическими изменениями в печени они укладываются в синдром холангиогепатита. В хронической фазе описторхоза нарушение функции печени обнаруживают у 3/4 больных. Они выражаются в диспротеинемии, гипергаммаглобулинемии, снижении сулемового титра крови, снижении содержания в крови холестерина и уровня сывороточного железа. Однако достоверно диагноз устанавливают только при нахождении яиц описторхов в дуоденальном содержимом или в испражнениях, что становится возможным только на 3-4-й неделе заболевания. Существует иммунная диагностика описторхоза: кожно-аллергические пробы, определение сывороточных антител, иммуноферментный анализ.
Лучевые и эндоскопические методы значимы в диагностике заболевания и его осложнений и в определении тактики лечения: ЭГДС, ЭРПХГ, УЗИ, КТ, МРТ. Особенности УЗИ-картины при описторхозе: увеличение печени, желчного пузыря, утолщение и повышение эхогенности внутрипечёночных протоков и воротной вены, участки локального расширения просвета внутрипечёночных желчных протоков (холангиоэктазы), множественные, мелкие, тонкостенные, неправильной формы кисты печени.
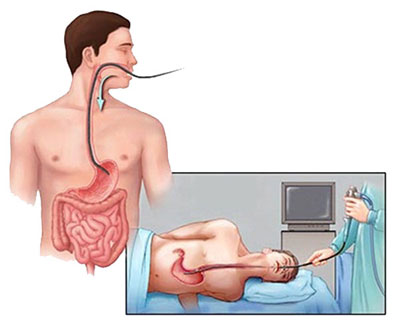
Лечение
Контроль эффективности дегельминтизации проводят через 1, 3 и 6 мес после лечения: выполняются гельминтоовоскопические исследования фекалий не менее 3 раз в каждый из указанных сроков и исследование дуоденального содержимого. Паразитологическое выздоровление далеко не всегда сопровождается клиническим выздоровлением: у лиц, страдавших описторхозом более 5 лет, сохраняются жалобы и объективные изменения, сформировавшиеся в хроническую фазу болезни, что обусловлено наличием глубоких морфологических изменений в органах. Вопрос же о тактике лечения резидуальных форм описторхоза остаётся до сих пор нерешённым.
Хирургическое лечение и особенности хирургической тактики
Оперативному лечению больные описторхозом подлежат лишь при наличии осложнений. Структура наиболее частых хирургических осложнений описторхоза:
-
в 70% случаев – стриктура пузырного протока;
-
в 44,6% – гнойный холангит;
-
в 35% – желтуха;
-
в 22,5% – стенозирующий папиллит;
-
в 24,3% – местный и общий перитонит;
-
в 17% – склерозирующий панкреатит;
-
в 14,2% – холедохолитиаз;
-
в 4,7% – склерозирующий холангит;
-
в 2,3% – кисты и абсцессы печени.
Одно из условий успешного лечения этих больных – своевременная нормализация оттока желчи, что и является основной задачей хирургического вмешательства. По поводу необходимости холецистэктомии при хроническом описторхозном холецистите мнения разных авторов расходятся. Одни считают, что застойный жёлчный пузырь не является показанием к его удалению (при отсутствии в нём деструктивных процессов). Другие – холецистэктомию считают обязательной, обосновывая это тем, что в 70% имеется стенозирующий шеечный холецистит, что ведёт к частым рецидивам обострений.
При наличии небольших кист без клинической симптоматики показано наблюдение с обязательной дегельминтизацией. Хирургическое лечение показано при больших кистах диаметром более 5-10 см, множественных кистах, расположенных в одной анатомической области, при сочетании кист с холелитиазом, обструкцией внепечёночных желчных протоков, разрыве и нагноении. Лечение описторхозных абсцессов печени определяется рядом факторов: преимущественно холангиогенный характер с разнообразием размеров и множественностью локализации, выраженность деструктивных изменений, наличие осложнений. При преимущественно инфильтративном характере поражения с незначительным деструктивным компонентом возможно консервативное лечение. При наличии преимущественно деструктивных изменений вследствие нагноения холангиоэктазов, кист, гнойного обструктивного холангита показано хирургическое лечение: санация билиарного тракта с использованием эндоскопических транспапиллярных или чрескожных вмешательств, пункция и дренирование полостей под УЗИ, КТ-контролем, вскрытие и дренирование абсцессов открытым способом, резекция печени.
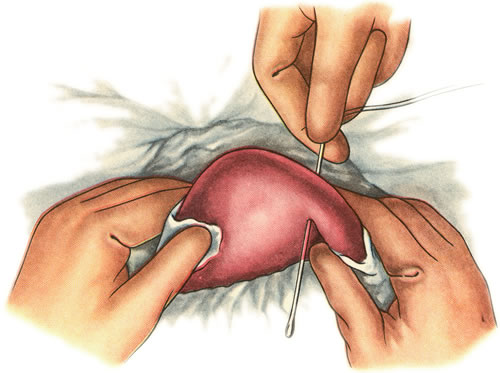
Можно выделить следующие особенности хирургической техники при описторхозе:
-
использовать в качестве доступа срединную лапаротомию или лапароскопию, а не разрез по С.П. Фёдорову, в связи с увеличенной печенью и низким расположением желчного пузыря;
-
все манипуляции с печенью производить бережно, чтобы не повредить тонкостенные холангиоэктазы;
-
необходимо перевязать или клипировать все, даже мельчайшие холангиоэктазы во избежание желчеистечения в послеоперационном периоде на фоне внутрипечёночной гипертензии;
-
жёлчный пузырь следует выделять под контролем зрения только острым путём, стараясь оставить на поверхности печени как можно больший слой склерозированной стенки пузыря;
-
раневую поверхность печени необходимо дополнительно герметизировать, используя гемостатические пластины, тампонировать сальником на ножке;
-
чаще прибегать к наружному дренированию желчных путей (для ликвидации гипертензии и санации);
-
обязательно дренировать подпечёночное пространство через дополнительный разрез в подреберье, так как, несмотря на все меры предосторожности, в первые 2-3 дня может иметь место подтекание желчи;
-
лапароскопическая холецистэктомия и лапароскопические вмешательства по поводу кист печени (фенестрация с деструкцией оставшихся стенок, цистэктомия, резекция печени) сопровождаются рядом дополнительных трудностей, обусловленных спаечным перипроцессом, сложностями в идентификации трубчатых структур, проблемами в достижении надежного гемо- и холестаза.
Послеоперационное ведение
Особенности послеоперационного ведения больных определяются необходимостью и целесообразностью проведения дегельминтизации, если она не проведена в дооперационном периоде (у плановых больных – за 1-2 мес. до операции). Если оперативное вмешательство завершено наружным дренированием желчных протоков, возможно проведение курса антигельминтной санации йод + калия йодид + поливиниловый спирт (йодинол) по способу Б.И. Альперовича (1989): через дренаж в желчных протоках вводят 2-3 мл йода + калия йодид + поливиниловый спирт (йодинол) в 10 мл 0,02% нитрофурала (фурацилин) в течение 2-3 нед. Возможно проведение дегельминтизации через 3 мес. после операции.
Прогноз
Как правило, прогноз даже при развитии хирургических осложнений при условии выполнения стандарта лечения благоприятен, однако это не исключает риск повторного заражения при проживании в эндемичном регионе, в связи с чем, необходимо строгое соблюдение правил профилактики.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания









Комментарии