Злокачественная опухоль сердца: симптомы, лечение, прогноз
Первичные злокачественные опухоли сердца составляют, по данным патологоанатомических исследований, 25% от их общего числа, тогда как частота их выявления в клинических условиях колеблется от 2 до 17%. Более 75% этих новообразований представлены саркомами, которые могут исходить из любого клеточного элемента сердца, что и предопределяет разнообразие их морфологической картины и сложность гистологической идентификации. Чаще всего встречаются:
-
ангиосаркомы;
-
рабдомиосаркомы;
-
фибросаркомы;

которые в совокупности составляют около 70% всех первичных злокачественных неоплазм сердца. В литературе описаны и другие случаи редких видов сарком сердца:
-
нейросаркомы;
-
лимфосаркомы;
-
гемангиоэндотелиосаркомы;
-
лейомиосаркомы;
-
мезотелиосаркомы;
-
миксосаркомы;
-
липосаркомы;
-
остеосаркомы;
-
хондросаркомы и многие другие.
Поражаются различные отделы сердца. Эти опухоли отличаются быстрым инвазивным ростом, приводящим к прорастанию всех слоев сердца и близлежащих органов, а также быстрым и обширным метастазированием в другие органы.
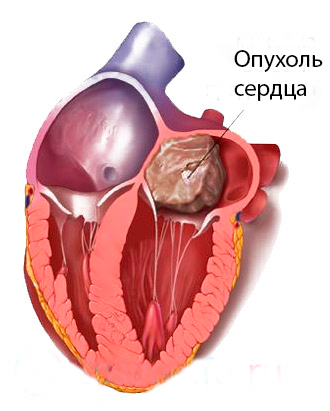
Первичные саркомы сердца могут располагаться эпикардиально, не проникая в полости сердца, а также эндокардиально и интрамурально, поражая при этом миокард. Как уже отмечалось выше, саркомы преимущественно исходят из правых отделов сердца, в основном из стенок правого предсердия, реже локализуются в желудочках. Злокачественные новообразования могут вызывать окклюзию клапанных отверстий и выводных отделов желудочков сердца, сдавливать или прорастать коронарные сосуды, крупные артерии и вены.
Ангиосаркома сердца
Ангиосаркома сердца — наиболее часто встречающаяся злокачественная опухоль сосудистого происхождения, составляющая 2,1-7,3% всех его новообразований. Гистологически эта опухоль представляет собой разновидность злокачественной гемангиоэндотелиомы и гемангиоперицитомы. Схожесть их течения и прогноза послужила основанием для использования в клинической практике собирательного термина «ангиосаркома».
Макроскопически ангиосаркомы представляют собой плотные образования, инфильтрирующие окружающие ткани, с очагами некроза и кровоизлияний на разрезе. Микроскопически эти опухоли имеют полиморфное строение. Они образованы веретенообразными или округлыми клетками, формирующими беспорядочно расположенные тяжи. Характерно, что в опухолевой ткани возникают сосудистые полости и каналы различного размера и конфигурации, анастомозирующие между собой и заполненные кровью.
Прогноз при ангиосаркомах сердца плохой. Большинство больных умирают в сроки 2-12 мес после появления симптомов заболевания.
Рабдомиосаркома сердца
Рабдомиосаркома сердца, так же как ангиосаркома, относится к числу часто встречающихся злокачественных опухолей. Наблюдается в любом возрасте.
Макроскопически опухоль представляет собой узловое образование в толще миокарда, с блестящей белесоватой поверхностью, белого или розоватого цвета, мягкой консистенции. На разрезе ткань пёстрая, с участками типа рыбьего мяса, преобладают кровоизлияния и некрозы. Микроскопически опухоль имеет пучковое строение и выраженный полиморфизм. Опухолевые клетки этого новообразования напоминают мышечные клетки на разных стадиях развития. В зависимости от этапа эмбриогенеза различают следующие виды рабдомиосарком:
-
эмбриональная;
-
альвеолярная;
-
плеоморфная;
-
смешанная.
Часто рабдомиосаркома состоит в равной мере из одинакового количества округлых, овальных и веретенообразных клеток. Эти новообразования обладают выраженным внутриполостным ростом, с быстрым развитием обтураций и врастанием в сердечные клапаны.
Прогноз при рабдомиосаркомах сердца плохой. Преобладающее большинство больных умирают в течение года с момента установления диагноза.
Лейомиосаркома сердца
Лейомиосаркома сердца — злокачественная опухоль мышечной ткани. Макроскопически опухоль представляет собой образование мягкой консистенции, серовато-желтого цвета, с капсулой и блестящей поверхностью; неоплазма обладает внутримиокардиальным ростом, часты инвазии в легкие и другие соседние органы. Встречается в большинстве случаев в предсердиях, часто бывает билатеральной. Микроскопически опухоль полиморфна, в строме выявляются гигантские клетки веретенообразной формы, образующие пучковые мышечные структуры.
Фибросаркома сердца
Фибросаркома сердца — злокачественная опухоль волокнистой соединительной ткани, составляющая 1,9-2,6% всех его первичных новообразований. Она встречается у больных обоего пола в любом возрасте. В патологический процесс одинаково часто вовлекаются правые и левые отделы сердца, причем в 64,2% случаев наблюдается множественный характер поражения. В половине наблюдений эти опухоли характеризуются выраженным внутриполостным ростом, приводят к частичной окклюзии и инвазии клапанного аппарата, наиболее часто — митрального клапана. Инвазия перикарда и отдаленные метастазы выявляются в 35,7% случаев при диагностике заболевания.
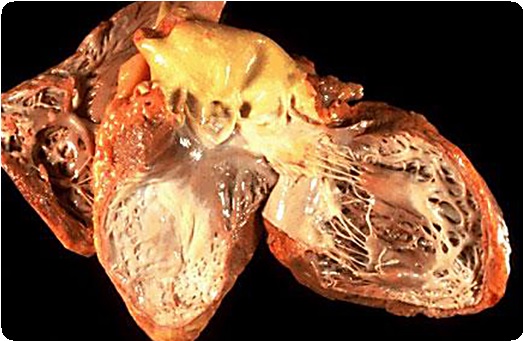
Макроскопически эта неоплазма представляет собой серовато-белое образование, плотной консистенции, с преобладающим инфильтративным ростом. Микроскопически состоит из фибробластоподобных клеток и коллагеновых волокон, представляющих клеточно-волокнистые тяжи, с обилием неправильных митозов и участков миксоматоза.
Прогноз при фибросаркомах сердца плохой. Все больные умирают в течение 2 лет после появления симптомов заболевания.
Липосаркома сердца
Липосаркома сердца — злокачественная опухоль из соединительной ткани и ее производных, по своему строению напоминает жировую ткань эмбриона с выраженным полиморфизмом. Макроскопически эта опухоль представляет конгломерат узлов плотной консистенции, бело-желтого цвета, на разрезе видны участки кровоизлияний и некроза. Микроскопически выявляются звездчатые и веретенообразные клетки, липоциты, жировые вакуоли и зрелые жировые клетки. Липосаркомы в равной мере поражают как правые, так и левые отделы сердца, с возможным развитием внутримиокардиального роста.
Прогноз при липосаркомах сердца, как и при перечисленных формах сарком, плохой, но все же липосаркома отличается относительно медленным ростом и редким метастазированием.
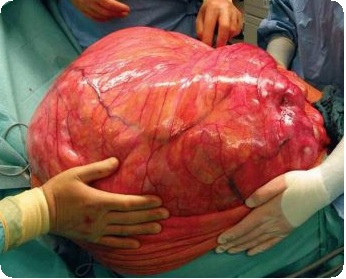
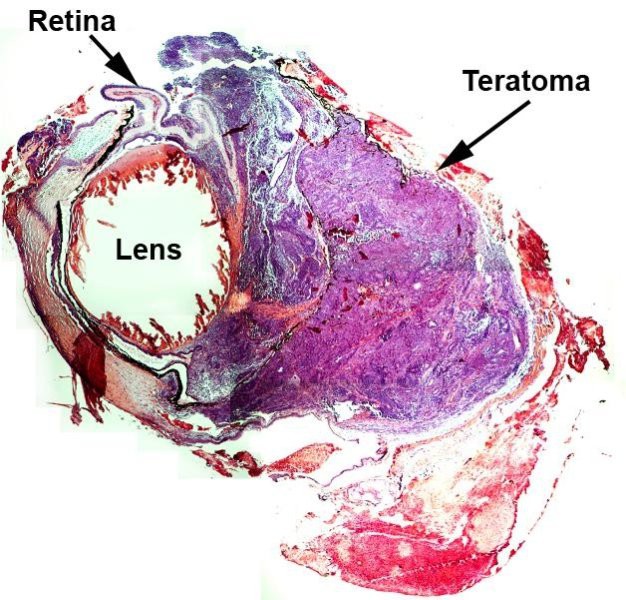
К первичным злокачественным новообразованиям сердца относятся также остеосаркома, хондросаркома, нейрогенная саркома, лимфосаркома, злокачественная тератома. Перечисленные опухоли встречаются редко, но сообщения, имеющиеся в мировой литературе по указанной патологии, свидетельствуют об их чрезвычайно неблагоприятном прогнозе, все больные умирают в течение 1 года-2 лет после появления первых симптомов заболевания.
Метастатические опухоли сердца
Метастатические опухоли сердца у детей — явление крайне редкое. В основном это опухоли мышечного происхождения, расположенные в правом желудочке и на трехстворчатом клапане. Внутрисердечная опухоль на ножке в виде опухоли Вильямса может заполнять просвет правого предсердия и желудочка, вызывая выраженное нарушение гемодинамики, не поражая при этом сам миокард.
У взрослых пациентов метастатические опухоли встречаются в 40 раз чаще, чем первичные опухоли сердца. Вторичные опухоли сердца встречаются в 13-40 раз чаще, чем первичные. Метастазирование в сердце или прорастание опухоли в миокард и перикард регистрируется, по различным данным, у 0,3-27% пациентов, умерших от злокачественных новообразований. Наиболее часто такое вторичное поражение наблюдается при раке легкого, пищевода, молочной или щитовидной железы, а также при меланомах, лимфомах, миеломах, лимфогранулематозе. Метастазы в сердце могут быть узловатыми или разлитыми, могут располагаться эндокардиально или эндоперикардиально, а иногда одновременно поражать обе структуры. Чаще всего поражение эндокарда приводит к образованию пристеночного тромба, а поражение перикарда вызывает его воспаление с геморрагическим экссудатом, приводящим к тампонаде сердца и нарушению гемодинамики.
Клиника
Именно особенности локализации опухолей сердца определяют проблемы диагностики и дифференциальной диагностики этого заболевания. Распознавание первичных опухолей сердца чрезвычайно затруднено в связи с отсутствием патогномоничных признаков и возможностью бессимптомного течения болезни. Клинические проявления опухолей сердца достаточно неоднородны и зависят не только от гистологического строения неоплазмы, но в основном от характера их роста, размера, локализации, степени внутрисердечной обструкции или деформации проводящей системы. Изолированные небольшие по размерам опухоли, расположенные в одном из желудочков, могут протекать бессимптомно, в то время как обширное новообразование с поражением миокарда приводит к выраженной сердечной недостаточности, являющейся причиной летального исхода. Опухоли больших размеров, выступающие в полости сердца, могут вызывать нарушение притока или оттока крови в полости сердца. Локализуясь в различных камерах сердца, опухоли чаще всего симулируют клиническую картину стеноза того или иного клапанного отверстия. У ребенка сужение просвета трехстворчатого клапана опухолью вызывает цианоз, обусловленный изменением тока крови через открытое овальное окно. Стеноз митрального клапана или его недостаточность могут быть вызваны рабдомиомой. Значительное гемодинамическое сужение выводного тракта правого или левого желудочка может быть обусловлено рабдомиомой, фибромой и тератомой. Опухоли больших размеров могут значительно снижать объем левого желудочка, без изменения его приточного или выводного тракта, вызывая при этом нарушение сократительной функции миокарда и левожелудочковую недостаточность.
Еще одним из симптомов опухолевого процесса является нарушение ритма сердца в результате поражения его проводящей системы. Описаны случаи развития:
-
полной AV-блокады;
-
суправентрикулярной и вентрикулярной тахикардии;
-
синдрома тахи-брадикардии;
-
синдрома внезапной смерти.
В отдельную группу выделяют симптомы, вызванные развитием миксомы. Диапазон клинических проявлений миксом обусловлен нарушением притока или оттока крови из пораженной камеры сердца, эмболическим синдромом, а также общей реакцией организма на неоплазму.
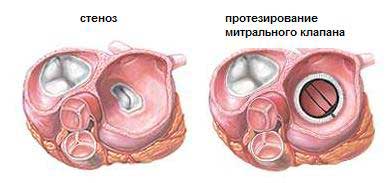
К основным проявлениям данной опухоли относятся симптомы стеноза митрального клапана и тромбоза сосудов большого круга кровообращения, вызванные отрывом частичек опухоли. Наиболее часто наблюдаются симптомы стеноза митрального клапана с развитием легочной гипертензии и выраженной сердечной недостаточности. Реже наблюдается недостаточность митрального клапана, обусловленная пролабированием опухоли или ее прорастанием, с поражением клапанного кольца либо створок клапана. Характерными признаками миксомы являются рецидивирующие приступы потери сознания в результате блокирования опухолью отверстия митрального клапана либо, при более редкой правопредсердной локализации, блокирования опухолью отверстия трехстворчатого клапана. Тромбозы легочных или системных сосудов, связанные с отрывом фрагментов опухоли, наблюдаются более чем у 50% детей с миксомой сердца. Разнообразные паранеопластические проявления, описанные при злокачественных опухолях, также могут наблюдаться при миксомах сердца, нередко маскируя сердечную симптоматику.
Диагностика
Клиническая диагностика опухолей сердца у детей чрезвычайно трудна в связи с отсутствием патогномоничных признаков заболевания и невозможностью ребенка объективно оценить свое состояние. Настороженность в отношении развития опухолевого процесса сердца у ребенка должна присутствовать при наличии сердечных шумов неясной этиологии с развитием застойной сердечной недостаточности, нарушениями ритма — от АV-блокады разной степени до не поддающихся медикаментозному лечению приступов тахикардии, сопровождающихся лихорадкой, анемией и беспричинной потерей массы тела. Заподозрить наличие опухолевого процесса в сердце возможно при сочетании заболевания сердца и эмболии периферических артерий. Основными диагностическими методами исследования являются расширенный биохимический анализ крови и кардиологическое исследование, позволяющее визуализировать функцию сердца.
Клиническая картина злокачественного процесса характеризуется неожиданным появлением определенных симптомов с быстро прогрессирующей сердечной недостаточностью и увеличением размеров сердца, гемоперикардом, болями в грудной клетке, аритмиями и внезапной смертью.
При злокачественных новообразованиях небольших размеров механический фактор обструкции атриовентрикулярных отверстий и выводных трактов желудочков отсутствует, а недостаточность кровообращения чаще обусловлена интоксикацией организма ребенка. Декомпенсация кровообращения может быть обусловлена частичным замещением контрактильного миокарда опухолевой тканью или хронической тампонадой. В этих случаях с уверенностью можно говорить о злокачественном росте, особенно если при пункции полости перикарда получено геморрагическое содержимое и определяется наличие атипичных клеток в пунктате. По данным ряда авторов, гемоперикард наблюдается в 40-50% всех случаев злокачественных неоплазм сердца.
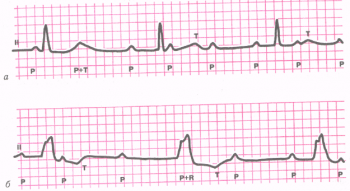
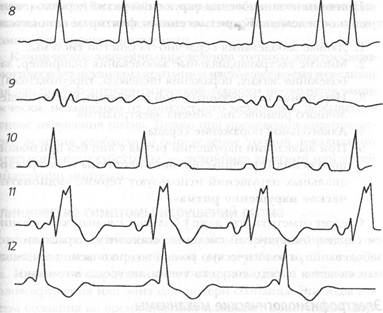
Изменения на ЭКГ могут быть неспецифическими либо совсем отсутствовать. При внутриполостных опухолях регистрируются гипертрофия левых или правых отделов сердца, что зависит от локализации и размеров новообразования, предопределяющих гемодинамические нарушения, а также суправентрикулярные или желудочковые нарушения ритма. У больных с внутримышечными опухолями сердца описывают укорочение интервала P-R, отстроченную реполяризацию правого желудочка, блокаду правого или левого пучка Гиса, полную AV-блокаду. Также могут наблюдаться рецидивирующие приступы мерцательной аритмии. Кроме того, при злокачественных новообразованиях возможна регистрация низкого вольтажа комплексов QRS и неспецифические изменения сегмента ST и зубца Т. При подозрении на рецидив рабдомиомы после ее радикального удаления хирургическим путем даже при локализации опухоли вне сердца и полости грудной клетки помимо обзорной рентгенограммы показано рутинное ЭКГ-исследование.
Рентгенологическое исследование больных с первичными опухолями сердца позволяет выявить многообразные признаки, присущие этому заболеванию. Однако они также не патогномоничны, так как в большинстве случаев отражают только гемодинамические изменения, наступающие, как правило, при новообразованиях больших размеров, а при злокачественных формах могут дополняться признаками изолированного экссудативного перикардита. Несимметричное увеличение тени сердца может определяться при локализации опухоли в области переднебоковой стенки левого желудочка. Выявление на рентгенограмме изолированного образования, выходящего за пределы границ сердца, также может свидетельствовать в пользу опухолевого процесса эпикардиально-перикардиальной локализации. Спорадически может отмечаться кальцификация опухоли. Пристального внимания заслуживает неодинаковая выраженность застойных явлений в легких, которая в сочетании с соответствующей клинической симптоматикой может способствовать косвенному обнаружению внутриполостных новообразований сердца. В то же время деформация контуров сердца с уменьшением амплитуды зубцов на рентгенокимограммах в сочетании с «застывшими» очаговыми инфарктоподобными изменениями на ЭКГ при отсутствии ишемической болезни сердца в анамнезе может свидетельствовать о наличии внутримышечной опухоли в сердце.
Эхокардиография является высокоэффективным неинвазивным методом исследования при опухолях сердца у детей. Она позволяет уже в поликлиническом подразделении поставить правильный диагноз и выработать оптимальную хирургическую тактику. Современное развитие эхокардиографии позволяет установить точные размеры опухоли, ее локализацию, подвижность и связь с другими анатомическими структурами сердца. Наблюдения показывают, что при внутриполостной локализации сердечных новообразований разрешающая способность этого метода исследования с применением В-режима приближается к 100%. ЭхоКГ позволяет установить детали анатомического строения опухоли и определить возможные нарушения внутрисердечной гемодинамики. Обладая высокой разрешающей способностью, этот метод достаточно точно определяет локализацию, размеры, инвазивный характер роста новообразования при таких опухолях, как рабдомиомы и фибромы сердца, а также функциональное состояние клапанного аппарата и сократительную способность миокарда. При ЭхоКГ с успехом выявляются такие важные отличительные особенности злокачественных новообразований, как малоподвижность опухоли, тесная взаимосвязь с сердечными структурами, отсутствие ножки опухоли, атипичное расположение и др. Используемая все чаще ЭхоКГ плода позволяет проводить раннюю диагностику новообразования во внутриутробном периоде.
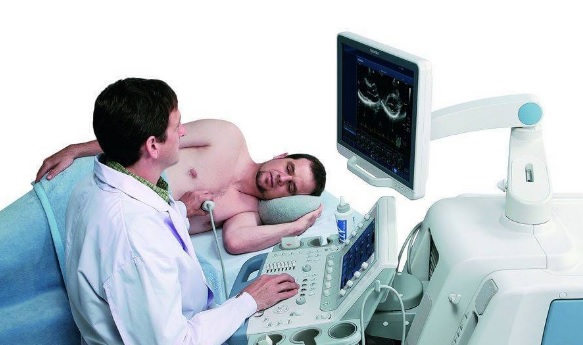
Компьютерная томография и МРТ показаны в случае распространения опухолевого процесса на структуры средостения. Анализ данных этих методов исследования позволяет определить место фиксации опухоли, провести дифференциальный диагноз между новообразованиями из жировой или солидной ткани, кистами, а при распространении патологического процесса на близлежащие органы и ткани сделать заключение о злокачественности процесса.
Ангиографическое исследование позволяет зарегистрировать особенности гемодинамических нарушений, обусловленные препятствием на путях притока и/или оттока крови из пораженных камер сердца, определить локализацию опухоли, ее размер и подвижность, распространение на коронарные сосуды. Это особенно важно при принятии решения об оперативном лечении, а также определении техники операции. Селективная коронарография дополняет эту информацию за счет выявления сосудистой сети новообразования, а эндомиокардиальная биопсия, проводимая при подозрении на злокачественный характер заболевания, подтверждает или отвергает этот диагноз. Однако проведение исследования при внутриполостных новообразованиях сопряжено с опасностью их фрагментации и последующей опухолевой эмболии, поэтому в настоящее время большинство клиницистов воздерживаются от зондирования камер сердца и перечисленного комплекса диагностических манипуляций, отдавая предпочтение неинвазивным методам исследования — ЭхоКГ, КТ и МРТ.
Лечение и его результаты
В настоящее время не вызывает сомнения тот факт, что радикальное хирургическое лечение при эндо- и миокардиальных опухолях возможно только под непосредственным контролем зрения.
Оперативное лечение, направленное на обширную резекцию опухоли в условиях искусственного кровообращения, является методом выбора при доброкачественных опухолях сердца, вызывающих значительное нарушение гемодинамики. Вероятность окклюзии клапанных отверстий и возможность фрагментации опухолей с возникновением эмболических осложнений свидетельствуют об экстренности оперативного вмешательства. Удаление новообразований сердца может сопровождаться значительной травмой структур сердца. Для замещения резецированных участков используют заплаты из аутоперикарда, гомографт или синтетический материал. Послеоперационное ведение больных не отличается от типичного для кардиохирургических операций, за исключением продленной инфузии катехоламинов для поддержания гемодинамики на должном уровне. В послеоперационном периоде доброкачественные опухоли не требуют проведения химио- и рентгенотерапии.

Обширное поражение миокарда в случае далеко зашедшего процесса при фиброме, липоме или рабдомиоме не позволяет провести радикальную резекцию опухоли. Более того, радикальное удаление этих новообразований сердца в большинстве случаев является неоправданной и даже калечащей операцией. В связи с этим хирургические вмешательства при интрамуральных опухолях должны выполняться исключительно при их симптоматических формах, иметь паллиативный характер и ограничиваться удалением только той части новообразования, которая приводит к стенозированию или окклюзии приточного или выводного отделов пораженных камер сердца. Теоретической предпосылкой к выполнению подобных операций при рабдомиоме служит морфологический характер опухоли, которая представляет собой доброкачественное новообразование, отличающееся незначительным потенциальным ростом, а в некоторых наблюдениях — медленной спонтанной регрессией, наступающей с возрастом. В отдельных случаях выбор хирургического вмешательства следует проводить между частичной резекцией опухоли и пересадкой сердца. В исключительных случаях, при труднодоступном расположении опухоли, показана аутотрансплантация сердца после резекции опухоли.
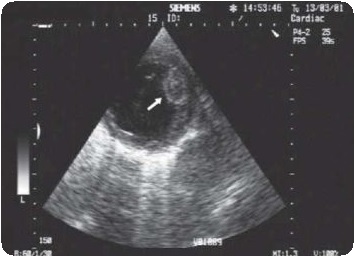
Хирургическая резекция миксомы должна обязательно сопровождаться дополнительной резекцией фрагмента миокарда в области ножки опухоли, чаще всего это участок межпредсердной перегородки. Считается, что замещение резецируемого участка заплатой из аутоперикарда или проведение электрокоагуляции экстрасептального участка, являющегося основанием ножки опухоли, препятствует ее рецидиву. Однако, несмотря на проведение подобных мероприятий, данная опухоль довольно часто рецидивирует. Одним из важных принципов успешного удаления миксом является комплекс мероприятий, направленных на профилактику фрагментации опухоли и последующей эмболии. Для этого все манипуляции, связанные с подключением аппарата искусственного кровообращения, должны быть максимально щадящими. Если канюляция полых вен при опухолях левых отделов сердца не представляет особых трудностей, то при опухолях правого предсердия может возникнуть необходимость ретроградной канюляции нижней полой вены через общую бедренную вену, а верхней полой вены непосредственно через ее устье. Кроме того, хирурги стремятся удалять новообразование без его фрагментации, а после окончания данного этапа операции обязательны ревизия и промывание всех полостей сердца. Соблюдение этих принципов позволяет полностью избежать опухолевой эмболии. Необходимо точно определить степень поражения AV-клапанов, особенно митрального клапана, который может разрушаться вследствие механического воздействия опухоли. В этом случае необходима пластика клапана либо, при значительном повреждении структуры створки, его протезирование. Во время операции показана рутинная ревизия всех полостей сердца в целях выявления дополнительных очагов поражения. При этой операции крайне полезным является проведение интраоперационной чреспищеводной эхокардиографии для установления радикальности резекции опухоли, а также функции АV-клапанов.
Прогноз
Злокачественные опухоли сердца, учитывая их быстрый рост, системное метастазирование и отсутствие удовлетворительного результата независимо от проводимой терапии, характеризуются плохим прогнозом. До настоящего времени не разработан общепринятый алгоритм терапии, в том числе и в отношении хирургического вмешательства. У данной категории больных выполняют паллиативные кардиохирургические вмешательства, направленные на снижение интенсивности проявления процесса и повышение качества жизни пациента. Операции по удалению злокачественной опухоли сердца технически крайне сложны и сопряжены с высоким риском. Основной опасностью является обнаружение распада опухоли, захватывающей все органы средостения, с развитием не поддающихся остановке кровотечений.
В связи с этим может возникнуть необходимость подключения аппарата искусственного кровообращения доступом через бедренные сосуды, а также полная остановка кровообращения на фоне глубокой гипотермии.
Радикальное удаление опухоли в пределах здоровых тканей сопряжено с массивной резекцией стенок сердца, травмой коронарных сосудов, последующим их замещением синтетическим или биологическим материалом, протезированием клапанов, аортокоронарным шунтированием и при необходимости имплантацией кардиостимулятора, что обусловливает высокую госпитальную летальность. Важно также отметить, что отсутствие метастазов или прорастания близлежащих органов и тканей принципиально не улучшает результаты хирургического лечения. Это связано со значительным распространением опухолевою процесса в пределах миокарда и необходимостью проведения операции большого объема. В послеоперационном периоде, учитывая массивную резекцию миокарда, требуется длительная инфузия катехоламинов. Помимо этого, могут отмечаться угрожающие жизни пациента нарушения ритма сердца.
Наряду с хирургическим вмешательством, для комплексного лечения злокачественных опухолей сердца у детей также используют химио-, лучевую терапию и методы иммунотерапии, что позволяет добиться существенного улучшения результатов у многих больных, особенно при опухолях, чувствительных к химиопрепаратам. Последовательность лечебных мер зависит от вида и особенностей новообразования. В большинстве случаев лекарственные препараты применяют у больных после радикальной операции удаления новообразования для уничтожения оставшихся клеток, профилактики метастазов и рецидива неоплазмы. Такую химиотерапию называют вспомогательной. Её проводят повторными курсами в течение продолжительного времени, как правило, 1 года-2 лет после операции.
При рабдомиосаркрме чаще всего используют винкристин, актиномицин D, циклофосфамид или сарколизин, адриамицин и другие препараты. При злокачественных опухолях мышечной ткани другой этиологии химиотерапия проводится в связи с высокой частотой метастазирования этих новообразований и отсутствием результатов при использовании местных методов лечения. Для лечения этой группы новообразований чаще всего используют циклофосфамид, винкристин и адриамицин.
Радиотерапия применяется в зависимости от каждого конкретного случая и заключается в паллиативном облучении первичного очага и метастазов. Этот метод чаще используют у тех пациентов, у которых оперативное вмешательство невыполнимо или влечет за собой значительное нарушение функции органов. Следует отметить, что многие химиопрепараты обладают синхронизирующим действием, повышая при этом радиочувствительность злокачественных клеток. Такое взаимодействие двух направлений подчеркивает большую значимость комбинированной противоопухолевой терапии.
Основными причинами неудовлетворительных результатов хирургического лечения больных с первичными опухолями сердца являются распространенность опухоли, а также метастазирование и рецидивирование опухолевого процесса. В связи с этим усилия клиницистов необходимо направить на более раннюю диагностику заболевания и безотлагательное проведение операции. Часто единственной надеждой у этой категории больных является ранняя пересадка сердца.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания










Комментарии