Транспозиция магистральных сосудов: операция, этапы, последствия
Ранние попытки хирургического лечения порока предпринимались в середине 1950-х годов. Они были прообразом современной анатомической коррекции — пересечения и реанастомозирования магистральных артерий с перемещением коронарных артерий. Все эти попытки были неудачны, так как большинство детей с интактными межжелудочковой и межпредсердной перегородками после закрытия боталлова протока находились в крайне тяжелом состоянии. В целях повышения оксигенации артериальной крови Blalock и Hanlon в 1950 г. предложили метод создания сообщения между системным и легочным кругами кровообращения на предсердном уровне. Эта операция решала только краткосрочные задачи, так как быстрое снижение давления в левом желудочке приводило к потере его способности нести нагрузку под системным давлением. Кроме того, в те годы еще не было необходимой перфузиологической техники и микрососудистого инструментария для выполнения анатомической коррекции.
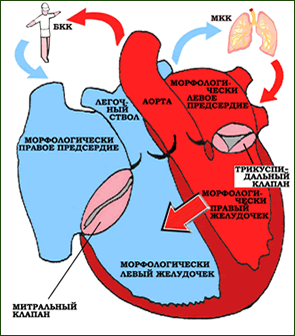
В конце 1960-х годов, когда начала развиваться хирургия коронарных артерий, была разработана техника микрососудистых анастомозов. Она стимулировала прогресс в хирургическом лечении ВПС у новорожденных. К началу 1970-х годов Barratt-Boyes в Новой Зеландии и Castaneda и соавторы в США первыми показали возможность первичной коррекции большинства ВПС в младенческом возрасте с достаточно низкой летальностью, компенсируя несовершенство искусственного кровообращения применением гипотермической остановки кровообращения.
К этому времени огромный вклад в лечение ТМА внесли Rashkind и Miller, которые внедрили метод баллонной атриосептостомии. Эта процедура как часть диагностической катетеризации сердца имела принципиальные преимущества перед операцией Blalock-Hanlon, такие, как безопасность, отсутствие сращений.
Первые успешные операции полной гемодинамической коррекции кровообращения при ТМА были описаны Senning и Mustard на основе первоначальной идеи Albert о возможности внутрипредсердного перемещения потоков артериальной и венозной крови с помощью заплаты при анатомически некорригированной морфологии порока. В конце 1970-х годов Brom возродил угасший интерес к операции Senning и вместе с соавторами Quaegebeur и Rohmer представил отличные непосредственные результаты этой операции. Trusler и соавторы в Торонто, где в свое время Mustard разработал свою операцию, продемонстрировали низкую госпитальную летальность при этом варианте гемодинамической коррекции.
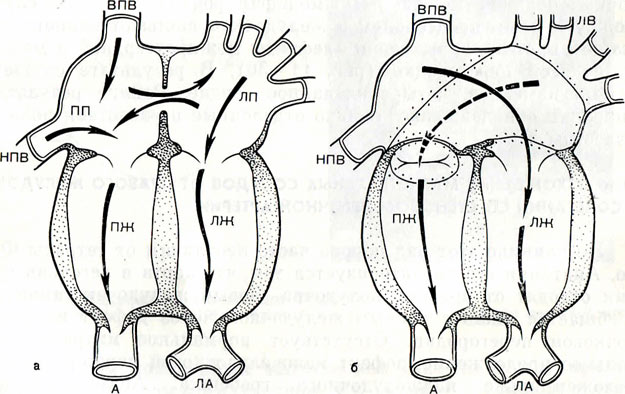
В тот же период активного поиска методов хирургического лечения сложных ВПС Jatene и соавторы в Бразилии показали осуществимость анатомической коррекции ТМА. Она была выполнена у ребенка, который оставался клинически благополучным после неонатального периода благодаря наличию ДМЖП, поддерживающего высокое давление в левом желудочке, что позволило ему справиться с системной нагрузкой. Yacoub и соавторы в Великобритании адаптировали операцию артериального переключения к больным с ТМА и ИМЖП. Они предложили двухэтапное лечение. Первое вмешательство предполагало суживание легочной артерии с целью подготовки левого желудочка к предстоящей системной нагрузке. Корригирующую порок операцию выполняли через 1 год после первого этапа. На основе экспериментальных данных о быстрой адаптации левого желудочка к острой нагрузке давлением и эхокардиографических исследований в клинике Jonas и соавторы внедрили операцию «быстрого» двухэтапного артериального переключения: суживание легочного ствола, дополненное системно-легочным анастомозом, и через 7-10 дней — артериальное переключение. В эти сроки не развиваются сращения, которые резко усложняют повторные операции.
Важнейший вклад в утверждение анатомической коррекции ТМА в качестве операции выбора внесли Castaneda и соавторы. Они предложили выполнять первичные операции артериального переключения в неонатальном периоде у детей с ИМЖП, что исключает необходимость специальной подготовки левого желудочка. Предпосылкой успеха этой тактики является то, что левый желудочек у плода нагнетает кровь под системным давлением благодаря функционированию ОАП.
В 1981 г. Lecompte и соавторы внесли существенное дополнение в технику операции артериального переключения — перемещение дистальной легочной артерии кпереди от восходящей аорты, таким образом, облегчая выполнение прямого анастомоза неолегочной артерии без использования кондуита.
На начальном этапе применения операции артериального переключения Castaneda и соавторы считали, что существует несколько редких вариантов отхождения и ветвления коронарных артерий, при которых успешная транслокация их в неоаорту невозможна и этому контингенту больных следует предлагать операцию Senning. Однако Yacoub и соавторы уже в то время утверждали, что все варианты коронарных артерий могут быть перемещены, и время доказало правильность этой позиции. Тем не менее, следует отметить, что некоторые редкие варианты коронарных артерий, в частности отхождение обеих главных коронарных артерий от одного синуса, создают значительные технические трудности.
В истории лечения ТМА были предложены альтернативные методы операций с целью избежать трудности перемещения коронарных артерий. Некоторые из них не утратили своего значения и по определенным показаниям применяются по сей день при коррекции не только ТМА. Независимо друг от друга Damus, Kaye и Stansel разработали операцию, предусматривающую анастомозирование «конец в бок» проксимального конца легочного ствола с восходящей аортой и имплантацию кондуита между правым желудочком и дистальной легочной артерией.
Предоперацоннная стабилизация
На дохирургическом этапе необходимо выполнить следующие лечебно-диагностические мероприятия:
1. Получить данные о насыщении артериальной крови кислородом и ее рН, провести кислородную пробу, чтобы подтвердить наличие циано- тического ВПС.
2. Провести коррекцию метаболического ацидоза, гипогликемии и гипокальциемии.
3. Начить инфузию простагландина E1 для улучшения насыщения артериальной крови кислородом путем поддержания проходимости ОАП. Она должна быть продолжена во время катетеризации вплоть до операции. Инфузия простагландина является лишь кратковременной альтернативой процедуре Rashkind. Утечка крови из системного круга кровообращения в легочный через ОАП приводит к феномену «обкрадывания», в частности, органов брюшной полости. Это может быть чревато развитием некротического энтероколита. Если нет достаточного по объему двунаправленного шунтирования через проток, сброс крови слева направо увеличивает легочный артериальный и венозный застой и левопредсердную гипертензию. После баллонной атриосептостомии создаются идеальные условия для декомпрессии левого предсердия через созданный дефект и восполнения объема крови в системном круге.
4. При тяжелой гипоксии проводить ингаляцию кислорода для снижения ЛСС и увеличения объема легочного кровотока, что может повысить сатурацию артериальной крови. Оперативному вмешательству обычно предшествуют катетеризация сердца и баллонная атриосептостомия. У больных без дефектов межжелудочковой и межпредсердной перегородок баллонная атриосептостомия должна быть выполнена сразу после их поступления в кардиохирургический центр. Повышение артериального насыщения дает свободу выбора срока операции в пределах 1-3 нед. после рождения. В случаях, когда у больного имеется достаточных размеров ДМПП, коррекция порока может быть выполнена без предшествующей катетеризации и атриосептостомии.
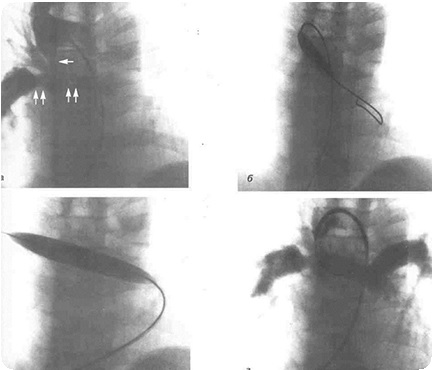
Операцию Rashkind производят следующим образом. Катетер с баллончиком на конце проводят в левое предсердие через открытое овальное окно. Баллон раздувают жидким рентгеноконтрастным веществом и резко продергивают в правое предсердие под рентген- или эхоскопическим контролем. Через образовавшееся межпредсердное сообщение увеличивается объем смешиваемой крови более чем на 10%. Минимальный межпредсердный градиент давления оценивается как удовлетворительный результат процедуры.
У детей более старшего возраста межпредсердная перегородка более прочна и не разрывается при попытке баллонной септостомии. В этих случаях применяется ножевая техника по Парку. С помощью встроенного на конце катетера лезвия рассекают перегородку и затем выполняют баллонную дилатацию.
Хирургическое лечение
При неудачных попытках катетерного разрушения межпредсердной перегородки выполняют операцию Hanlon-Blalock — хирургическое иссечение задней части межпредсердной перегородки без искусственного кровообращения.
Операция Hanlon-Blalock и открытая септэктомия с искусственным кровообращением создают лучшие условия для перемешивания крови и более высокое насыщение артериальной крови кислородом, чем баллонная септостомия, и этот эффект сохраняется более продолжительное время. В ранних сериях операций летальность превышала 30%. В последующем ее удалось снизить до 1,4%. В настоящее время к этому вмешательству прибегают редко из-за достаточно высокой эффективности катетерных методов атриосептостомии. Однако эта операция остается в арсенале закрытых методов лечения и применяется, когда жесткость перегородки не позволяет выполнить катетерные вмешательства.
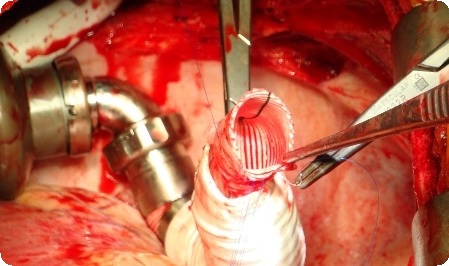
В течение нескольких дней после атриосептостомии состояние новорожденного стабилизируется после родовой травмы, гипоксии и ацидоза, связанных с закрытием ОАП. Важно оценить состояние почек, печени, кишечника и мозга. К моменту операции все системы органов должны функционировать нормально. В интубации и искусственной вентиляции нет необходимости. Однако если нет адекватного перемешивания крови на предсердном уровне после септостомии, следует возобновить инфузию простагландина и интубация в этих условиях может оказаться полезной в качестве меры предосторожности от возможных эпизодов апноэ. Нет необходимости также в постоянном артериальном катетере, так как насыщение кислородом может адекватно мониторироваться пульсоксиметром. Тем не менее, перед доставкой больного в операционную целесообразно для экономии времени катетеризировать артерию и вену.
Коррекция гемодинамики направлена на перемещение артериальной крови в большой круг кровообращения, а венозной — в малый на одном из трех уровней:
-
предсердном;
-
желудочковом;
-
артериальном.
Выбор типа операции и сроков ее выполнения определяется наличием или отсутствием сопутствующих пороков сердца, неблагоприятной анатомии коронарных артерий, временем направления на хирургическое лечение. Вне зависимости от планирования операции артериального или венозного переключения больным обязательно производят баллонную атриосептостомию.
Хирургическое лечение простой транспозиции
Физиологическая коррекция
На предсердном уровне осуществляют перераспределение потоков крови, используя один из двух вариантов — операцию Senning или операцию Mustard. Легочный и системный венозный возврат перенаправляют с помощью перикардиальной заплаты или с использованием тканей предсердий в противоположные желудочки, таким образом, искусственно создавая предсердно-желудочковые дискордантные отношения.
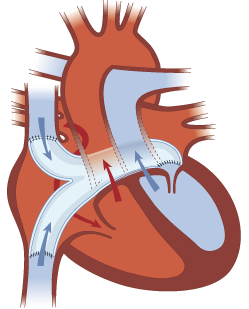
Операции Mustard и Senning в определенной степени являются паллиативными, так как устраняют лишь гемодинамические, а не анатомические нарушения. Правый желудочек продолжает функционировать как системный, а левый — как легочный. Внутрипредсердные пути имеют неестественную конфигурацию. С этим связаны осложнения раннего и отдаленного послеоперационного периодов:
-
обструкция легочного и системного венозного возврата;
-
остаточный шунт на предсердном уровне;
-
недостаточность трехстворчатого клапана в отдаленные сроки после операции;
-
отсутствие синусового ритма и частая суправентрикулярная аритмия;
-
сниженная толерантность правого желудочка к физической нагрузке;
-
внезапная смерть, обусловленная нарушением ритма;
-
обструктивная болезнь легочных сосудов.
Перечисленные осложнения в большей степени характерны для операции Mustard.
Операция Mustard может быть выполнена в любом возрасте, если больной нуждается в неотложном дальнейшем лечении после баллонной атриосептостомии. Однако до 3 мес. летальность выше и осложнения встречаются чаще. Оптимальным сроком операции является возраст 6-12 мес. Операция может быть выполнена при сопутствующем ДМЖП со СЛА или с легочной гипертензией.
Операцию выполняют в условиях искусственного кровообращения и поверхностной или глубокой гипотермии. Верхнюю полую вену канюлируют через ее стенку, а нижнюю полую вену — в месте ее соединения с правым предсердием изогнутыми под прямым углом канюлями. Выполняют продольную атриотомию. Заплату выкраивают из аутоперикарда по предложению Brom в виде брюк. Размер «штанин» по краям, прилежащим к полым венам, должен быть равен 3/4 окружности соответствующей вены. Межпердсердную перегородку иссекают, создавая общее предсердие. Коронарный синус рассекают кзади в левое предсердие для того, чтобы он продолжал дренироваться в системное венозное предсердие и чтобы увеличить межпредсердное сообщение. Обнаженные края иссеченной перегородки обшивают для соединения листков эндокарда и улучшения заживления без сращений и чрезмерного рубцевания. Далее производят атриосептопластику: заплату подшивают вначале к переднему краю левых легочных вен, затем линию шва проводят по задней стенке левого предсердия, вдоль верхнего и нижнего краев легочных вен, достигая стенки правого предсердия у отверстий верхней и нижней полых вен. «Штанины брюк» подшивают тем же непрерывным швом к передней полуокружности полых вен и слева от коронарного синуса к остаткам межпредсердной перегородки. При левой юкстапозиции правого ушка и других редких случаях малого правого предсердия необходимо его увеличить лоскутом перикардиальной заплаты.
В результате реконструкции межпредсердной перегородки кровь из легочных вен и коронарного синуса дренируется через трехстворчатый клапан в правый желудочек, а кровь из полых вен — через митральный клапан в левый желудочек, т.е. полная ТМА переводится в корригированную. Попутно закрывают ДМЖП и устраняют стеноз легочной артерии.
В настоящее время операцию Mustard выполняют редко, главным образом у детей не младше 4-5 лет, из-за возможного нарушения оттока крови из легочных и системных вен. Эта операция вновь появилась в арсенале современной кардиохирургии в связи с внедрением двойного переключения на артериальном и предсердном уровнях при корригированной ТМА.
-
Операция Senning.
Главное преимущество этой операции состоит в том, что при меньшей частоте осложнений в отдаленном периоде по сравнению с операцией Mustard и при отсутствии ограниченных неонатальным периодом сроков вмешательства, как при операции артериального переключения, она может быть выполнена в любом возрасте. Противопоказанием к выполнению стандартной операции Senning является левосторонняя юкстапозиция ушек предсердий и декстроверсия.
Обычно операцию выполняют в возрасте 5-6 мес в условиях умеренной гипотермии без остановки искусственного кровообращения, используя канюляцию обеих полых вен непосредственно через их переднюю стенку. При наличии ДМЖП и других сопутствующих аномалий они устраняются в начале операции. Перед началом искусственного кровообращения измеряют окружность полых вен, что необходимо для определения ширины передней стенки канала полых вен. Накладывают маркировочные швы по верхнему и нижнему краям межпредсердной борозды, расстояние между которыми определяет длину будущего разреза левого предсердия.
Маркировочным швом также помечают нижнюю точку будущего разреза правого предсердия. Расстояние между нижними концами разрезов левого и правого предсердий должно быть равно 2/3 окружности нижней полой вены. После начала перфузии и охлаждения до 24 °С распрепаровывают межпредсердную борозду и делают в ней короткий разрез для дренажа левого предсердия. Верхняя точка разреза стенки правого предсердия должна быть примерно на 1 см кпереди от crista terminalis. Между подготовленными ориентирами выполняют атриотомию. Остатков межпредсердной перегородки после баллонной атриосептостомии обычно недостаточно для формирования передней стенки легочно-венозного канала. Этот дефект перегородки восполняют лоскутом аутоперикарда. Иссекают «полу» межпредсердной перегородки трапециевидной формы в основном за счет лимбической ткани. Разрез проводят до верхнего и нижнего края правых легочных вен. Отсеченная «пола», частично сформированная из ранее пришитого лоскута перикарда, остается прикрепленной в области межпредсердной борозды.
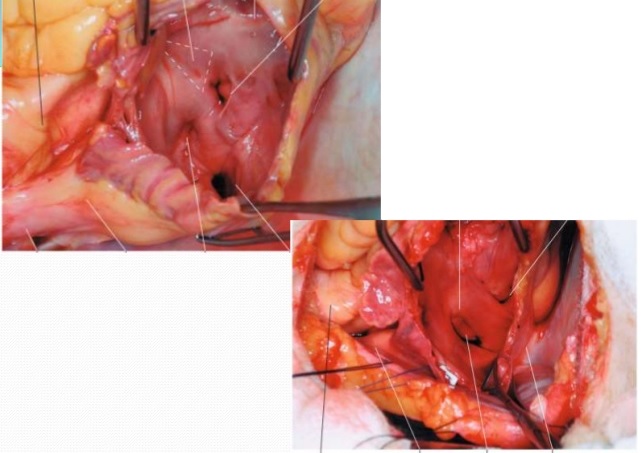
Для создания передней стенки легочно-венозного канала в целях минимального использования неживого материала формируют дополнительную полу путем рассечения общей с левым предсердием стенки коронарного синуса. Образовавшуюся «полу» из стенки коронарного синуса удлиняют путем собирания в складку задней стенки левого предсердия на участке между устьями левых легочных вен и отверстием левого ушка. В результате образуется некий навес, к которому непрерывным швом фиксируют вершину полы, сформированной из межпредсердной перегородки. Шов продолжают в обе стороны по задней стенке левого предсердия до устьев правых легочных вен у основания «полы».
Разрез левого предсердия продлевают до его максимальной длины между маркировочными швами. Канал системных вен образуют, используя латеральную стенку правого предсердия между разрезами правого и левого предсердий. Латеральный край разреза стенки правого предсердия пришивают двумя непрерывными швами вокруг устьев верхней и нижней полых вен, далее к остатку межпредсердной перегородки, где оба шва встречаются в ее центре. Коронарный синус остается во вновь создаваемом левом предсердии.
После создания путей притока по полым венам конструируют легочно-венозный путь. Для увеличения полезной площади сечения отверстия в левом предсердии производят надрез правой верхней легочной вены на глубину до 1 см. В некоторых случаях удается пришить край оставшейся медиальной «полы» правого предсердия вокруг верхней и нижней полых вен к свободному краю разреза левого предсердия. Однако если есть сомнения относительно чрезмерного натяжения стенки правого предсердия и обструкции легочного венозного или системного венозного пути, можно расширить стенку предсердия свободным лоскутом перикарда или, что более предпочтительно, использовать его in situ. Фиксацию перикарда начинают в переходной складке в месте соединения верхней полой вены с правым предсердием у головного конца разреза левого предсердия. Линия шва проходит по верхней полой вене и стенке правого предсердия. Делают поверхностные стежки для избежания повреждения синусового узла. Аналогично фиксируют перикард к месту впадения нижней полой вены и к стенке правого предсердия. Конструирование легочного венозного пути завершают, сшивая свободный край перикарда с краем медиальной «полы» стенки правого предсердия.
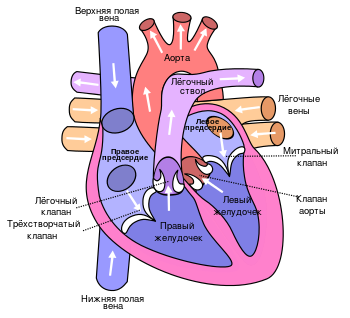
Анатомическая коррекция
-
Артериальное переключение.
Преимущества операции артериального переключения. Простая логика и многочисленные исследования убеждают, что левый желудочек более приспособлен для системной гидродинамической нагрузки, чем правый. Этому способствуют анатомические особенности строения левого желудочка — насоса, идеально адаптированного к работе под давлением:
-
цилиндрическая форма;
-
малый диаметр полости, оптимизирующий постнагрузку;
-
концентрическое сокращение;
-
расположение входного и выпускного клапанов в непосредственной близости.
Правый желудочек с его серповидной формой полости с большой площадью внутренней поверхности, с отличным от левого желудочка типом сокращения, напоминающим меха, и удаленными друг от друга приточным и выпускным отделами является насосной камерой, приспособленной выполнять объемную нагрузку под низким давлением. Кроме того, левый желудочек кровоснабжается двумя артериями, а правый — только одной. Левый желудочек имеет больший объем сократительной массы, так как филогенетически левожелудочковый синус развивается из примитивного желудочка на стадии образования петли сердечной трубки, а конус и большая часть правого желудочка происходят от бульбуса сердца. Множественные и малые папиллярные мышцы правого желудочка прикрепляются к перегородке и передней свободной стенке желудочка, в отличие от левого желудочка, имеющего две мощные папиллярные мышцы, поэтому при дилатации правого желудочка створки трехстворчатого клапана растягиваются в разные стороны, вызывая регургитацию. Операция Jatene подключает левый желудочек в качестве системного насоса и воссоздает нормальные анатомические и гемодинамические характеристики.
Показания к операции артериального переключения
Операция Jatene применяется не только при простой d-ТМА, но и при:
-
d-ТМА с ДМЖП;
-
отхождении магистральных сосудов от правого желудочка с подлегочным ДМЖП;
-
сочетании ТМА с коарктацией аорты или перерывом дуги аорты и обструкцией выводного тракта правого желудочка;
-
двуприточном единственном желудочке сердца левого типа с ТМА, тяжелым субаортальным стенозом, коарктацией, гипоплазией или перерывом дуги аорты и дуктусзависимым системным кровотоком у новорожденных. При данном сочетании артериальное переключение производится с целью обхода субаортального стеноза путем создания выхода в аорту через легочный ствол — неоаорту. Вскоре после операции может потребоваться системно-легочный анастомоз в результате прогрессирования подлегочного стеноза;
-
дисфункции правого желудочка с недостаточностью трехстворчатого клапана после операции предсердного переключения. Эти вмешательства выполняют в два этапа, первый из которых — суживание легочной артерии. Тренировка левого желудочка у больных старшего возраста требует более продолжительного времени и эффект его менее предсказуем, чем у быстро растущих новорожденных и грудных детей. Ухудшение функции левого желудочка и недостаточность митрального клапана являются относительным противопоказанием к двухэтапной конверсии в артериальное переключение. В этих случаях показана трансплантация сердца;
-
прогрессирующей динамической обструкции левого желудочка после гемодинамических операций на предсердном уровне. Теоретически эта проблема решается одноэтапной конверсией в артериальное переключение. Однако вследствие воздействия струи крови стенка легочного ствола истончена, что усложняет гемостаз;
-
врожденной корригированной транспозиции с ДМЖП и увеличенным легочным кровотоком.
В последнее время при благоприятных анатомических и гемодинамических условиях выполняют двойное переключение — на артериальном и предсердном уровне.
Сроки выполнения операции
Операцию выполняют в неонатальном периоде, пока левый желудочек еще не утратил способности осуществлять системное кровообращение, как во внутриутробном периоде. Инволюция левого желудочка может отсрочиться благодаря персистированию большого ОАП или наличию динамической обструкции выводного тракта левого желудочка. При эхокардиографическом исследовании динамическое сужение выводного тракта левого желудочка можно отличить от анатомического по выбуханию межжелудочковой перегородки влево при отсутствии утолщения эндокарда, гребня и узелков. Безопасный период можно на какое-то время удлинить инфузией ПГЕ1, если есть необходимость отсрочить операцию. Идеальное время операции — первые недели жизни. Позднее этого срока левый желудочек не может преодолевать сопротивление большого круга кровообращения. Не существует надежных критериев утраты левым желудочком способности осуществлять системный кровоток. Нельзя отнести к ним даже прямое измерение давления в левом желудочке или определение градиента давления между желудочками. Например, при быстром закрытии ОАП и быстром снижении ЛСС давление в левом желудочке может упасть ниже системного уровня уже на 4-5-й день после рождения. Это не значит, что левый желудочек не способен выполнять системную работу, если операция будет сделана в это время. Однако если низкое давление будет держаться несколько недель, левый желудочек, скорее всего, станет непригодным для артериального переключения. Чем дольше функционирует ОАП, тем больше шансов, что желудочек не утратил своей исходной мощности в 3-4-недельном возрасте.
Обычно пользуются эмпирическими, весьма относительными критериями для предсказания послеоперационной работоспособности левого желудочка. Операция не противопоказана, если давление в левом желудочке не ниже 70% давления в правом желудочке, если масса левого желудочка соответствует норме для данной поверхности тела и если возраст ребенка менее 2 нед. Всем пациентам с d-ТМА и ИМЖП в возрасте до 2 нед. выполняют коррекцию порока вне зависимости от давления в левом желудочке. Информации, полученной при эхокардиографическом исследовании, достаточно для принятия решения об операции. Вне неонатального периода показана катетеризация сердца.
-
Двухэтапная коррекция d-ТМА с интактной межжелудочковой перегородкой.
Существует множество причин отсрочки операции за пределы «безопасного» для артериального переключения периода: некротический энтероколит, почечная и печеночная недостаточность, кровоизлияние в мозг, сепсис, недоношенность с очень малой массой ребенка, географическая удаленность от хирургического центра, ожидаемое спонтанное закрытие ДМЖП, поздняя постановка диагноза. В этих случаях есть выбор между первичной коррекцией гемодинамики на предсердном уровне и двухэтапным анатомическим хирургическим лечением.
В пользу двухэтапного лечения свидетельствуют следующие показатели:
-
возраст старше 1-2 мес;
-
отношение массы левого желудочка к массе правого желудочка < 0,6;
-
давление в левом желудочке < 50 мм рт. ст.
Дополнительными полезными, но не решающими критериями являются эхокардиографические показатели — наличие или отсутствие выбухания межжелудочковой перегородки в полость левого желудочка, толщина стенки, объем желудочка.
Как указывалось выше, было предложено суживание легочной артерии, чтобы увеличить постнагрузку и стимулировать гипертрофию левого желудочка. Примечательно, что первая успешная анатомическая коррекция ТМА с ИМЖП предусматривала на первом этапе суживание легочной артерии в сочетании с наложением системно-легочного анастомоза или без него и через несколько месяцев — дебандаж и артериальное переключение. Впоследствии было показано, что суживание может обеспечить тренированность левого желудочка в течение нескольких дней, так что подготовительная и окончательная операции могут быть выполнены в пределах одной госпитализации. Клиническое течение интервала между операциями характеризуется низким сердечным выбросом из-за сочетания острой объемной перегрузки правого желудочка, обусловленной шунтом, и дисфункцией левого желудочка, связанной с суживанием легочной артерии. Клиническое улучшение происходит на 7-10-й день, когда мощность левого желудочка становится достаточной, чтобы нести системную нагрузку.
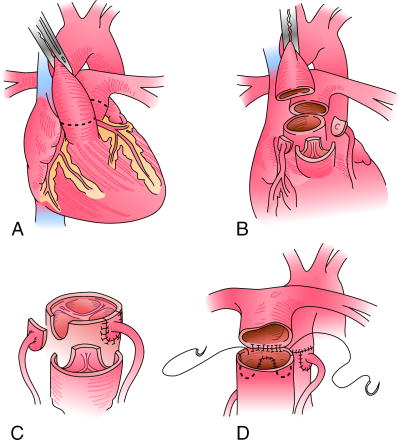
Первый этап производят через правостороннюю торакотомию или срединную стернотомию. Выполняют подключично-легочный анастомоз с помощью сосудистого протеза из GoreTex диаметром 3,5-4 мм, затем суживание легочного ствола под контролем давления в левом желудочке. Давление в его полости должно составлять приблизительно 75% системного.
Если первый этап был выполнен в периоде новорожденности, семи дней достаточно для подготовки левого желудочка к основной операции. Она выполняется в благоприятных условиях отсутствия перикардиальных сращений. Техника операции отличается от стандартной лишь необходимостью пересечения и ушивания анастомоза и дебандажа легочной артерии. Если же суживание легочной артерии произведено в более поздние сроки, необходим более длительный период тренировки левого желудочка и последующая операция может быть отложена на один год, так как исчезает выигрыш от быстрого двухэтапного лечения. В этом случае окончательная коррекция порока сложнее первичной операции из-за трудностей выполнения маневра Lecompte и необходимости иссечения суженного сегмента легочной артерии.
Разработаны и другие методы подготовки левого желудочка к операции артериального переключения: частичная чрескожная баллонная окклюзия легочного ствола, системно-легочный анастомоз без бандажа легочной артерии и первичная операция с параллельным экстракорпоральным артериальным насосом в послеоперационном периоде.
Изучение отдаленных результатов двухэтапного хирургического лечения ТМА обнаружило худшее, чем после первичной коррекции, функциональное состояние левого желудочка, большую частоту регургитации неоаортального клапана и дилатации клапанного кольца.
Методика операции артериального переключения
Особенности проведения искусственного кровообращения и защиты миокарда
Аорту канюлируют непосредственно ниже брахиоцефальной артерии, используя прямую жесткую канюлю. В хирургии ТМА используется как бикавальная канюляция, так и канюляция правого предсердия одним катетером через ушко. Последний метод имеет преимущество, так как одна канюля при наличии межпредсердного сообщения одновременно обеспечивает дренаж левопредсердного возврата. Прямая же канюляция полых вен создает вероятность дисбаланса венозного оттока из верхней и нижней половины тела и отека соответствующей области. После начала перфузии канюлируют нижнюю полую вену и обжимают ее тесьмой. Верхнюю венозную канюлю проводят в верхнюю полую вену.
-
Гематокрит.
Ранее считалось, что гемодилюция является обязательной при гипотермической перфузии и остановке кровообращения. Существует концепция, что повышенная вязкость крови при глубокой гипотермии может привести к ухудшению перфузии тканей. Однако многие исследования показали, что гемодилюция снижает доставку кислорода. Кроме того, снижение онкотического давления приводит к отеку тканей. Разбавление факторов свертывания крови увеличивает послеоперационную кровопотерю и вызывает необходимость увеличения объема переливаемой крови, что также способствует отеку. Поэтому перфузат, включающий кровь и плазморасширители, должен быть в такой пропорции, чтобы концентрация гемоглобина составляла 9 г%, а гематокрит — 25-30%. рН-стратегия обеспечивает снижение частоты осложнений во время операции и в послеоперационном периоде по сравнению с альфа-стат-стратегией. В частности, было показано, что отек мозга после гипотермической остановки кровообращения более выражен при альфа-стат-стратегии, чем при рН-стат-стратегии.
-
Объемная скорость кровотока.
До настоящего времени нет единого протокола по вопросу об оптимальной скорости перфузии при операции артериального переключения. Существуют три предпочтения: полная объемная скорость перфузии с глубокой гипотермией, полная объемная скорость с умеренной гипотермией и даже полная производительность насоса при нормотермической перфузии. Большинство хирургов используют глубокую гипотермию при сниженном объеме перфузии. При полной объемной скорости перфузионное давление у детей массой 3-5 кг должно быть в пределах 35-45 мм рт.ст. При ИМЖП применяют короткий период полной остановки кровообращения для закрытия ДМПП. При наличии ДМЖП или других аномалий, таких, как коарктация, гипоплазия или перерыв дуги аорты, применяют два периода гипотермической остановки кровообращения с 10-15-минутной реперфузией между ними.
Глубокая гипотермия у новорожденных вносит существенный вклад в защиту миокарда и позволяет произвести одноразовую инфузию кардиоплегического раствора на длительное время ишемии миокарда. Повторные дозы кардиоплегии у новорожденных способствуют отеку миокарда.
-
Кальций.
Для поддержания гематокрита в пределах 25-30% в перфузат добавляют кровь, консервированную цитратом, который связывает кальций. Поэтому во время охлаждения концентрация ионизированного кальция низкая. Это важно для улучшения защиты миокарда и уменьшения его послеоперационного отека.
-
Сосудорасширяющие препараты.
После периода остановки кровообращения или значительно сниженного объема перфузии часто отмечается спазм периферических сосудов. Вероятно, он является следствием повреждения эндотелия и связанного с этим снижения активности синтазы оксида азота. В связи с этим полезно во время перфузии вводить сосудосасширяющие средства, такие, как фентоламин, феноксибензамин и нитроглицерин.
Хирургическая техника
Операцию выполняют через срединную стернотомию. Вилочковую железу почти полностью резецируют. Из передней поверхности перикарда выкраивают большой прямоугольный лоскут и сохраняют его в ледяном солевом растворе. Легкое подтягивание турникета на кисетном шве правого ушка позволяет улучшить экспозицию магистральных артерий. Исследование анатомии преследует цели:
-
определить место отхождения и маршрут коронарных артерий;
-
констатировать наличие или отсутствие аномального петлевого хода артерий;
-
определить взаимоотношение магистральных сосудов.
Обычно при d-ТМА аорта расположена спереди легочного ствола. Наиболее частой и простой анатомией является нормальное прохождение коронарных артерий, переднезадняя ориентация магистральных сосудов и примерно одинаковые их размеры.
При выделении сосудов используют электрокоагуляцию. Выделяют и мобилизуют центральные легочные артерии, включая первые ветви в корнях легких. Ветви легочной артерии и аорту обводят резиновыми тесемками. Стенка артериального протока крайне слабая, если продолжается инфузия простагландина. Проток начинают выделять под правой стороной аорты, освобождая его правый край. Подтягивание тесьмы вокруг левой легочной артерии облегчает выделение левого края артериального протока. Под проток подводят две 3/0 лигатуры, которые завязывают сразу после начала искусственного кровообращения. Проток дважды перевязывают и ушивают оба конца. Аортальный конец можно перекрыть сосудистой скобкой. Манипуляции на протоке должны быть крайне осторожными, так как возникшее кровотечение трудно контролировать. Наложение дополнительных прямых швов обычно усиливает кровотечение или приводит к сужению перешейка аорты. Серьезное кровотечение лучше контролировать во время остановки кровообращения. В случае выраженного легочного кровотока через большой артериальный проток пережимают турникетом правую легочную артерию в целях повышения диастолического давления в аорте и улучшения коронарного кровотока.
Накладывают маркировочные швы в проксимальной части легочного ствола для обозначения предполагаемых мест транслокации устьев коронарных артерий с учетом необходимости минимальной ротации артерий. Больного охлаждают до температуры 18 °С в прямой кишке. Зажимают аорту и вводят первую дозу кардиоплегического раствора в просвет аорты в месте предполагаемой аортотомии.
У большинства пациентов с d-ТМА анатомия коронарных артерий приближается к норме. В этих случаях выполняют стандартную операцию Jatene.
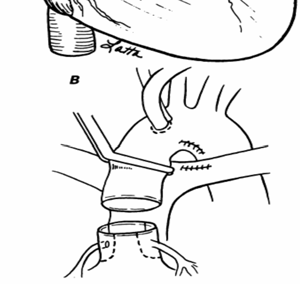
Восходящую аорту пересекают приблизительно на 1 см дистальнее устьев коронарных артерий на уровне бифуркации легочной артерии. Это приблизительно соответствует середине расстояния между зажимом и аортальным кольцом. Аорта должна быть пересечена достаточно высоко, чтобы уменьшить длину реконструируемой аорты, которая будет лежать позади легочной артерии.
По этой же причине легочный ствол пересекают низко, на несколько миллиметров выше комиссур легочного клапана. Низкий разрез оставляет достаточное количество нативной ткани у бифуркации легочной артерии, уменьшает длину корня будущей аорты и позволяет выполнить маневр Lecompte без компрессии. Далее завершают выделение легочных артерий до долевых ветвей. Бифуркацию легочной артерии перемещают кпереди от восходящей аорты, используя второй зажим или пинцет. Зажим на аорте перемещают книзу от бифуркации, располагая рядом с аортальной канюлей для экспозиции максимальной длины дистальной восходящей аорты.
При оптимальном уровне пересечения магистральных сосудов будущая неоаорта короткая, а неолегочная артерия длинная. Зажим на аорте фиксируют в хирургическом поле на 12 ч для стабилизации дистальной аорты.
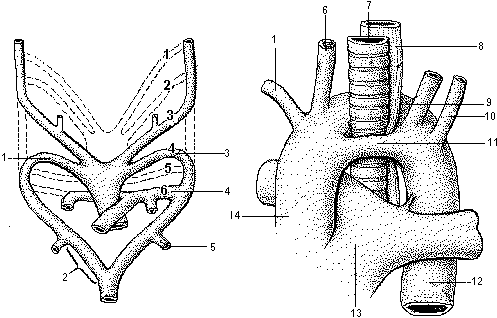
Иссечение и имплантация «пуговиц» коронарных артерий
Коронарные артерии иссекаются вместе с площадкой, составляющей большую часть стенки коронарного синуса, чтобы выполнить анастомоз на безопасном расстоянии от устьев. «Пуговица» представляют собой участок стенки аорты с устьем коронарной артерии. Вначале иссекают левую «пуговицу». Передний вертикальный разрез производят близко к левой латеральной комиссуре, продлевая до дна синуса. Задний вертикальный разрез делают вдоль задней комиссуры. Горизонтальным разрезом, параллельным аортальному кольцу, соединяют два предыдущих. В зависимости от локализации устья этот разрез может быть на большем или меньшем расстоянии от аортального кольца. В редких случаях, когда устье расположено очень низко, аортальное кольцо может быть резецировано в этом месте. С помощью коагуляции отделяют от миокарда 2-4 мм ствола левой коронарной артерии, стараясь не повредить ее ветви. При необходимости мобилизуют также мелкие веточки из-под эпикарда. Таким же образом формируют «пуговицу» правой коронарной артерии, освобождая несколько миллиметров начального участка правой коронарной артерии, чтобы перемещение не сопровождалось перегибом правой коронарной артерии.
Имплантация «пуговиц» коронарных артерий требует соблюдения трех принципов:
1. Места пересадки должны располагаться по латеральным сторонам неоаорты, чтобы они не сдавливались неолегочной артерией, которая лежит спереди.
2. Вырезы в неоаорте должны быть овальными.
3. Место имплантации левой «пуговицы» должно быть ниже, а правой — выше аортального анастомоза.
В местах проксимальной неоаорты, предварительно помеченных маркировочными швами, делают U-образные вырезы, по размерам пуговиц коронарных артерий. Дно этих вырезов обычно находится на уровне вершин комиссур неоаортального клапана. Левую коронарную артерию пересаживают в нижнюю латеральную часть неоаорты. Вершину «пуговицы» выкраивают остроконечной, чтобы она не увеличивала корень неоаорты, который всегда больше, чем размер дистальной восходящей аорты. Край выреза неоаорты должен отступать на 2-3 мм влево от передней комиссуры. Глубина выреза должна соответствовать высоте «пуговицы», но быть не ближе 2 мм от кольца. «Пуговицу» левой коронарной артерии вшивают в соответствующий вырез проленовой нитью 7/0.
Иногда при обычном отхождении коронарных артерий встречается длинная извитая левая главная коронарная артерия без окружающей жировой клетчатки, подвешенная на «брыжейке». В этих случаях артерию реимплантируют правее и выше шва аортального анастомоза.
Неплотности ушивают отдельными швами на этом этапе, так как после завершения реконструкции очень трудно остановить кровотечение, особенно из-под левой коронарной артерии.
Альтернативой U-образному вырезу в неоаорте является J-образный разрез, образующий медиально открывающуюся «дверь». Этот прием уменьшает степень ротации коронарной артерии, однако увеличивает диаметр проксимальной неоаорты, который уже исходно был больше диаметра дистального конца пересеченной аорты.
Правую коронарную артерию имплантируют в латеральной позиции выше аортального анастомоза. Верхнюю часть «пуговицы» выкраивают остроконечной. В латеральном правом крае неоаорты иссекают место для имплантации правой коронарной артерии высотой 2-8 мм, в зависимости от длины свободного перемещения «пуговицы». Слишком низкое размещение правой коронарной артерии является ошибкой. Обычно основание пуговицы пришивают на уровне аортального шва.
Несоосность прилежащих комиссур аортального и легочного клапанов встречается редко и никогда не препятствует перемещению «пуговицы» правой коронарной артерии, так как она располагается выше комиссур. Несоосность может осложнить имплантацию «пуговицы» левой коронарной артерии, которая может точно попасть на переднюю комиссуру. Соосность прилежащих комиссур можно восстановить вращением корня неоаорты вправо, что позволит сместить переднюю комиссуру медиально. При необходимости проксимальную неоаорту можно повернуть на 10-40° вправо и зафиксировать в этом положении несколькими стежками задней линии аортального анастомоза. После поворота проксимальной неоаорты левая «пуговица» может разместиться нормально в левом латеральном положении.
Аортальный анастомоз и имплантация пуговицы правой коронарной артерии в дистальную аорту
Правую коронарную артерию включают в дистальную аорту, выполняя вертикальный разрез. Как правило, диаметры проксимальной и дистальной аорты не совпадают. Анастомоз аорты выполняют непрерывным швом проленовой нитью 6/0. Области в углах «пуговиц» укрепляют матрацными швами. Проксимальная легочная артерия обычно шире дистальной аорты, поэтому при выполнении шва заднюю стенку легочной артерии присобирают, не сморщивая переднюю стенку, содержащую коронарные артерии.
Аортальный анастомоз начинают с правой стороны, используя конец нити, фиксирующей заднюю часть основания правой «пуговицы». Далее выполняют левую часть анастомоза с помощью второго конца этой нити. По ходу шва нить связывают, чтобы не ослаблялась линия шва.
При выполнении анастомоза аорты необходимо обеспечить латеральное положение левой «пуговицы». По достижении середины передней стенки аорты накладывают узловой шов, ориентированный на точку 12 ч по циферблату. Далее линия шва достигает передней части основания правой «пуговицы». Дистальный сегмент восходящей аорты рассекают вертикально на длину, соответствующую высоте правой «пуговицы». При сближении концов нити их связывают вместе. Правую «пуговицу» вшивают в разрез дистальной аорты, начиная от задней части основания и двигаясь вверх. Имплантация правой «пуговицы» позволяет уравнять размеры дистальной и проксимальной аорты и реконструировать синотубулярное соединение.
Перед завершением анастомоза дренаж левого предсердия пережимают, пока левый желудочек не заполнится кровью. После этого связывают концы нитей и открывают дренаж левого предсердия.
Для проверки герметичности анастомоза оба ствола коронарных артерий нежно пережимают пинцетами и открывают аорту. Места неплотностей уточняют с помощью струи солевого раствора из шприца и накладывают дополнительные швы или наносят биологический клей.
Реконструкция неолегочного ствола
Реконструкцию неолегочного ствола лучше выполнять при пережатой аорте. В благоприятных условиях аортальный зажим можно открыть. Кровь из коронарного синуса отсасывают и дополнительной вакуумной линией дренируют правый желудочек.
Для заполнения вырезов в неолегочном стволе используют большой прямоугольный лоскут свежего аутоперикарда, обработанного глютаральдегидом. Используют пролен 6/0.
Заплату помещают в переднее средостение и швы проводят на расстоянии, начиная с левой стороны. По достижении задней комиссуры заплату разрезают вертикально, создавая место для комиссуры. Избыток ткани резецируют. Далее линию шва ведут, повторяя конфигурацию вырезов.
Удаление аортального зажима
После снятия зажима тщательно оценивают качество реперфузии по окраске миокарда и наполнению коронарных артерий. Обращают внимание на прохождение проксимальных стволов коронарных артерий. Начинают согревание пациента.
Дистальный анастомоз легочного ствола
Дистальный анастомоз легочного ствола выполняют непрерывным швом проленом 6/0. Когда шов на задней полуокружности завершен, начинают согревание.
Пересадка коронарных артерий при петлевом прохождении
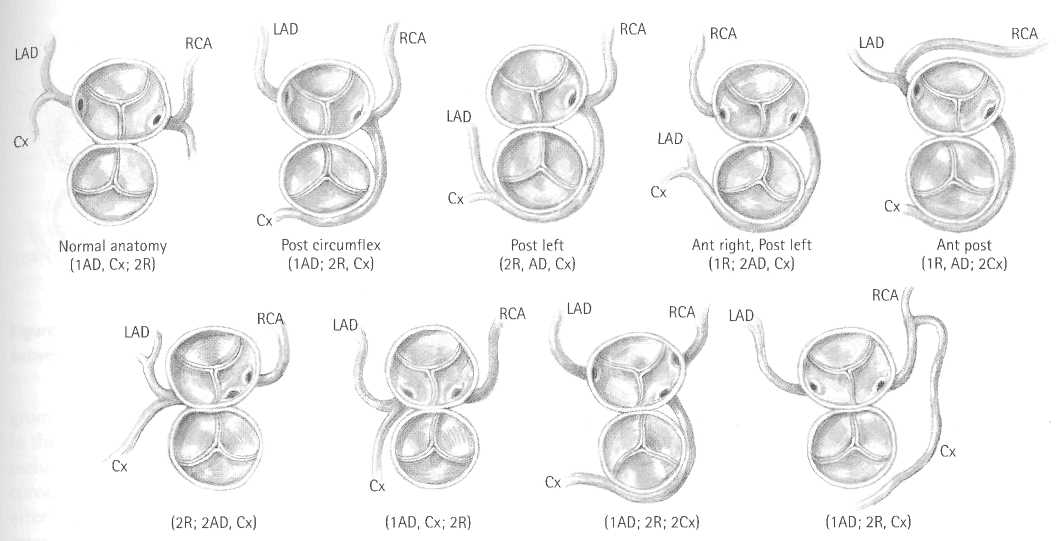
В 35% случаев коронарные артерии образуют петли, проходя позади или спереди легочной артерии. Различают 3 типа петлевого хода коронарных артерий.
1. Задний петлевой ход коронарных артерий встречается у 20% пациентов в двух вариантах:
-
огибающая артерия отходит от правой коронарной артерии и огибает легочный ствол сзади;
-
единственное коронарное устье с общим левым стволом, проходящим позади легочной артерии.
2. Передний петлевой ход коронарных артерий наблюдается у 1% пациентов и существует в трех вариантах, два из которых встречаются в виде единственной коронарной артерии. «Чистая» передняя петля встречается очень редко.
3. Двойные петлевые коронарные артерии имеют место у 14% пациентов. Артерии огибают аорту спереди и легочную артерию сзади. Чаще встречаются два варианта:
-
с задней петлей, образованной общим левым коронарным стволом — инвертированные коронарные артерии по Castaneda
-
с задней петлей, образованной огибающей артерией. Редким вариантом является единственная коронарная артерия.
Техника транслокации всех петлевых коронарных артерий аналогична таковой при нормальном прохождении коронарных артерий. Опасность пересадки артерий зависит от варианта их петлевого хода. Задняя петля создает риск перегиба, а передняя петля — риск растяжения коронарного сосуда.
Для успешной транслокации петлевых коронарных артерий следует руководствоваться тремя принципами:
-
место имплантации «пуговицы» должно быть с боковой поверхности аорты, чтобы артерия не сдавливалась расположенной спереди легочной артерией;
-
отверстие под имплантацию «пуговицы» должно иметь овальную форму;
-
левая «пуговица» должна быть расположена низко, а правая — высоко, выше аортального анастомоза.
Для предупреждения перегиба и растяжения необходимо полное выделение коронарных стволов. В частности, при заднем петлевом ходе огибающей артерии, отходящей от правой коронарной артерии, огибающую артерию следует полностью выделить позади легочного ствола для обеспечения свободной мобилизации. При двойных петлевых коронарных артериях заднюю огибающую артерию максимально выделяют, а переднюю, в данном случае правую коронарную артерию, которая пересекает правый желудочек, выделяют на протяжении 20 мм и отделяют от правого желудочка и аорты.
Пересадка коронарных артерий в нестандартных условиях
Пересадка коронарной артерии при интрамуральном ходе сопровождается большими техническими трудностями. Диагноз этого редкого варианта коронарных артерий до операции устанавливают главным образом с помощью ЭхоКГ и подтверждают после открытия аорты. Во многих случаях эта аномалия является внутриоперационной находкой. Устье левой аномальной коронарной артерии почти во всех случаях расположено высоко в правом синусе в непосредственной близости от задней комиссуры. Вследствие этого начальная часть левой коронарной артерии проходит в толще стенки аорты. Протяженность этого участка может быть достаточно длинной, он может пересекать левый синус сзади. Правое устье также может располагаться необычно. Правая артерия проходит кверху и вправо, изредка она исходит из левого синуса. Два устья близко прилежат один к другому, иногда обе артерии имеют общее устье. Кроме того, левое устье часто гипоплазировано и стенозировано.
Описаны различные методы операций. Наиболее безопасным из них считается метод Azou и Mee. Принцип операции при интрамуральном ходе коронарной артерии заключается в разделении двух устьев. Если обе коронарные артерии отходят от одного синуса, можно ограничиться иссечением единого более длинного блока для обоих устьев при условии, что каждая артерия не имеет интрамурального хода. При этом может потребоваться отделение задней комиссуры неолегочного клапана с последующей ресуспензией на этапе реконструкции легочной артерии перикардом. При наличии интрамурального сегмента одной из коронарных артерий общий блок разделяют на два устья, если это возможно. Интрамуральный ход оценивают с помощью коронарного зонда, его протяженность может быть до 20 мм. Левое устье рассекают на протяжении 5 мм, освобождая его от «крыши». В результате этого расстояние между устьями увеличивается, что позволяет создать две «пуговицы». Выделяя левую «пуговицу», следует с помощью коронарного зонда действовать очень осторожно из-за возможности длинного интрамурального сегмента. Финальный разрез может пройти по самому дну левого синуса, поэтому, в отличие от правой «пуговицы», левая «пуговица» может оказаться сложной конфигурации и крайне длинной. Устья располагаются очень близко к краю «пуговицы», что сильно затрудняет выполнение анастомоза. Для создания точного анастомоза необходимо использовать 8/0 и 9/0 проленовые нити.

В некоторых случаях инфундибулярная артерия отходит высоко от левой главной коронарной артерии. После пересадки левой коронарной артерии инфундибулярная ветвь создает натяжение и стеноз основного ствола, поэтому ее нужно выделить, мобилизовать и пересечь. Реже инфундибулярная ветвь отходит от правой коронарной артерии, и при необходимости ею также следует пожертвовать.
Пересадка коронарных артерий при единственном устье
Единственное коронарное устье является вариантом коронарных артерий, имеющих петлевой ход. По мнению Lacour-Gauet, несмотря на то, что из стенки аорты иссекается только единственная «пуговица», пересадку этих артерий выполняют по тем же принципам, что и артерий, имеющих петлевой ход. Существенным элементом операции является максимальная мобилизация коронарных стволов, идущих как спереди аорты, так и позади легочной артерии. Правую «пуговицу» перемещают в аорту выше линии аортального шва, а левую — ниже линии шва. Единственное устье часто сочетается с расположением магистральных сосудов «бок о бок», что создает дополнительные технические трудности и необходимость смещения бифуркации легочной артерии вправо.
Как отмечалось выше, наиболее частым вариантом единственной коронарной артерии является отхождение общего ствола коронарной артерии от синуса 2 и ответвление от него правой и левой коронарной артерии, которая проходит позади легочного ствола и затем делится на переднюю нисходящую и огибающую артерии. При пересадке в неоаорту имеются анатомические условия для перегиба огибающей артерии и снижения кровотока в зоне ее кровоснабжения — тупого края левого желудочка и задней части межжелудочковой перегородки. Во избежание крутого изгиба артерии используется метод создания полы из передней стенки неоаорты по типу ловушки, открывающейся медиально. Как впоследствии выяснилось, ишемии миокарда способствует дополнительный механизм порочного круга, специфичного для прохождения левых коронарных артерий позади легочной артерии, особенно если они отходят от синуса 2. Пусковым механизмом этого порочного круга служит умеренная степень ишемии левого желудочка, возникающая в результате перегиба, неадекватной мобилизации и натяжения левой главной коронарной артерии, образования петли или перегиба на эпикарде, если артерия не освобождена от эпикардиального жира. Ишемия приводит к растяжению левого желудочка. Часто у новорожденных сердце значительно увеличивается в объеме и не вмещается в грудную клетку. Это приводит к дальнейшему растяжению и перегибу коронарной артерии. Поддержание адекватного артериального давления путем дополнительной трансфузии и увеличение давления наполнения желудочков ухудшают ситуацию.
Образовавшийся «порочный круг» трудно прервать. Полезно попытаться мобилизовать на большем протяжении главную левую коронарную артерию, чтобы ее петля ложилась более свободно. Можно реимплантировать артерию в другое место, используя небольшой лоскут аутоперикарда, хотя это технически трудно из-за необходимости распустить циркулярный шов на легочной артерии для обеспечения необходимой экспозиции. Нужно вновь пережать аорту и повторно ввести в ее корень кардиоплегический раствор. Перечисленные действия существенно удлиняют время перфузии, и поэтому сохраняется угроза отека миокарда.
Предупреждение указанных осложнений перспективнее их лечения. Sheule и Jonas, руководствуясь большим личным опытом, рекомендуют точно следовать приведенным ниже советам.
Первый прием в процессе пересадки коронарных артерий чрезвачайно важен. Пока сердце сокращается и магистральные сосуды находятся под нормальным давлением, накладывают швы-маркеры в места, куда предполагается пересадить коронарные артерии. Они должны быть точно на уровне устьев коронарных артерий. Прежние представления о преимуществе более дистальной фиксации устьев артерий себя не оправдали.
Очень важно избегать ротации при наложении аортального анастомоза. Если проксимальная часть неоаорты будет ротирована, коронарные артерии окажутся не в оптимальном месте. Некоторые хирурги считают полезным перед пересечением легочного ствола наложить 3 шва-держалки: прямо на переднюю стенку и на 120 влево и вправо. Необходимо также избегать ротацию восходящей аорты при ее пережатии.
U-образный вырез в проксимальной неоаорте должен располагаться выше комиссур неоаортального клапана. Следует помнить, что собственный аортальный клапан располагается на субаортальном конусе и потому находится дистальнее неоартального клапана. При иссечении стенки легочной артерии для реимплантации устьев коронарных артерий надо следить, чтобы дно U-образного выреза находилось на уровне вершин комиссур неоаортального клапана или несколько дистальнее.
Фиксация устьев коронарных артерий к U-образным вырезам должна быть тщательно выполнена без перекоса и деформации просвета устья.
Важно мобилизовать адекватную длину единственной главной коронарной артерии и проксимальные отделы правой и левой коронарных артерий, не пересекая мелких ветвей, таких, как артерия синусового узла. Ветви должны быть мобилизованы на протяжении нескольких миллиметров, при необходимости — до 1 см. Выделенные из эпикарда артерии отличаются выраженной эластичностью и хорошо тянутся.
При перемещении единственной коронарной артерии, отходящей от первого синуса, риск развития «порочного круга» с вовлечением фактора отека миокарда отсутствует. Устья обеих коронарных артерий иссекают общим блоком. Верхний его край пришивают непосредственно к краю подлежащей проксимальной легочной артерии. К полуокружности этого блока подшивают лоскут аутоперикарда, формируя карман. Образованный синус, не ротирован ни в каком направлении. Восходящую аорту пришивают к передней стенке этого кармана во время выполнения неоаортального анастомоза.
Была предложена также модификация приведенной выше методики, при которой коронарные артерии не иссекаются и остаются in situ. В стенке аорты в области синуса вырезают углубление. Более глубокий вырез делают в стенке прилежащей проксимальной легочной артерии и края обоих вырезов сшивают. Формируют карман, используя не перикард, а частично иссеченную стенку соседнего некоронарного синуса. Ее пришивают в глубину синуса, содержащего устья коронарных артерий. При анастомозировании неоаорты край кармана вовлекают в шов таким образом, что содержащий коронарные артерии карман оказывается в просвете аорты. При реконструировании неолегочной артерии передняя стенка кармана становится ее задней стенкой.
Этот вариант анатомии коронарных артерий часто наблюдается, когда аорта и легочная артерия лежат «бок о бок». Устье артерии при этом расположено более кпереди. Единственный ствол дает начало правой коронарной артерии, которая проходит спереди аорты. Трудность ее пересадки заключается в том, что «пуговица» устья должна быть повернута на 1800 относительно правой коронарной артерии, в то время как при пересадке обычных артерий происходит ротация «пуговицы» к прилежащей неоаорте не более чем на 900. Как правило, удается выделить правую главную коронарную артерию из ее эпикардиального ложа, что обеспечивает достаточную мобильность, позволяющую подтянуть артерию к легочному стволу и анастомозировать «пуговицу» без чрезмерного натяжения. В случаях сильного натяжения артерию можно удлинить трубкой диаметром 4 мм и длиной 4-5 мм, свернутой из аутоперикарда. Размер этой трубки достаточен для взрослого.
В редких случаях единственной коронарной артерии, идущей между аортой и легочной артерией, «пуговицу» устья нужно было бы развернуть на 1800, что привело бы к окклюзии артерии. Предложен прием, который позволяет ротировать «пуговицу» только на 900. Используется лоскут аутоперикарда для создания крыши.
Пересадка коронарных артерий является ключевым элементом операции артериального переключения, от которого зависят непосредственная летальность и осложнения отдаленного периода. Перегиб и растяжение пересаженных коронарных артерий приводят к летальной ишемии миокарда. Даже у переживших операцию больных с ростом ребенка может развиться поздняя обструкция коронарных артерий. Поэтому, несмотря на, казалось бы, установившуюся технику операций и низкую госпитальную летальность в клиниках, накопивших большой опыт этих операций, в литературе появляются новые предложения по методике транслокации коронарных артерий. Их цель — сделать операцию независимой от индивидуального искусства хирурга, особенно в трудных для пересадки вариантах анатомии — интрамуральных коронарных артериях, артериях с коротким стволом, множественных устьях коронарных артерий в одном синусе, прохождении коронарнарной артерии между магистральными артериями.
Исходные пространственные отношения между площадкой коронарного синуса Вальсальвы и стволом артерии после транслокации в легочную артерию изменяются в лучшем случае на 900. Протокольными стали приемы, позволяющие если не устранить, то уменьшить степень нарушения исходной геометрии площадки коронарного синуса Вальсальвы и ствола коронарной артерии. Так, при типе Г по Yacoub и Radley-Smith, при котором огибающая артерия отходит от правого заднего синуса и проходит позади легочного ствола, место пересадки коронарной артерии на легочный ствол смещают краниально, чтобы избежать перегиба огибающей артерии. Однако при этой методике сохраняется риск растяжения артерии.
Этой же цели служит прием «открытой двери», описанный еще в 1988 г.. Несомненная польза этого приема уменьшается возможностью сморщивания содержащих устья коронарных артерий выступов неоаорты после анастомозирования дистальной аорты с неоаортой.

Для увеличения объема канала пересаживаемых коронарных артерий используют дополнительную заплату из аутоперикарда. Этот метод чреват такими осложнениями, как тромбоз, отсутствие роста и дегенерация, поэтому его нельзя признать идеальным.
Yamagiushi и соавторы предложили способ транслокации коронарных артерий, который является дальнейшим усовершенствованием приема «trap door» и его последующей модификации. После стандартного начала операции аорту пересекают достаточно высоко — на 10 мм выше устья коронарной артерии. Легочную артерию пересекают у бифуркации. После тщательного подтверждения конфигурации коронарных устьев и характера ствола коронарной артерии иссекают U-образные «пуговицы» устьев. Множественные устья одного синуса высекают в едином U-образном блоке. Поскольку восходящая аорта пересекается выше, чем обычно, «пуговица» имеет удлиненную форму. Используя маркировочный шов на проксимальном пеньке легочной артерии, рассекают его переднюю стенку в виде клюшки. Разрез не продолжают вглубь синуса Вальсальвы, ограничиваясь синотубулярной зоной, чтобы сохранить конфигурацию синуса. «Пуговицу» коронарной артерии пришивают нитью 7/0, начиная с основания выреза. Когда шов достигает верхнего уровня пенька легочного ствола, избыточную часть «пуговицы» сгибают и сшивают с верхним краем «двери» легочного ствола, формируя выпячивающийся коронарный канал. После перемещения бифуркации легочной артерии кпереди от восходящей аорты легочный ствол анастомозируют с дистальной аортой нитью 6/0. При этом переднюю стенку восходящей аорты анастомозируют с внутренним краем согнутой «пуговицы». При необходимости этим способом пересаживают и вторую артерию. Далее реконструкцию неолегочной артерии выполняют как обычно.
По мнению авторов, этот метод обладает рядом преимуществ перед методом trap door, так как создает более широкий коронарный канал, который не деформируется после выполнения анастомоза между дистальной аортой и неоаортой, не используются нерастущие ткани, не требуется проведения разреза легочного ствола вглубь коронарного синуса при коротком стволе коронарной артерии. Последнее позволяет избежать деформации синуса Вальсальвы и дальнейшей регургитации неоаортального клапана. Данный метод хорош при несовпадении комиссур аортального и легочного клапанов, так как местом транслокации коронарной артерии на неоаорту является синотубулярная зона, и нет необходимости углубляться в синус Вальсальвы. При общепринятой технике, правильное определение места имплантации коронарной артерии в неоаорту зависит от опыта хирурга. Этот фактор существенно влияет на осложнения при операции артериального переключения. Данный метод значительно снижает зависимость качества транслокации коронарной артерии от индивидуального опыта хирурга, может стать стандартной универсальной методикой и особенно показан при интрамуральных коронарных артериях, коротком стволе коронарной артерии и множественных устьях коронарной артерии в одном синусе. Однако, по мнению авторов, она не пригодна при типах Б и В по классификации Yacoub и Radley-Smith.
Одной из проблем пересадки единственной коронарной артерии при расположении магистральных сосудов «бок о бок» и при аномалии Taussig-Bing является компрессия левой «пуговицы», от которой отходит правая петлевая коронарная артерия, бифуркацией легочной артерии. Для предупреждения сдавления правой коронарной артерии рассекают правую легочную артерию от бифуркации вправо на 20 мм и анастомозируют реконструированный легочный ствол непосредственно с правой легочной артерией для смещения легочного ствола вправо. Левую часть легочного ствола закрывают заплатой или ушиванием для увеличения длины левой легочной артерии.
Внутрисердечный этап операции
Закрытие межпредсердного дефекта и ДМЖП производится после завершения конструирования неоаорты. Вводят дополнительную дозу кардиоплегического раствора в просвет неоарты в условиях полной скорости перфузии при температуре 22 0С или, по выбору хирурга, при полной остановке кровообращения и температуре 18 0С. Дефект межжелудочковой перегородки закрывают через просвет аорты или через разрез правого предсердия непрерывным или матрацным швом с прокладками. Дефект межпредсердной перегородки ушивают.
Заключительную часть операции выполняют при восстановленном коронарном кровотоке. Зажим с аорты снимают. Обследуют состояние кровоснабжения всех отделов сердца, заполнение коронарных артерий. При наличии внешних признаков гипоперфузии миокарда проводят ревизию качества транслокации коронарных артерий. При необходимости зажимают аорту, вновь вводят кар- диоплегический раствор в корень аорты, распускают шов на легочной артерии и проводят соответствующую коррекцию коронарных анастомозов.
Во время согревания вводят катетер в левое предсердие для мониторирования давления.
Больного отлучают от АИК на фоне кардиотонической поддержки допамином в дозе 5 мкг/кг/мин. Для мониторирования давления и газов венозной крови вводят катетер в ушко правого предсердия.
Завершение операции
После завершения коррекции для мониторирования давления вводят катетеры в ушко левого предсердия и в неолегочный ствол через линию шва. Оба катетера фиксируют к эпикарду проленом 6/0. Пришивают электроды к правым предсердию и желудочку. Проводят предсердную стимуляцию для поддержания синусового ритма 130-150 ударов в минуту. После полного согревания искусственное кровообращение останавливают на фоне инфузии допамина 5-10 мг/кг/мин, при необходимости применяют милринон и адреналин. Тщательно обследуют состояние перфузии сердца.
Признаками ишемии являются бледность миокарда и повышение давления в левом предсердии, которые обнаруживаются раньше, чем изменения на ЭКГ. Повышение давления в левом предсердии более 10 мм рт. ст. свидетельствует скорее о механическом нарушении кровотока по коронарным артериям, чем об исходной несосостоятельности левого желудочка, и требует немедленного возобновления искусственного кровообращения и коррекции качества транслокации коронарных артерий. Дисфункция левого желудочка на фоне нормального коронарного кровотока обычно связана с недостатком массы левого желудочка и может потребовать ранней ЭКМО.
Операции у новорожденных часто осложняются отеком миокарда. В этих случаях прибегают к отсроченному закрытию раны. Грудину не сводят, оставляя распорки из резиновых трубок, для того чтобы края распила грудины не сомкнулись. Рану закрывают пленкой или зашивают мобилизованную кожу с подкожной клетчаткой. Через 2-4 дня рану закрывают полностью в отделении интенсивной терапии.
-
Гемостаз.
Кровотечение является одним из частых осложнений операции артериального переключения. С накоплением опыта проблемы гемостаза становятся редкими. Если кровотечение не удается остановить обычными средствами, возобновляют искусственное кровообращение и при необходимости распускают шов дистального легочного анастомоза, чтобы получить доступ ко всем кровоточащим местам.
Послеоперационный период
Больного доставляют в отделение интенсивной терапии, не прерывая введения релаксирующих средств и искусственной вентиляции. Парциальное напряжение кислорода вначале понижено и постепенно возрастает в течение 12 ч. После операции в течение 9-18 ч сердечный выброс обычно снижен на 10-20%, что сопровождается умеренной олигурией при отсутствии признаков низкого сердечного выброса, таких, как снижение периферической перфузии и гипотензии. Больным назначают минимальные дозы кардиотоников, одновременно продолжая введение периферических вазодилататоров. Путем манипуляции объемной нагрузкой стараются удерживать давление в левом предсердии до 10 мм рт. ст. и артериальное давление не выше 60 мм рт. ст., чтобы не создавать избыточную постнагрузку, приводящую к растяжению левого желудочка, повышению давления в левом предсердии и развитию митральной недостаточности. Артериальная гипертензия также способствует кровотечению. При отсутствии сердечной недостаточности и кровотечения больного отлучают от ИВЛ, как правило, в течение 48 ч после операции.
У больных, оперированных после 2-3 нед. и не имеющих значимого ОАП или динамической обструкции выводного тракта левого желудочка, среднее артериальное давление в течение 2-3 дней удерживают на уровне 40-45 мм рт. ст. при условии, что конечности остаются теплыми. У этих пациентов избегают объемной перегрузки и стараются удержать давление в левом предсердии на уровне 6-8 мм рт. ст., пока не увеличится масса миокарда левого желудочка. Экстубацию производят на 3-6-е сутки после операции. Если при отлучении от вентиляции давление в предсердии становится выше 10 мм рт. ст., больного возвращают на полную вентиляцию и через 2 сут. предпринимают новую попытку. Периферические вазодилататоры продолжают вводить в течение 3-4 дней после экстубации.
Осложнения отдаленного периода после операции артериального переключения
Артериальное переключение с максимальным приближением воссоздает нормальные анатомические соотношения. Оно имеет существенное преимущество, так как не сопровождается осложнениями, характерными для внутрикардиальной коррекции гемодинамики. Однако у 5-10% больных развивается СЛА в месте реконструкции, у 5-10% — полная AV-блокада, у 20% — недостаточность аортального клапана как позднее осложнение, особенно у больных после суживания легочной артерии. Причиной аортальной недостаточности могут быть также неравные размеры створок легочного клапана и их эксцентрическая коаптация. Как ранним, так и поздним осложнением является обструкция коронарных артерий, которая может привести к ишемии миокарда, инфаркту и даже смерти. Указанные осложнения встречаются все реже по мере совершенствования методики операции и при выраженных нарушениях устраняются хирургическим путем.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания








Комментарии