Транспозиция магистральных артерий: показания, последствия, фото
Полная транспозиция магистральных артерий представляет собой аномалию вентрикулоартериального соединения, при котором на фоне предсердного situs solitus аорта отходит от анатомически правого желудочка, а легочная артерия — от анатомически левого желудочка. Порок сопровождается аномальными пространственными отношениями между магистральными сосудами, что является важным, но не принципиальным признаком.
Классическую полную ТМА называют d-транспозицией, при которой аорта расположена спереди и справа от легочного ствола.
Полная транспозиция магистральных артерий составляет 5-7% всех ВПС, чаще она наблюдается у лиц мужского пола. Первое описание сердца с транспонированными магистральными артериями принадлежит Bailie. Позже, в 1814 г., Farre впервые использовал этот термин, отражающий аномальное расположение больших сосудов относительно межжелудочковой перегородки.
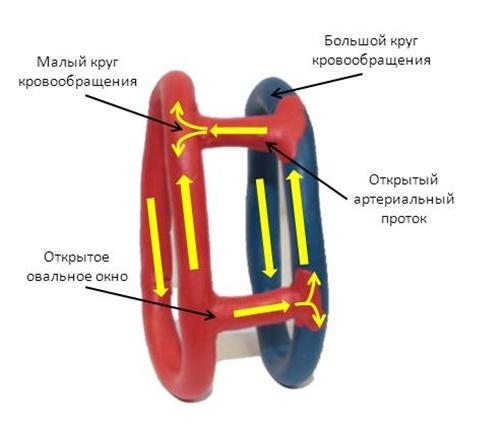
Анатомия
Аорта, расположенная спереди, отходит от правого желудочка, а легочная артерия позади аорты — от левого желудочка. Отличительной анатомической особенностью порока является наличие митрально-легочного контакта и субаортального конуса.
В нормальном сердце аорта отходит от левого желудочка, имеется митрально-аортальный фиброзный контакт и подлегочный конус. При d-ТМА легочное и системное кровообращение полностью разделены. Десатурировання кровь циркулирует в большом круге кровообращения, а насыщенная кислородом кровь — в малом.
Для выживания больного необходимо перемешивание крови, которое происходит на различных уровнях — через ДМПП, ДМЖП и ОАП.
У 50% больных кровь смешивается недостаточно — только через открытое овальное окно или небольшой ОАП.
У 20% пациентов имеется динамическая обструкция выводного тракта левого желудочка во время систолы, возникающая вследствие смещения межжелудочковой перегородки влево из-за более высокого давления в правом желудочке. Однако в период диастолы выводной тракт левого желудочка свободен. Выбухание межжелудочковой перегородки влево происходит в течение неонатального периода по мере снижения давления в левом желудочке ниже системного уровня при отсутствии легочной гипертензии и анатомической обструкции выводного тракта левого желудочка. Выпячивание перегородки в период систолы отражает противоположное норме транссептальное соотношение давлений в желудочках при ТМА. После коррекции гемодинамики на предсердном уровне часто обнаруживается градиент систолического давления от небольшого до умеренного на подлегочном выводном тракте.
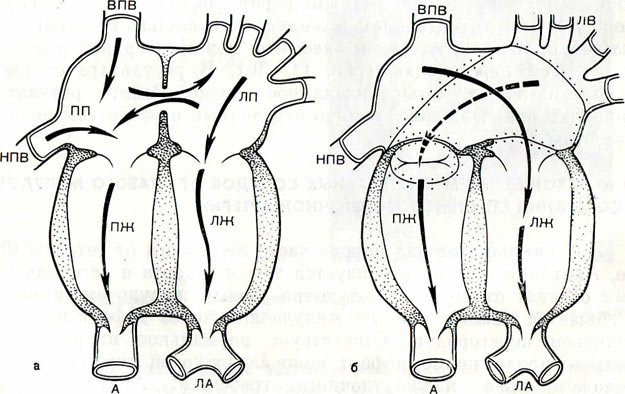
Особая форма подлегочного сужения образуется в результате отклонения инфундибулярной перегородки кзади при ДМЖП, образовавшемся вследствие нарушения соосности обеих частей перегородки — Malalignment defect.
Фиксированная форма обструкции развивается у некоторых младенцев за счет появления пластинчатого утолщения эндокарда на выбухающей перегородке. Оно подвергается фиброзному перерождению с образованием острого гребня или дискретной мембраны, аналогичной мембранозному субаортальному стенозу по линии митрально-аортального контакта. Реже фиксированная подлегочная обструкция представлена туннелевидным фиброзно-мышечным сужением выводного тракта, распространяющимся до передней створки митрального клапана. Редко встречаются клапанный стеноз или гипоплазия кольца, которые почти всегда сочетаются с комбинированными подклапанными обструктивными поражениями. Другие редкие формы подлегочного стеноза обусловлены:
-
прикреплением передней створки митрального клапана к мышечной части выводной перегородки аномальной фиброзной или хордальной тканью;
-
избыточной тканью трехстворчатого клапана в виде мешочка, пролабирующего через ДМЖП;
-
подлегочной мембраной;
-
аневризмой мембранозной перегородки;
-
гипертрофией мышцы Moulaert.
Дефект межжелудочковой перегородки встречается у 30-40% больных и может локализоваться в различных отделах перегородки. У 10% больных имеется так называемая сложная форма ТМА, представляющая собой сочетание ДМЖП с выраженной обструкцией тракта оттока левого желудочка. Среди других сопутствующих аномалий чаще встречаются коартация аорты, перерыв дуги аорты, атрезия легочной артерии, добавочная верхняя полая вена, аномальный дренаж легочных вен.
Обструкция системного кровотока у больных с транспозиционными комплексами значительно изменяет патофизиологию и естественное течение этих пороков, влияя на время, характер вмешательства и исходы лечения. Препятствие оттоку крови из правого желудочка в большой круг кровообращения может располагаться на различных уровнях — субаортальном, клапанном, на уровне дуги аорты и на нескольких уровнях одновременно. Клапанный стеноз и атрезия аортального клапана наблюдаются крайне редко.
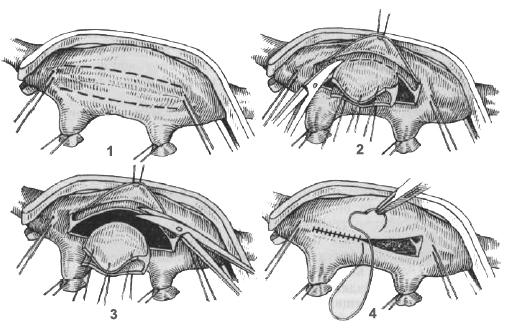
Субаортальный стеноз редко встречается при ТМА с интактной межжелудочковой перегородкой, однако при ТМА с ДМЖП — у 20-40% больных, особенно при передних ДМЖП, образовавшихся вследствие смещения инфундибулярной части перегородки. Смещение инфундибулярной перегородки кпереди и вправо приводит к сужению подклапанного конуса, что является причиной перераспределения кровотока в пользу легочного. Этому способствуют также гипертрофия септомаргинальной трабекулы, вентрикулоинфундибулярной складки и аномального прикрепления AV-клапанов. Наиболее часто субаортальный стеноз наблюдается при аномалии Taussig-Bing.
Сужение на уровне дуги при ТМА-ИМЖП отмечается у 2-3% больных, однако при ТМА-ДМЖП этот показатель достигает 10-30% и непропорционально увеличивается при Malalignement ДМЖП — до 88%. Обструкция на уровне дуги при аномалии Taussig-Bing встречается, по данным разных авторов, в среднем у 50% пациентов и часто сопровождается субаортальным стенозом, особенно при аномалии Taussig-Bing. Она бывает в форме коарктации, тубулярной гипоплазии или перерыва дуги аорты. Считается, что первоначальное неравное разделение аортального и легочного выводных трактов у плода приводит к преимущественному направлению кровотока в легочную артерию, ОАП и нисходящую аорту. Следствием этого является недоразвитие дуги аорты в трех упомянутых выше формах. При аномалии Taussig-Bing субаортальный инфундибулум часто гипоплазирован, поскольку он обычно расположен между трехстворчатым клапаном и подлегочным конусом.
Диагностика коарктации и перерыва дуги аорты не вызывает затруднений, чего нельзя сказать о гипоплазии дуги. В то время как тубулярная гипоплазия отмечается в 60% случаев изолированной коарктации аорты, ее частота превышает 90% в комплексе с внутрисердечными аномалиями.
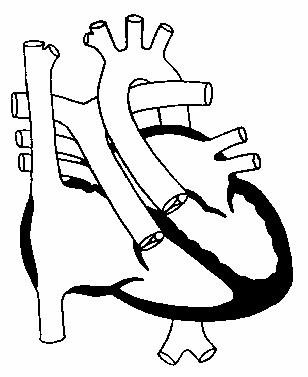
Индивидуальная анатомия коронарных артерий при ТМА принципиально важна в силу специфики анатомической коррекции порока.
Аномалии устьев коронарных артерий
Сужение и атрезия устья коронарной артерии обычно компенсируются более развитыми артериями и не проявляют себя до операции, однако во время и после вмешательства они представляют потенциальную угрозу развития инфаркта миокарда или ишемии и снижения сердечного выброса.
-
Интрамуральные коронарные артерии.
С хирургической точки зрения идеальными являются артерии, отходящие высоко от соответствующего синуса Вальсальвы и расположенные в центре между двумя комиссурами. На практике существует множество вариантов анатомии коронарных артерий, усложняющих их перемещение. Например, устье может быть расположено очень низко в синусе Вальсальвы у места прикрепления створки клапана. Иссечение устья может сопровождаться повреждением основания створки и требует очень тщательного наложения шва из-за риска последующего кровотечения. Нередко устье может быть расположено близко к одной из комиссур, обычно у задней комиссуры. При таком эксцентрическом расположении устья в синусе оно часто имеет щелевидную форму. Центрально расположенное устье имеет круглую форму, и проволочный зонд может быть проведен в артерию перпендикулярно к стенке синуса. В противоположность этому при щелевидном синусе зонд проходит в артерию под острым углом. Некоторые наблюдения показывают, что даже при нормальном расположении магистральных сосудов и косой форме устья коронарной артерии существует повышенный риск острой коронарной ишемии и внезапной смерти во время физической нагрузки. Эта анатомическая особенность при выполнении операции артериального переключения у больных с ТМА играет большую роль в развитии ишемии миокарда.
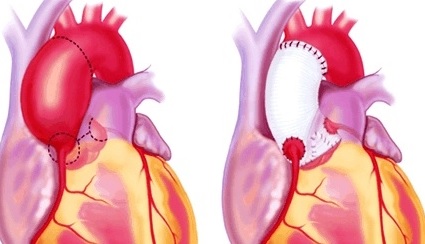
Крайним вариантом эксцентрического расположения устья является его смещение в прилежащий соседний синус Вальсальвы. В результате оба устья оказываются расположеными рядом:
-
одно находится в центре синуса;
-
другое, обычно левое, расположено между правым устьем и задней комиссурой.
Аномальная коронарная артерия отходит от синуса не под прямым углом, а очень косо и фактически остается в толще стенки аорты и далее прилежит к соответствующему синусу Вальсальвы. Снаружи распределение коронарных артерий выглядит обычным, однако изнутри аорты обнаруживаются два устья в одном синусе. Важно помнить, что интрамуральная коронарная артерия часто проходит позади задней комиссуры аортального клапана. Эта комиссура неолегочного клапана должна быть отсепарирована при формировании «пуговицы», содержащей интрамуральную коронарную артерию на всю длину интрамурального хода.
Единственное коронарное устье является крайним вариантом интрамуральной коронарной артерии. Благодаря более длинному интрамуральному прохождению аномальное устье тесно прилежит к другому, и может даже слиться с ним, образуя единственное коронарное устье.
Ветвление коронарных артерий при d-ТМА
Для систематизации множества вариантов ветвления коронарных артерий, наблюдающихся при d-ТМА, предложено несколько различных классификаций.
Лейденская конвенция является широко используемой системой классификации. Данная классификация определяет синусы аорты, от которых отходят три главные коронарные артерии. Два аортальных синуса Вальсальвы, прилежащие к аортолегочной перегородке, обращены к соответствующим синусам легочной артерии и в 99% случаев содержат устья коронарных артерий. Их называют «септальными» или «facing» синусами. Согласно конвенции, принято обозначать цифрами коронарные синусы:
-
синус 1 — прилежащий к легочной артерии с левой стороны;
-
синус 2 — прилежащий к легочной артерии с правой стороны.
Если магистральные артерии расположены в переднезадней проекции, септальные синусы направлены влево и вправо. Если артерии расположены бок о бок, синусы направлены соответственно кпереди и кзади. Если аорта расположена спереди и справа от легочной артерии, септальные синусы имеют переднелевое и заднеправое расположение.
В сердцах с нормальным расположением магистральных артерий имеются три главные коронарные артерии:
-
правая коронарная артерия, идущая в правой AV-борозде;
-
огибающая коронарная артерия, проходящая в левой AV-борозде;
-
передняя нисходящая артерия, идущая параллельно межжелудочковой перегородке по передней поверхности сердца.
Кроме вариабельности дистального распределения, проксимальная часть каждой из трех больших ветвей может следовать интрамуральным курсом, обычно между двумя магистральными сосудами. В этих случаях медии аортальной и коронарной стенок соединены между собой без разделения их адвентицией.
Наиболее часто встречающимся вариантом является отхождение передней нисходящей и огибающей артерий от синуса 1. Синус 2 дает начало правой коронарной артерии. Согласно общепринятым аббревиатурам, этот вариант описывается как 1AD, CX; 2R.
Yamaguchi и соавторы предложили следующий уровень классификации для обозначения характера прохождения коронарных артерий по эпикарду. Единственная коронарная артерия, отходящая от синуса 2 с левой коронарной артерией, направляющейся влево позади легочной артерии, обозначается как 2R, AD, CX c задним левым направлением.
Yacoub и Radley-Smith в 1978 г. предложили ныне популярную классификацию, согласно которой 6 вариантов отхождения и ветвления коронарных артерий получили буквенное обозначение — от А до Е. Обычная анатомия коронарных артерий классифицируется как тип А.
Описательная классификация вариантов ветвления коронарных артерий. В детском госпитале Гарвардской медицинской школы отказались от приведенных выше классификаций из-за того, что они не отражают многочисленных вариантов коронарных артерий при d-ТМА, и применяют описательный метод для подробного обозначения индивидуальной анатомии больного. Полагают, что в первую очередь должны быть описаны пространственные отношения аорты и легочного ствола.
При такой ориентации сосудов коронарные артерии отходят от синусов 1 и 2 как при наиболее часто встречающемся варианте.
Описательная классификация, по мнению авторов, позволяет выделить такие варианты анатомии коронарных артерий, которые являются существенными при статистической оценке степени риска:
1. Все коронарные артерии, отходящие от одного синуса.
2. Интрамуральные коронарные артерии.
3. Ретропульмональное прохождение всей левой коронарной системы.
4. Ретропульмональное расположение только огибающей артерии.
5. Левая коронарная артерия или любая ее ветвь, исходящие из синуса 2.
Классификация Marie Lannelongue основана главным образом на маршруте коронарных артерий и не акцентирует локализацию устий. Техника транслокации коронарных артерий определяется характером их прохождения. При situs solitus идентифицируют устья левой и правой коронарных артерий. Выделяют четыре варианта маршрута коронарных артерий:
1. Нормальный курс.
2. Петлевой курс.
3. Внутримышечный курс.
4. Смешанные варианты прохождения, включающие внутримышечный и петлевой курс.
Чаще других встречается единственное устье в синусе 2. От единственного коронарного ствола ответвляется левая главная коронарная артерия, которая проходит позади легочной артерии перед делением на огибающую и переднюю нисходящую артерии. Правая коронарная артерия, как обычно, расположена в правой AV-борозде.
Вторым по частоте является вариант, при котором единственное устье встречается в синусе 1. Правая коронарная артерия проходит спереди аорты и далее идет в АV-борозде. Левая коронарная артерия расположена обычно. У 10% пациентов единственное устье расположено в синусе 2, и левая главная коронарная артерия пересекает аорту спереди перед ее вхождением в левую АV-борозду. Правая коронарная артерия следует нормальным курсом в правой АV-борозде. Изредка встречается вариант, при котором устье расположено в синусе 2, а левая коронарная артерия проходит между аортой и легочной артерией и далее в АV-борозде, а правая артерия идет нормально. При наиболее редко встречающемся варианте единое устье находится в синусе 1. Правая коронарная артерия огибает легочный ствол позади, а левая проходит нормально.
Гемодинамика
Кровоток при ТМА осуществляется по двум разобщенным кругам кровообращения. В аорту поступает венозная кровь из правого желудочка. Пройдя большой круг кровообращения, она возвращается в правые отделы сердца. Левый желудочек получает артериализированную кровь из легочных вен и нагнетает ее в легочную артерию. Смешение крови двух кругов кровообращения возможно лишь при наличии сообщений на различных уровнях. Степень артериальной гипоксемии зависит от размера сообщений и, соответственно, от объема смешивания легочного и системного венозного возврата крови. Сброс крови осуществляется в двух направлениях, так как односторонний его характер привел бы к полному опорожнению одного из кругов кровообращения. При так называемой простой транспозиции смешивание венозной и артериальной крови происходит только на предсердном уровне через овальное окно и на уровне магистральных артерий через ОАП. Обычно это смешивание минимальное, поэтому имеет место тяжелая гипоксемия. Внутриутробное кровообращение не страдает при этой аномалии. Однако сразу после рождения остро возникает угроза жизни из-за низкого насыщения системной артериальной крови кислородом. В случаях, когда имеются широкие сообщения на разных уровнях между большим и малым кругами кровообращения, гипоксемия невыраженная. При небольшом и среднем ДМЖП сброс крови справа налево происходит во время систолы, слева направо — во время диастолы. При большом ДМЖП с легочной гипертензией из-за быстро развивающейся обструктивной болезни легочных сосудов, а также при выраженном стенозе легочной артерии сброс крови справа налево происходит в диастолу, слева направо — в систолу. При наличии сообщений на разных уровнях сброс крови через них осуществляется в противоположных направлениях.
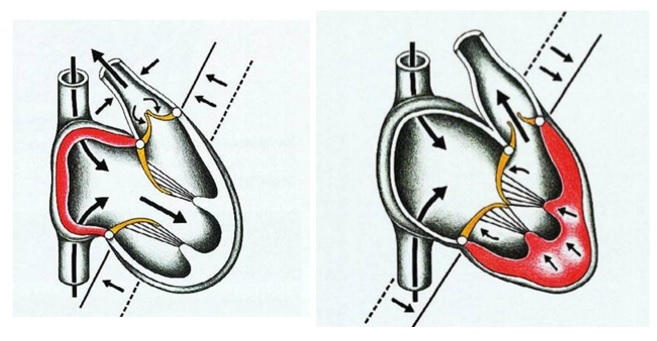
При тяжелой обструкции тракта оттока правого желудочка кровоток в большом круге является дуктусзависимым. Закрытие ОАП сопровождается быстро прогрессирующим ухудшением системной перфузии с развитием метаболического ацидоза, острой почечной недостаточности и некротического энтероколита. Клиническое течение абсолютно безысходное, если не открыть ОАП инфузией простагландинов. При умеренной обструкции системный кровоток может быть независимым от ОАП. Тем не менее, клиническая картина характеризуется усиленным легочным кровотоком, тяжелой застойной сердечной недостаточностью и отеком легких.
Для ТМА характерно асимметричное распределение кровотока между правым и левым легкими. На рентгенограммах грудной клетки, легочных контрастных и радиоизотопных ангиограммах у 50% больных с ТМА обнаруживается преимущественно правостороннее направление кровотока. Эта неравномерность распределения кровотока отсутствует у новорожденных и с разной степенью выраженности прогрессирует со временем. В редких случаях она может привести к прекращению эффективной перфузии левого легкого. Распределение кровотока зависит от наклона легочного ствола, который создает прямой ток крови из левого желудочка в правую легочную артерию. У больных вне периода новорожденности инерция потока крови усиливается благодаря увеличению линейной скорости кровотока, обусловленному развивающимся сужением тракта оттока и ударного объема левого желудочка, который увеличивается в первые месяцы жизни у не оперированных пациентов. Правостороннее направление кровотока сопровождается недоразвитием левых легочных сосудов и проявляется, в частности, левосторонним стенозом или гипоплазией легочных вен. Это обнаруживается при катетеризации или при операциях предсердного переключения венозного возврата. Феномен аномального перераспределения не оказывает заметного влияния на течение ТМА и не обнаруживается у больных, подвергшихся неонатальной операции артериального переключения.
Клиника
Для больных с ТМА характерно сочетание цианоза с застойной сердечной недостаточностью, одышкой, трудностями кормления в период новорожденности. Особенно цианотичны новорожденные мальчики с большой массой тела; тахипное обычно без втяжения, если нет застойной сердечной недостаточности.
Второй тон громкий, нерасщепленный. Шумы отсутствуют при интактной межжелудочковой перегородке. Систолический шум слышен у больных с сопутствующим ДМЖП. Эти дети обычно менее цианотичны. Иногда выслушивается мягкий систолический шум выброса при стенозе легочной артерии.
При застойной сердечной недостаточности увеличена печень.
При исследовании газов крови отмечается тяжелая артериальная гипоксемия, которая не устраняется ингаляцией кислорода.
-
Электрокардиография.
Электрическая ось сердца отклонена вправо. Гипертрофия правого желудочка сохраняется при простой ТМА. Гипертрофия обоих желудочков регистрируется при сопутствующих ДМЖП, ОАП, ОБЛС, так как их наличие сопровождается дополнительной гипертрофией левого желудочка. Иногда отмечается гипертрофия правого предсердия.
-
Рентгенограмма.
Характерны кардиомегалия, яйцеобразная форма сердечной тени с узким верхним средостением. Легочной рисунок усилен.
-
Эхокардиографическое исследование.
Эхокардиографическое исследование, включающее цветную допплерографию, демонстрирует все анатомические и функциональные данные, необходимые для проведения лечения:
-
наличие дискордантных вентрикулоартериальных соотношений;
-
пространственную ориентацию магистральных сосудов;
-
отхождение проксимальных сегментов коронарных артерий;
-
большинство важных сопутствующих аномалий, включая количество, размер и локализацию ДМЖП, анатомический тип обструкции выводного тракта левого желудочка, аномалии AV-клапанов, наличие пороков, обусловленных нарушением соосности частей межжелудочковой перегородки и связанным с ней отхождением обоих магистральных сосудов от правого желудочка с подлегочным ДМЖП и нависающей легочной артерией.
Эхокардиография стала методом, достаточным для принятия решения об операции при простой ТМА, во многих центрах оставляя для катетеризации баллонную септостомию. Критериями для выполнения операции артериального переключения являются: нормальные размеры левого желудочка, адекватная толщина задней стенки левого желудочка, геометрия левого желудочка и искривление межжелудочковой перегородки, отражающее степень снижения давления в левом желудочке. Митральный клапан и выводной тракт левого желудочка должны иметь относительно нормальные размеры и функцию. Выводной тракт должен быть обследован для выявления анатомической обструкции. Динамическая или хирургически устранимая обструкция не являются противопоказанием к выполнению артериального переключения.
-
Катетеризация сердца и ангиография.
Несмотря на то, что баллонная септостомия является рутинным методом стабилизации больных с транспозицией, полная гемодинамическая и ангиографическая информация, получаемая при катетеризации, утратила свое прежнее диагностическое значение. Поэтому эта часть процедуры катетеризации не является обязательной. Это связано не только с совершенствованием метода ЭхоКГ, но и с развитием хирургической техники, позволяющей произвести успешную транслокацию коронарных артерий при любом анатомическом варианте. Тем не менее, катетеризацию, предпринимаемую для выполнения баллонной атриосептостомии, используют и с диагностической целью для измерения давления в левом желудочке, уточнения деталей анатомии порока и особенностей отхождения коронарных артерий. При выполнении коронарографии для более плотного заполнения артерий применяют баллонную окклюзию дистальной части восходящей аорты с инъекцией контрастного вещества в корень аорты. Несмотря на этот прием, оценка ангиограммы столь же трудна, как и интерпретация ЭхоКГ. В частности, трудно получить информацию о локализации коронарных устьев. Интрамуральные коронарные артерии, как правило, не диагностируются обоими методами, поэтому коронарография в настоящее время при ТМА не применяется.
Насыщение крови кислородом измеряют в верхней полой вене, аорте, легочной артерии и легочных венах. При условии измерения потребления кислорода можно рассчитать объем легочного и системного кровотока и эффективный легочный кровоток. В отличие от других пороков, насыщение в легочной артерии намного выше, чем в аорте. Крайне высокое насыщения крови кислородом в легочной артерии у больных с интактной межжелудочковой перегородкой является причиной малой артериовенозной разницы. Небольшие ошибки в измерениях существенно отражаются на расчетном объеме легочного кровотока. Ценность этих расчетов мало полезна еще и потому, что эффективный легочный кровоток обычно составляет менее 20% общего легочного кровотока. Это означает, что только небольшая часть общего легочного кровотока принимает участие в системной оксигенации.
В течение первых дней жизни у здоровых детей и больных с ИМЖП давление в желудочках и магистральных артериях одинаковое. После 48-72 ч жизни сопротивление легочных сосудов и давление в левом желудочке начинает снижаться, к 4-5-му дню становится равным 2/3 системного уровня и прогрессивно снижается в течение первого месяца жизни. У больных с нерестриктивным ДМЖП и/или персистирующим ОАП давление в левом желудочке остается равным системному. Легочная гипертензия отмечается также у некоторых больных с ИМЖП. Если операция артериального переключения не выполнена в первые недели жизни, рекомендуется выполнить катетеризацию для измерения давления в легочной артерии. Если оно окажется повышенным, необходимы строгие показания к коррекции.
Перед баллонной септостомией отмечается межпредсердный градиент давления в среднем около 10 мм рт. ст. После успешной процедуры он практически исчезает.
Если давление в левом желудочке у больных вне периода новорожденности превышает 2/3 системного, необходимо выяснить причину обструкции ангиографически. Это важно для выбора типа операции.
Естественное течение
Без хирургического лечения 30% младенцев умирают в течение первой недели жизни, 50% — в течение первого месяца, 70% — в течение 6 мес, 90% — до годовалого возраста от гипоксии, ацидоза, сердечной недостаточности. Выживаемость зависит от варианта порока.
Состояние больных с ИМЖП более тяжелое, чем с ДМЖП и ОАП: 80% переживают первую неделю жизни, ко второму месяцу живыми остаются 17%, к концу первого года — только 4% детей. Однако, после баллонной атриосептостомии по Rashkind наступает более радикальное улучшение, чем в группе с сопутствующими шунтовыми поражениями. У больных с простой ТМА имеется тенденция к развитию ОБЛС в более раннем возрасте, чем у пациентов с другими ВПС, поэтому хирургическая коррекция показана в раннем возрасте.
Больные с ДМЖП менее цианотичны, но у них имеется склонность к развитию застойной сердечной недостаточности и ОБЛС, которая возникает уже к 3-4 мес жизни; при этом к концу периода новорожденности выживают 91% младенцев, к 5 мес — 43%, к концу первого года жизни — 32% детей.
Динамика естественного течения детей с сопутствующим большим ОАП аналогична таковой при большом ДМЖП.
Аномалия Taussig-Bing физиологически аналогична ТМА-ДМЖП. Несмотря на это, естественное течение ее часто хуже из-за раннего развития ОБЛС и большой частоты сопутствующей системной обструкции. В то время как сужение выводного тракта левого желудочка при ТМА-ДМЖП играет защитную роль и обеспечивает 70% выживаемость больных к первому году и 29% — к 5 годам, наличие субаортального стеноза и обструкции дуги аорты резко ухудшает прогноз.
Сочетание ДМЖП с легочным стволом значительно удлиняет продолжительность жизни, однако хирургическая коррекция сопровождается более высоким риском.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания








Комментарии