Синдром гипоплазии левых отделов сердца: диагностика, лечение
Синдром гипоплазии левых отделов сердца в периоде новорожденности встречается у 9% детей и является самой частой причиной смерти от ВПС в течение первого месяца жизни.
Заболевание является комбинацией тесно связанных между собой аномалий, которая характеризуется гипоплазией левого желудочка, обусловленной атрезией или критическим стенозом аорты и митрального клапана, гипоплазией восходящей аорты и дуги.
Анатомия
Атрезия аортального клапана сочетается с гипоплазией восходящей аорты, средний диаметр которой у новорожденного составляет 2,5 мм; при стенозе аорты гипоплазия ее восходящей части менее выражена — диаметр составляет от 4 до 5 мм. Аортальная атрезия представлена отсутствующим или неперфорированным клапаном. Самым узким местом являются синусы аорты, представленные только устьями коронарных артерий. Атрезия аорты встречается также у новорожденных с аортолевожелудочковым туннелем.
В месте соединения боталлова протока с аортой имеется уступ, разделяющий кровоток из боталлова протока на антеградный — в нисходящую аорту — и ретроградный — в дугу и восходящую аорту, которая функционирует как единственная коронарная артерия. Боталлов проток широкий и представляет собой прямое продолжение легочного ствола в нисходящую аорту. Проток обычно левосторонний, однако в редких случаях сопутствующего предсердного изомеризма, ОАП может быть правосторонним.
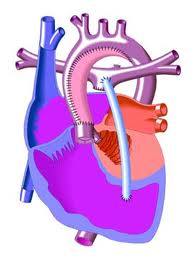
Левое предсердие имеет малые размеры, открытое овальное окно или ДМПП. Встречается пять вариантов морфологии межпредсердной перегородки:
-
недоразвитое или отсутствующее с рождения овальное окно;
-
первичный ДМПП как часть несбалансированной формы АВСД;
-
широко открытое овальное окно или вторичный ДМПП;
-
аневризма первичной перегородки;
-
аномальное прикрепление первичной перегородки прямо к задне-верхней части стенки левого предсердия далеко влево от вторичной перегородки.
У пациентов с атрезией митрального клапана и овального окна при отсутствии других путей для легочного венозного возврата развивается легочная лимфангиэктазия. Альтернативными путями для оттока венозной крови могут быть левая кардинальная вена — венозный канал, соединяющий легочные вены с системными, и фенестрация коронарного синуса — так называемый коронарный синус без «крыши». Часть легочных вен может открываться в правом предсердии, в коронарном синусе или системной вене. При свободном оттоке легочной венозной крови через аномальные пути из отдельной доли или сегмента легкого на рентгенограмме можно увидеть меньшую степень отека соответствующей части легкого.
Дефект межжелудочковой перегородки встречается у 10% больных, коарктация аорты — у 75%. Вариантами СГЛОС являются наличие сложных сопутствующих аномалий — несбалансированной формы АВСД, отхождения магистральных сосудов от правого желудочка с атрезией митрального клапана, трикуспидальной атрезии с ТМА, одножелудочкового сердца с атрезией аортального клапана. Все варианты требуют одинакового предоперационного ведения и встречаются в 30% всех случаев СГЛОС.
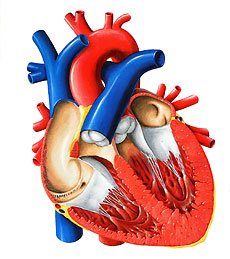
Атрезия аорты с нормальным левым желудочком. Левый желудочек нормальных размеров встречается у 2-7% больных с атрезией аорты. Как правило, имеются ДМЖП и митральный клапан. Дефект формируется в результате отсутствия соосности инфундибулярной перегородки и перегородочно-краевой трабекулы. В некоторых случаях ДМЖП образуется вследствие дефицита инфундибулярной перегородки без нарушения соосности. Размер митрального клапана приближается к нормальному. Левое предсердие развито лучше, чем у пациентов с гипоплазированным желудочком. В то же время аорта у этих больных гипоплазирована.
-
Атрезия аорты с АВСД.
Обычно левый желудочек мал, как при несбалансированной форме АВСД с доминирующим правым AV-отверстием, когда большая его часть связана с морфологически правым желудочком. Митральный компонент общего AV-отверстия сужен или атрезирован. Субаортальный вестибулум перекрыт аномально прикрепленной передней створкой митрального компонента общего отверстия и дополнительными тканями. Желудочковый компонент АВСД обычно мал, а межпредсердное сообщение нерестриктивное. Как и у пациентов с обычной формой СГЛОС, системный кровоток дуктусзависимый. В некоторых случаях имеются левопредсердный изомеризм и слезеночные аномалии.
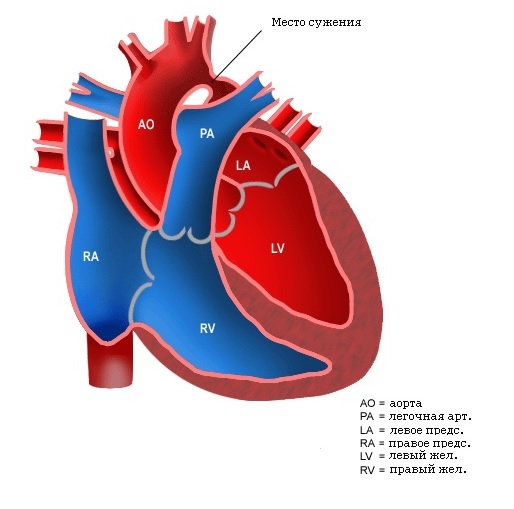
-
Атрезия аорты с ТМА.
При этой редкой аномалии имеются конкордантные AV-соотношения и дискордантные желудочко-артериальные соотношения. Правый желудочек недоразвит, инфундибулярный отдел гипоплазирован, с атрезией аортального клапана. Восходящая аорта заполняется через синусоиды миокарда правого желудочка и связанные с ними коронарные артерии. От морфологически левого желудочка отходит легочная артерия и широкий артериальный проток. Дефект межжелудочковой перегородки отсутствует.
Атрезия аорты с одножелудочковым сердцем встречается редко. Наиболее типичным вариантом является наличие единственного левого желудочка с инфундибулярной выпускной камерой и дискордантными транспонированными магистральными артериями. Бульбовентрикулярное отверстие облитерировано или минимальное. Системный кровоток дуктусзависимый. Инфундибулярная камера крошечная, а анатомически связанная с ней аорта атрезирована. Оба AV-клапана могут быть нормально сформированы и связаны с левым желудочком. Левое предсердие расширено, овальное окно небольшое. Один из AV-клапанов может быть атрезированным.
-
Атрезия аорты с корригированной ТМА.
При этой аномалии левый AV-клапан недоразвит и миокард свободной стенки анатомически правого желудочка истончен, как при аномалии Uhl.
Патофизиология
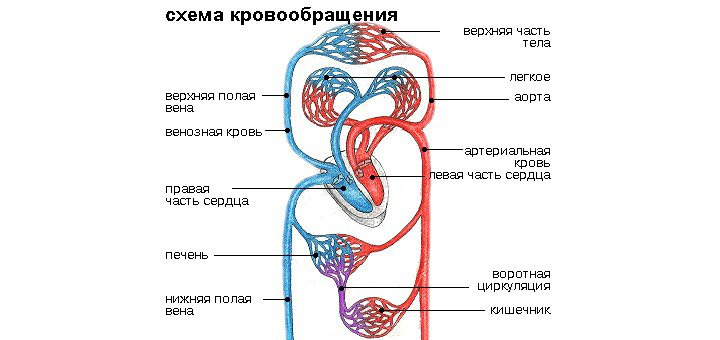
Синдром гипоплазии левых отделов сердца является одним из представителей группы пороков, имеющих гемодинамически единственный желудочек, патофизиология которых характеризуется смешиванием артериальной и венозной крови и параллельным кровообращением в большом и малом кругах. Системный кровоток дуктусзависимый, так как осуществляется только через боталлов проток.
Во внутриутробном периоде ЛСС превышает общее периферическое сопротивление. Преобладающий правый желудочек поддерживает нормальное перфузионное давление в нисходящей аорте и плаценте через ОАП. Проксимальная аорта, коронарные и мозговые сосуды кровоснабжаются ретроградно. В целом кровоснабжение всего организма плода не страдает.
После рождения при переходе на последовательное кровообращение порок становится несовместимым с жизнью из-за противоположно направленных изменений легочного и системного сопротивлений и закрытия ОАП. При этом резко снижается системный кровоток, развиваются циркуляторный шок и метаболический ацидоз.
Адекватность системного кровотока зависит от достаточных размеров ОАП, обеспечивающего системное кровообращение, и межпредсердного сообщения, через которое разгружается левое предсердие. При свободном оттоке артериализированной крови из левого предсердия не развивается отек легких, и насыщение артериальной крови кислородом превышает 80%. При интактной межпредсердной перегородке или при малом межпредсердном сообщении развиваются гипертензия в легочных венах и артериях с отеком легких и артериальной гипоксемией. Если ОАП остается открытым, жизнь ребенка зависит от благопрятного соотношения сосудистых сопротивлений легочного и системного кровотока. При СГЛОС развита гладкая мускулатура легочных артериол. Эти резистивные сосуды очень чувствительны к изменениям концентрации кислорода и величине артериального рН, поэтому искусственная вентиляция легких с повышенным содержанием О2, снижая рН и рСО2, нарушает баланс системного и легочного кровотока в пользу увеличения последнего. Вследствие этого гипоперфузия всего организма сопровождается объемной перегрузкой малого круга кровообращения. Частичное закрытие ОАП приводит к дальнейшему ухудшению кровоснабжения организма, а полное закрытие протока несовместимо с жизнью.
Клиника и диагностика
С первых часов и дней жизни новорожденные находятся в критическом состоянии. Характерны одышка, тахикардия, хрипы в легких, слабый периферический пульс, спазм периферических сосудов. Тяжелого цианоза может не быть.
Второй тон усилен и не расщеплен. Шумы сердца обычно отсутствуют, хотя иногда выслушивается негромкий неспецифический систолический шум выброса над всей предсердечной областью. Проявлением застойной сердечной недостаточности являются ритм галопа и гепатомегалия.
На ЭКГ почти всегда — признаки гипертрофии правого желудочка, изредка — гипертрофии левого желудочка. В отведениях V5 и V6 регистрируется высокий зубец R, отражающий дилатацию правого желудочка.
На рентгенограмме — признаки легочного венозного застоя или отека легких. Сердце расширено умеренно или значительно.
При исследовании газов артериальной крови обнаруживаются небольшое снижение рО2 при нормальном рСО2, метаболический ацидоз вследствие недостаточного объема системного кровотока.
Эхокардиография позволяет установить диагноз, однако для уточнения анатомических деталей необходимы катетеризация сердца и ангиокардиография. Полость левого желудочка резко уменьшена, в то время как правый желудочек расширен, трехстворчатый клапан широкий. Обнаруживается выраженная гипоплазия восходящей аорты и аортального кольца. Митральный клапан отсутствует или резко изменен. Часто встречаются сопутствующая коарктация аорты, ДМПП или открытое овальное окно с лево-правым сбросом. Иногда имеется ДМЖП с относительно большими левым желудочком, аортальным кольцом и восходящей аортой. С помощью цветной допплерографии обнаруживается ретроградный кровоток в дуге и восходящей аорте.
Принципиально важной является оценка размеров левого желудочка, исходя из которых определяют, какой тип вмешательства следует предпринять — одно- или двухжелудочковую коррекцию. Это решение может оказаться особенно трудным при наличии митрального и/или аортального стеноза. Задачу осложняют гемодинамические условия, косвенно свидетельствующие о приемлемых функциональных качествах левого желудочка: двухнаправленный кровоток через ОАП часто в сочетании с коарктацией аорты и лево-правый сброс через межпредсердный дефект. К числу важных критериев при определении адекватности размеров левого желудочка относятся наличие фиброэластоза эндокарда, соотношение размеров левого и правого желудочков и кольца митрального клапана.
Катетеризация сердца, кроме уточнения деталей анатомии с помощью ангиокардиографии, позволяет произвести специальные гемодинамические пробы, облегчающие принятие адекватного тактического решения. Пациенты, которые переносят баллонную окклюзию межпредсердной перегородки без значительного снижения насыщения кислородом смешанной венозной крови и без повышения давления в левом предсердии и имеют соотношение объемов легочного и системного кровотоков более 1, являются потенциальными кандидатами на двухжелудочковую коррекцию. К сожалению, не всегда удается точно измерить это соотношение у больных с антеградным кровотоком через левый желудочек. При атрезии аортального и митрального клапанов отмечается сброс крови слева направо на предсердном уровне и справа налево через ОАП. Насыщение системной венозной крови кислородом снижено, что указывает на уменьшенный объем системного кровотока и сердечную недостаточность. Насыщение крови в восходящей и нисходящей аорте соответствует таковому в легочной артерии, но не всегда. При наличии венозной обструкции возможно внутрилегочное шунтирование справа налево, и насыщение системной артериальной крови при этом ниже. В случаях, когда аортальный и митральный клапаны не атрезированы, артериальное насыщение выше. Артериальное насышение кислородом тем выше, чем больше соотношение объемов легочного и системного кровотока.

Давление в правых отделах сердца значительно повышено, в правом предсердии — из-за сердечной недостаточности. В правом желудочке и легочной артерии систолическое давление равно системному или превышает его. Это зависит от степени сужения артериального протока.
При катетеризации возможны эпизоды угрожающей брадикардии, когда катетер проходит через узкий боталлов проток или когда его ретроградно проводят в гипоплазированную восходящую аорту. В обоих случаях нарушается коронарный кровоток и возникает ишемия, проявляющаяся брадикардией. Сама по себе узкая восходящая аорта может создавать препятствие ретроградному коронарному кровотоку.
Давление в левом предсердии отражает адекватность межпредсердного сообщения. При минимальном дефекте прямое измерение давления в левом предсердии невозможно. Однако о его величине можно судить по давлению заклинивания легочных капилляров. Давление в левом предсердии отражает степень гипоплазии митрального и аортального клапанов и выраженность сердечной недостаточности.
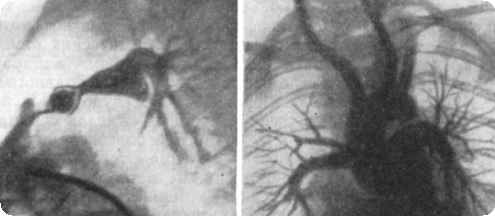
При ангиокардиографии селективное введение контрастного вещества в правый желудочек и легочный ствол позволяет диагностировать атрезию аорты при вторичном заполнении узкой восходящей аорты справа от легочного ствола. При проведении венозного катетера в ОАП и нисходящую аорту можно определить ее диаметр и наличие коарктации аорты, но только ретроградная аортография позволяет четко продемонстрировать восходящую аорту, оценить ее просвет и распределение коронарных артерий.
Восходящая аорта может быть разных размеров — от нормальных до крошечных. Обычно аорта начинает суживаться на уровне безымянной артерии. Реже просвет аорты имеет грушеобразную форму, суживаясь к брахиоцефальным сосудам.
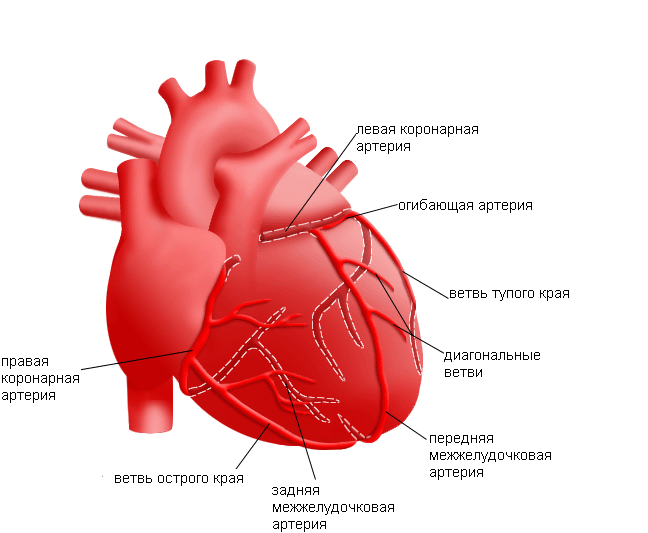
Прохождение коронарных артерий по эпикарду позволяет приблизительно оценить размеры левого желудочка, который ограничен пространством между передней нисходящей коронарной артерией и огибающей артерией. Идеальное заполнение восходящей аорты и коронарных артерий можно получить с помощью методики баллонной окклюзии аорты. Редко при СГЛОС обе коронарные артерии отходят от легочного ствола. Баллонная окклюзия аорты не приносит пользы для визуализации восходящей аорты при таких необычных вариантах, как окклюзия и перерыв дуги аорты. В этих случаях кровоток в восходящей аорте обеспечивается правосторонним боталловым протоком или открытым аортолегочным окном. Изредка источником кровоснабжения коронарной системы являются синусоиды в толще миокарда, соединяющие полость левого желудочка с коронарными артериями аналогично тому, как это наблюдается при атрезии легочной артерии с интактной межжелудочковой перегородкой.
В отличие от правого предсердия при атрезии легочной артерии или атрезии трехстворчатого клапана левое предсердие редко бывает расширенным. Обычно оно малых размеров и толстостенное. При атрезии митрального клапана дно левого предсердия плоское. При малом межпредсердном сообщении отмечается рефлюкс контрастного вещества в расширенные легочные вены. При левой атриографии может быть обнаружен дренирующийся в левое предсердие коронарный синус.
Дифференциальная диагностика СГЛОС
Дифференциальная диагностика СГЛОС и критического аортального стеноза часто бывает трудна и чрезвычайно важна для выбора соответствующей тактики лечения — бивентрикулярной коррекции или одножелудочковой гемодинамической коррекции. При обоих пороках полость левого желудочка уменьшена. Разными авторами были предложены различные критерии оценки степени гипоплазии левого желудочка: диаметр кольца митрального клапана, аортального клапана, восходящей аорты, размер полости левого желудочка. Бивентрикулярная коррекция не показана, если эти размеры составляют менее 60% средних величин при данной массе тела, а также, если верхушка сердца не образована левым желудочком. Leung и соавторы показали, что при критическом аортальном стенозе вальвулотомия опасна, если приточный размер по данным ЭхоКГ <25 мм, желудочково-аортальное соединение < 5 мм, а диаметр кольца митрального клапана < 9 мм. В детском госпитале Бостона разработаны свои индексы риска: площадь митрального клапана < 4,75 см2/м2, отношение размера левого желудочка по длинной оси к размеру сердца < 0,8, диаметр корня аорты < 3,5 см/м2, масса левого желудочка < 35 г/м2. Объем левого желудочка, равный 20 мл/м2, в этом центре считают достаточным для выполнения вальвулотомии.
Естественное течение
В течение первой недели жизни развиваются отек легких и застойная сердечная недостаточность. Больные умирают в период новорожденности от циркуляторного шока, прогрессирующей гипоксемии и ацидоза. Принципиально важное значение имеет дородовое эхокардиографическое исследование, которое позволяет заподозрить этот порок уже на 16-20-й неделе беременности и сразу после рождения транспортировать ребенка в специализированный центр. Иногда больных выписывают из роддома, не подозревая наличие порока. Это бывает при персистировании ОАП и благоприятном соотношении сопротивления большого и малого кругов кровообращения. Однако после выписки ОАП может быстро закрыться, что приводит к тяжелому метаболическому ацидозу, шоку, вторичным поражениям всех жизненно важных органов. Обратимость этих изменений зависит от тяжести ацидоза и его продолжительности. При условии своевременного начала введения простагландина можно выиграть время для транспортировки больного в хирургический центр.
Возможен другой вариант течения. При интактной перегородке или рестриктивном овальном окне затрудняется разгрузка левого предсердия. Это приводит к повышению левопредсердного давления, застою в легочном венозном и легочном артериальном русле, снижению объема легочного кровотока и увеличению системного кровотока. Однако такая ситуация не улучшает общего состояния пациента, так как при снижении легочного кровотока возникают цианоз и метаболический ацидоз в результате артериальной гипоксемии. Медикаментозное лечение не эффективно.
Дооперационное лечение
Синдром гипоплазии левых отделов сердца относится к группе пороков, хирургическое лечение которых сопровождается высокой степенью риска. Хотя выживаемость больных после первой стадии реконструкции во многих западных центрах достигла 90% и после последующих этапов по Fontan превысила 75%, определенную часть младенцев не направляют на хирургическое лечение. Родители родившихся в срок детей с установленным до родов диагнозом в 7-36% случаев отказались от лечения. Среди младенцев, которым предполагалось проводить лечение, у 14-21% имелись противопоказания к операциям.

Большинство больных прибывают для хирургического лечения из отделений интенсивной терапии новорожденных с эхокардиографическим диагнозом СГЛОС. При постановке анатомического диагноза очень важно также оценить функцию миокарда, проходимость ОАП и нарушение оттока легочной венозной крови. Когда эхокардиографическое исследование ввиду каких-либо обстоятельств недоступно, СГЛОС может быть заподозрен среди других причин развития коллапса кровообращения, слабого пульса, ацидоза. Следует исключить инфекционные факторы риска или лабораторные данные, указывающие на сепсис.
Целью предоперационного ведения новорожденных со СГЛОС является своевременная доставка пациента в операционную с хорошим сердечным выбросом, сохранной функцией всех органов и сбалансированным легочным и системным кровотоком. Некоторые больные, поступающие в кардиохирургическую клинику в состоянии шока, нуждаются в реанимационных действиях, другие требуют энергичной коррекции резко увеличенного легочного кровотока, реже возникает необходимость ургентного вмешательства для увеличения легочного кровотока путем декомпрессии левого предсердия.
Решающую роль в предоперационном ведении больных со СГЛОС играют несколько важных анатомических факторов. Снижение функции правого желудочка и сопутствующая недостаточность трехстворчатого клапана могут потребовать инотропной поддержки. Степень проходимости ОАП определяет дозировку ПГЕ1. Наличие аномального дренажа легочных вен может сопровождаться сдавлением вертикальной вены между ветвью легочной артерии и главным бронхом. Наконец, при интактной межпредсердной перегородке или рестриктивном дефекте требуется срочное выполнение септостомии или септэктомии. В то же время наличие широкого межпредсердного сообщения может привести к быстро прогрессирующему увеличению легочного кровотока и сердечной недостаточности.
-
Простагландин.
Сразу после возникновения подозрения на сложный ВПС необходимо быть готовыми начать инфузию ПГЕ1 и продолжать ее во время транспортировки. Лучше начинать инфузию ПГЕ1 уже в роддоме. При полностью открытом ОАП для стабилизации больного обычно достаточна доза 0,01-0,025 мкг/кг/мин. Для больных, поступивших со сниженным кровотоком через ОАП, необходимая начальная доза составляет 0,1 мкг/кг/мин. Детям более старшего возраста могут потребоваться большие дозы для открытия уже закрывшегося протока.
ПГЕ1 имеет два клинически значимых дозозависимых побочных эффекта. Это гипотензия, которая особенно неблагоприятна у больных, находящихся в шоке и требующих более высоких доз препарата, и апноэ. Сосудорасширяющий эффект ПГЕ1 можно компенсировать инфузией жидкости 10-20 мл/кг и малых доз допамина. Кетамин поддерживает системное давление крови и хорошо переносится дооперационными больными со СГЛОС. Фентанил или морфин титруют до получения эффекта. Для обеспечения адекватной вентиляции следует устранить ригидность грудной клетки нейромышечной блокадой. Преоксигенация 50-100% кислородом в течение нескольких минут хорошо переносится больными без существенной гипотензии, несмотря на то, что кислород является легочным вазодилататором, способным увеличить легочный кровоток за счет системной перфузии. Показан режим нормовентиляции. Гипервентиляция может нарушить соотношение легочного и системного кровотока в пользу первого.
-
Кислород.

На дооперационном этапе у детей со СГЛОС следует избегать применения кислорода, так как он повышает соотношение Qл/Qc. Необходимость применения кислорода может возникнуть при наличии легочной патологии или рестриктивного ДМПП. При отсутствии этих обстоятельств у большинства младенцев с СГЛОС на дохирургическом этапе легочный кровоток увеличен и насыщение артериальной крови кислородом при дыхании комнатным воздухом составляет 88-95%. Более низкое насыщение требует тщательной оценки. Хотя имеется соблазн назначения ингаляции кислорода, когда снижение SaO2 отражает гипоперфузию большого круга кровообращения при высоком Qл/Qc, добавление кислорода в дыхательную смесь может снизить SаО2 еще больше.
-
Инотропная поддержка.
Больным со сниженной функцией правого желудочка показана инфузия допамина или других кардиотонических средств. Следует предостеречь от введения больших доз допамина или иных инотропных средств, обладающих системным сосудосуживающим действием, так как это может увеличить соотношение Qл/Qc.
Милринон снижает как легочное, так и периферическое сосудистое сопротивление после операции у детей. Добутамин снижает в большей степени сопротивление системных артерий, чем легочных. В литературе отсутствуют сведения о действии этих препаратов на сосудистое сопротивление легочных и системных артерий у младенцев с СГЛОС, поэтому их следует применять с осторожностью из-за непредсказуемого действия на Qл/Qc.
При назначении симпатомиметиков следует удовлетворяться минимально допустимыми показателями достаточности системного кровотока: небольшим дефицитом оснований, небольшой концентрацией лактата и умеренной гипотензией. Малые дозы допамина оказывают минимальное действие на Qл/Qc, но увеличивают минутный объем сердца, доставку кислорода и уменьшают степень гипотензии.
-
Коррекция ацидоза.
У дооперационных больных со СГЛОС введение щелочных растворов следует проводить с осторожностью, так как они могут снижать ЛСС и увеличивать Qл/Qc, тем самым уменьшая системный кровоток и способствуя усилению системного ацидоза. Однако больные, находящиеся в шоке и глубоком метаболическом ацидозе, нуждаются в коррекции дефицита оснований. При введении оснований следует добиваться оптимизации Qл/Qc. Недоношенным младенцам щелочные растворы необходимо вводить медленно во избежание кровоизлияния в мозг.

Антибиотики назначают уже в роддоме при наличии факторов риска инфекции и продолжают их введение в течение 48-72 ч, т.е. до тех пор, пока посевы, сделанные до начала терапии, не окажутся отрицательными. При отсутствии факторов риска антибиотики не назначают.
-
Рестриктивное межпредсердное сообщение.
Сбалансированность кровотока по большому и малому кругам кровообращения, обусловливающая относительное благополучие ребенка со СГЛОС, или исключительная тяжесть состояния с глубокой гипоксемией, гипотензией и полной обструкцией легочного венозного возврата зависят от степени ограничения тока крови через ДМПП и выраженности гипоплазии левого желудочка. Интактная межпредсердная перегородка с наличием разгружающей вертикальной вены или без нее встречается у 6% пациентов. Результаты лечения таких больных неудовлетворительные.
Трудность лечения определяется необходимостью организации целенаправленных ургентных действий сразу после рождения, поэтому очень важны пренатальная диагностика и родоразрешение в заранее выбранной больнице, в которой есть отделение кардиохирургии или лаборатория катетеризации сердца. Ребенок должен быть интубирован в родзале, и здесь же следует начинать введение ПГЕ1 через пупочную вену. Ребенка сразу транспортируют в кардиохирургическую операционную или лабораторию катетеризации для выполнения декомпрессии левого предсердия путем септэктомии, процедуры Рашкинда или стентирования вертикальной вены.

При отсутствии дородового диагноза больному клинически может быть ошибочно поставлен диагноз обструктивного ТАДЛВ. Тактика реанимационных действий при обеих аномалиях сходна: интубация, положительное давление на выдохе, при показаниях — кислород, инотропная поддержка, восполнение объема жидкости и оснований. Однако есть существенные отличия в интервенционных действиях, которые и определяют исход лечения. Поэтому при клинической картине легочно-венозной обструкции крайне необходимо экстренное эхокардиографическое обследование. При обструкции легочно-венозного возврата в критических ситуациях используют венозно-артериальную ЭКМО или корригирующее хирургическое лечение. При СГЛОС с интактной межпредсердной перегородкой состояние больных можно стабилизировать, только выполнив септэктомию или паллиативную операцию по Norwood. ЭКМО при СГЛОС требует осуществления трансторакальной канюляции с лигированием ОАП.
Предоперационное обследование
Предоперационное обследование в кардиохирургической клинике проводится в порядке подготовки к экстренной операции. Исследуют газы крови, электролиты, ионизированный кальций и глюкозу. Рентгенограмма грудной клетки позволяет определить правильность расположении эндотрахеальной трубки, желудочного зонда и рентгеноконтрастного венозного катетера. Обычно отмечаются умеренное увеличение размеров сердца и признаки увеличенного легочного кровотока. Легочно-венозный застой является признаком рестриктивного межпредсердного сообщения или аномального дренажа легочных вен с обструкцией.
Физикальное обследование направлено на оценку состояния кровообращения. Слабый периферический пульс свидетельствует об избыточном легочном кровотоке или небольшом ОАП. Одышка указывает на застой в легких. Аускультация обычно не обнаруживает отклонений от нормы, за исключением нерасщепленного II тона. При выраженной гепатоспленомегалии может выслушиваться систолический шум трикуспидальной недостаточности.
У новорожденных с недостаточной системной перфузией и ацидозом необходимо оценить функцию внутренних органов. При гипоксическом повреждении печени:
-
повышается концентрация печеночных ферментов;
-
снижаются уровень сывороточного альбумина;
-
протромбиновый индекс;
-
возрастает уровень аммиака.
Функция печени чаще всего восстанавливается, однако иногда развивается скоротечная печеночная недостаточность. Нормализация функции печени является одним из условий для выполнения первой стадии хирургического лечения порока. Это же относится к дисфункции почек, проявляющейся повышением уровня азота мочевины и креатинина. В этих случаях уместно ультразвуковое исследование почек.
У всех недоношенных и поступивших в состоянии шока необходимо исключить мозговое кровоизлияние с помощью ультразвукового исследования головы. Оно показано также у стабильных детей с сопутствующей врожденной патологией, особенно при микроцефалии. При обнаружении аномалий рутинно выполняют компьютерную томографию. Оптимальная хирургическая тактика у детей с кровоизлияниями в мозг не выработана.
Риск, связанный с гепаринизацией и остановкой кровообращения, превышает риск отсрочки операции и чрезмерного увеличения легочного кровотока. В ведущих кардиохирургических центрах мира операцию откладывают на 1-3 дня.
У детей со СГЛОС высока вероятность развития некротического энтероколита. Пациенты с молочнокислым ацидозом, расширенными петлями кишечника, примесью крови в стуле и тромбоцитопенией должны быть обследованы рентгенографически на наличие пневмотоза или свободного воздуха в брюшной полости. Если позволяют гемодинамические условия, пациентам с клинически выраженным некротическим энтероколитом назначают 7-10-дневный курс трех антибиотиков для смягчения последствий ишемических и реперфузионных повреждений кишечника, связанных с искусственным кровообращением. Этот курс следует сократить, если у больного определяется значительный дисбаланс между легочным и системным кровотоком, который может еще больше ухудшить перфузию кишечника. Больных, перенесших ургентное вмешательство в связи с некротическим энтероколитом, приходится оперировать по поводу основного заболевания до истечения нормального периода восстановления после абдоминальной операции.

Предоперационное ведение
Если принять, что у больного со СГЛОС минутный объем сердца в норме, насыщение смешанной венозной крови равно 60% и при отсутствии легочной патологии насыщение легочной венозной крови равно 100%, то насыщение системной артериальной крови кислородом, равное 80%, при соотношении Qp/Qs будет равно 1. У больнго с более высоким насыщением венозной крови соотношение Qp/Qs будет составлять 1, если SaO2 составит 87,5%. Очевидно, что при SaO2 > 90% соотношение Qp/Qs >1. К сожалению, SaO2 80% не всегда свидетельствует о том, что кровоток в большом и малом кругах кровообращения одинаков. У больных с небольшим минутным объемом и SvO2 30%, SpvO2 100% и SaO2 80%, соотношение легочного и системного кровотока Qp/Qs составляет 2,5/1, с клинически значимой легочной гиперволемией и большой артериовенозной разницей по кислороду.
У кардиохирургических больных обычно мониторируют SvO2. В венозной системе младенцев со СГЛОС нет места, где бы можно было измерить истинное SvO2. Правое предсердие и легочная артерия содержат смешанную легочную и системную венозную кровь. Считается, что кровь из верхней полой вены с максимальным приближением отражает SvO2. Хотя верхняя полая вена является лучшим местом забора проб смешанной венозной крови, длительное нахождение в ней катетера может привести к ее тромбозу и невозможности выполнения двунаправленного кавопульмонального анастомоза Glenn или паллиативной операции hemi-Fontan.
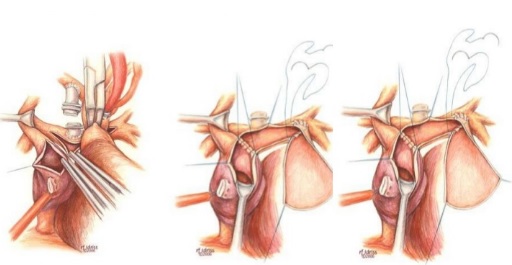
Варианты клинического течения и терапевтическая тактика
Клинически стабильные младенцы до операции могут переносить увеличенный легочный кровоток достаточно продолжительное время. Если диагноз поставлен рано, своевременное начало инфузии ПГЕ1 позволяет избежать ацидоза и интубации трахеи. Относительное благополучие обусловлено оптимальными размерами межпредсердного сообщения, что обеспечивает баланс Qp/Qs. Хотя частота дыхания достигает 60-80 в минуту, а SaO2 может превысить 90% при РаО2 40-50 мм рт. ст., они остаются клинически стабильными при минимальном вмешательстве. В этой группе пациентов несмотря на увеличенный легочный кровоток сохраняется адекватная системная перфузия.
Другая группа младенцев со СГЛОС нуждается в интенсивной регуляции баланса легочного и системного кровотока. К ним относятся больные, поступившие в клинику в состоянии шока в результате поздней диагностики, а также пациенты с клинически выраженной легочной гиперволемией, независимой от времени постановки диагноза.
У больных с поздним диагнозом может развиться кардиогенный шок, обусловленный одной из следующих причин:
-
наличием рестриктивного межпредсердного сообщения с застоем крови в легочных венах;
-
прекращением системного и коронарного кровотока из-за частичного или полного закрытия ОАП;
-
недостаточной системной перфузией, вызванной чрезмерным легочным кровотоком при открытом ОАП.
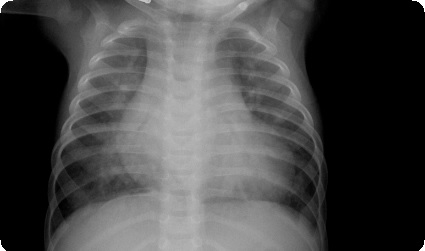
Часто этих детей выписывают из роддома без диагноза, в состоянии видимого благополучия, но вскоре они поступают в реанимационное отделение с одышкой, холодными конечностями и другими признаками недостаточности периферического кровообращения. Обычно у этой когорты пациентов имеет место нерестриктивный ДМПП. Из-за тяжести состояния их не выписывали из стационара и ошибочно назначали лечение кислородом и гипервентиляцией до постановки точного диагноза. Вне зависимости от этиологии шока у больных часто снижена функция желудочка, сопровождающаяся трикуспидальной недостаточностью и увеличением печени, тяжелым метаболическим ацидозом, печеночно-почечной недостаточностью, а также ишемией кишечника и диссеминированной внутрисосудистой коагулопатией.
Такие больные требуют быстрой и агрессивной реанимации. Необходимо начинать с инфузии ПГЕ1 в дозе, соответствующей степени проходимости ОАП. Для увеличения общего сердечного выброса вводят допамин в дозе 5 мкг/кг/мин. Седация, релаксация и интубация трахеи позволяют контролировать вентиляцию и минимизировать потребление кислорода. Если вентиляция комнатным воздухом сопровождается неприемлемо увеличенным легочным кровотоком, в дыхательную смесь добавляют СО2 для улучшения доставки кислорода в ткани. Функции всех внутренних органов должны быть восстановлены до операции. Если, несмотря на реанимационные усилия, сохраняется метаболический ацидоз, необходимо проверить проходимость ОАП с помощью ЭхоКГ. При устойчивой к лечению выраженной легочной гиперволемии прибегают к безотлагательной хирургической реконструкции.
Следовательно, если у больного, который находится на самостоятельном дыхании в условиях гипоксии, наступит кратковременное апноэ, например в связи с инфузией ПГЕ1, может наступить преходящее повышение РаСО2 до 70 мм рт. ст. При этом альвеолярное РАО2 станет равным 34 мм рт. ст. Парциальное давление системной артериальной крови РаО2 определяется смешанным венозным и альвеолярным РАО2. Таким образом, в условиях дыхания гипоксической газовой смесью и умеренного дыхательного ацидоза может возникнуть выраженная системная гипоксия.
У детей, находящихся на искусственной вентиляции, повышение концентрации вдыхаемого СО2 улучшает доставку кислорода, однако у пациентов, находящихся на спонтанном дыхании, этот механизм еще не доказан. Повышение парциального давления СО2 увеличивает потребление кислорода и вызывает тахипноэ, что потенциально может нивелировать ожидаемый положительный эффект.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания









Комментарии