Первичная легочная артериальная гипертензия. Синдром Эйзенменгера у детей
Хотя первичная ЛГ не имеет прямого отношения к ВПС, дети с этой патологией иногда поступают в кардиохирургические клиники для дифференциальной диагностики. Специалистам многократно встречались пациенты с тяжелой формой ЛГ, которую нельзя было связать с незначимыми сопутствующими ВПС. Кардиохирурги вынуждены брать на себя консультативную помощь в вопросах не только диагностики, но и терапевтического лечения этого тяжелого контингента пациентов.
Первое сообщение о семейной первичной ЛГ было сделано в 1927 г.. Clarke и соавторы описали клинику и морфологические находки на аутопсии первичной ЛГ у сестер 5- и 8-летнего возраста. Однако Dresdale и соавторы первыми показали семейную передачу заболевания от одного поколения к следующему. Они описали историю болезни семьи, в которой женщина и ее сын умерли от первичной ЛГ соответственно в возрасте 43 года и 21 год. Кроме того, у нее в раннем детстве умер брат и сестра в возрасте 31 года от правожелудочковой недостаточности, вероятно, вследствие первичной ЛГ. Эти ранние клинические описания содержали много теперь хорошо установленных фактов наследственной семейной первичной ЛГ, включая вертикальную трансмиссию, генетическое предвидение и любопытное наблюдение, что в семье клиническое течение заболевания у лиц мужского пола более тяжелое и они умирают в более молодом возрасте, чем лица женского пола.
Частота семейной первичной ЛГ составляет 1-2 случая на 1 млн населения и 6% – в регистре ЛГ различной этиологии США, хотя есть основания считать, что достаточно много случаев не учтено. Семейная первичная ЛГ отличается от спорадической формы более ранним диагнозом после появления первых симптомов. Однако она не отличается от спорадической ни клинически, ни по соотношению женщин и мужчин – 2:1 среди взрослых и 1,3:1 в детском возрасте.
Семейная первичная ЛГ передается вертикально. Так, известна семья, в которой 5 поколений страдали этим заболеванием. Оно может передаваться от мужчины к мужчине, однако в Торонто в детской клинике по лечению ЛГ зарегистрирован случай, когда у здорового отца родились две дочери с первичной ЛГ от разных матерей. Этот пример трансмиссии исключает Х-связку генов и с высокой долей вероятности предполагает наличие аутосомального доминантного гена.
Гистология
Гистологические особенности семейной легочной артериопатии гетерогенны и часто сочетают тромботические и плексиформные поражения. Гистологически семейная, спорадическая первичная ЛГ и комплекс Эйзенменгера неотличимы. Lee и соавторы показали, что плексиформные поражения легочных сосудов при семейной первичной ЛГ содержат моноклонально пролиферирующие эндотелиальные клетки в противоположность поликлональной пролиферации эндотелиальных клеток при вторичной ЛГ. Наличие моноклональной пролиферации эндотелиальных клеток при первичной ЛГ показывает, что повреждение соматического гена, подобно таковому при неопластических процессах, может способствовать клональной экспансии легочных эндотелиальных клеток. При первичной ЛГ при гистологическом исследовании иногда обнаруживают окклюзию легочных венозных микрососудов и капиллярный гемангиоматоз.
Клиника
Этиология первичной легочной артериальной гипертензии неизвестна. Она поражает преимущественно молодых людей, и течение заболевания неумолимо фатально, хотя зафиксированы отдельные случаи спонтанной регрессии. Диагноз устанавливается уже в раннем возрасте обычно в далеко зашедших стадиях заболевания. Средняя продолжительность жизни составляет 4 года. Важной детерминантой выживания является функция правого желудочка. Жизненный прогноз лучше у пациентов с давлением в правом предсердии менее 7 мм рт. ст. Плохим предвестником является низкое насыщение кислородом смешанной венозной крови. У детей ответ на сосудорасширяющие препараты лучше, чем у взрослых. Положительный гемодинамический эффект лечения улучшает прогноз, но не у всех. По данным биопсии легких у детей более выражена гипертрофия медии, объясняющая склонность к вазоконстрикции, и менее выражены ангиоматозные изменения и фиброз интимы.
Легочная сосудистая гипертензия при отсутствии внутрисердечных шунтов плохо диагностируется в детском возрасте, так как объективные симптомы выражены не резко. Наиболее типичными признаками являются:
-
одышка;
-
обмороки или полуобморочные состояния;
-
генерализованные судороги;
-
вялость;
-
сердцебиение или цианоз при нагрузке;
-
отеки на ногах.
Всегда отмечается непереносимость нагрузок. Боли в сердце для детей нетипичны, в отличие от взрослых. Однако ишемия миокарда может проявляться и у детей, когда давление в легочной артерии превышает системное, а также при нагрузке.
На рентгенограмме грудной клетки видны характерные признаки ЛГ:
-
расширение сердечной тени;
-
выбухание второй дуги по левому краю сердца;
-
расширение проксимальных легочных артерий с «обрубленными» периферическими ветвями.
На электрокардиограмме определяется гипертрофия правого предсердия и желудочка с признаками перегрузки у 70-80% пациентов.
Эхокардиография позволяет диагностировать повышение давления в правом желудочке, отсутствие патологии митрального клапана и легочных вен, а также отсутствие других вероятных причин правожелудочковой гипертензии – подклапанного, клапанного и надклапанного стенозов легочной артерии. Наличие узких проксимальных легочных артерий с постоянным дистальным кровотоком при допплер-кардиографическом исследовании указывает на множественные обструкции периферических легочных артерий. Должны быть также исключены экстра- и интракардиальные шунты.
Катетеризация сердца и ангиокардиография являются важнейшими исследованиями для установления правильного диагноза.
Лечение первичной ЛГ
До последнего 10-летия общепринятая терапия носила в основном симптоматический характер и ограничивалась назначением дигоксина, диуретиков, блокаторов кальциевых каналов и антикоагулянтов. Однако последние достижения сосудистой биологии и молекулярной генетики быстро внедряются в практику в виде этиопатогенетически обоснованного лечения.
Блокаторы кальциевых каналов
В 1992 г. Rich и соавторы показали, что большие дозы блокаторов кальциевых каналов снижают давление в легочной артерии и сопротивление более чем на 20% у 26% пациентов с первичной ЛГ. При пероральном приеме нифедипина или дилтиазема у больных отмечены 94% выживаемость в течение 5 лет и признаки регрессии гипертрофии правого желудочка, улучшение толерантности к нагрузке и качества жизни. Однако у той части испытуемых, у которых снижение ЛСС не сопровождалось снижением давление в легочной артерии, уменьшения симптомов при длительной терапии не отмечалось. Отмечено, что блокаторы кальциевых каналов могут усилить правожелудочковую недостаточность и должны назначаться с осторожностью. Блокаторы кальциевых каналов эффективны только у небольшой части пациентов и вытеснены более новыми лекарственными средствами.
Вазоктивные медиаторы и фармакологическое лечение
Как упоминалось выше, простациклин является эндогенным вазоактивным медиатором, который способствует вазодилатации, угнетению агрегации тромбоцитов и пролиферации гладкой мускулатуры сосудов. Тромбоксан оказывает противоположное действие и ухудшает течение болезни легочных сосудов. Соотношение простациклина к тромбоксану снижено при первичной ЛГ, комплексе Эйзенменгера и у детей с лево-правым внутрисердечным шунтом и возвращается к норме после успешной коррекции порока.
Пролонгированная инфузия простоциклина
Higenbottam и соавторы первыми сообщили о положительном эффекте продолжительной инфузии простоциклина у больных с первичной ЛГ. Было отмечено улучшение самочувствия, переносимости физических нагрузок и выживаемости. Впоследствии эти результаты были подтверждены другими исследованиями. Годичная выживаемость больных, ожидающих трансплантацию сердца и легких, увеличилась на 66%. Интересно, что при 2-летнем проведении такого лечения не отмечено преимуществ перед общепринятой терапией, за исключением более тяжелых стадий заболевания. У этих пациентов длительный эффект не был связан с вазодилатацией, которая отмечается в начале курса пролонгированной инфузии простоциклина. Эффект объясняется иными, чем вазодилатация, механизмами, а именно – угнетением агрегации тромбоцитов и ремоделированием сосудистой стенки.
Побочное действие в виде головной боли, покраснение кожи и боли в животе обычно преходящее, продолжается в течение 24 ч, однако может вновь проявиться при увеличении дозы.
Осложнения связаны главным образом с длительно стоящим венозным катетером, неисправностью насоса. В среднем у пациента возникают два эпизода сепсиса в год. При прерывании инфузии могут возникнуть одышка и потеря сознания. Со временем потребность в простациклине и необходимость коррекции дозы для поддержания нормального сердечного выброса возрастает. Тем не менее, пролонгированное внутривенное введение простоциклина значительно улучшает выживаемость в течение 1, 2 и 3 лет и составляет 88%, 76% и 63% соответственно, что значительно лучше, чем в контроле.
Ведущими факторами, определяющими выживаемость больных, являются:
-
переносимость физических нагрузок;
-
функциональный класс МУНА;
-
давление в правом предсердии;
-
непосредственный сосудорасширяющий ответ на аденозин или ингаляционный NО.
После годичного лечения дополнительными прогностическими факторами становятся сердечный выброс и среднее давление в легочной артерии.
Постоянное внутривенное введение простоциклина революционизировало хроническое лечение ЛГ. Однако приведенные выше недостатки и осложнения особенно обременительны при лечении детей. Неудивительно, что многие пациенты неохотно принимают решение о таком лечении. Это стимулирует поиск альтернативных методов введения простоциклина – аэрозолей, оральных или подкожных аналогов. Берапрост является оральным активным аналогом простоциклина, который оказался эффективным как при краткосрочном, так и при длительном лечении ЛГ. Эффективность орального аналога является сравнимой с эффективностью внутривенного введения простоциклина и также сохраняется в течение 1 года. Побочные реакции – покраснение лица, артралгия, мышечные боли, тошнота или понос – отмечались достаточно часто, однако тяжелые осложнения, связанные с катетером, были исключены.
Ингаляционная форма простоциклина в виде аэрозоля по эффективности сравнима с ингаляционным NО, однако их комбинация не дает дополнительного ответа. Более благоприятным является сочетание ингаляционного илопроста с оральными препаратами, такими, как босентан или силденафил.
Исследования последних лет открыли перспективную альтернативу постоянному внутривенному введению простоциклина при ЛГ. Перемещение гена синтазы человеческого простоциклина в печень крыс с вызванной монокроталином ЛГ позволило добиться высокого уровня экспрессии гена синтазы простоциклина в гепатоцитах печени животных. В результате давление в легочной артерии снизилось с 88% до 60% по отношению к системному, а содержание ЭТ-1 в легочной ткани снизилось в 2 раза по сравнению с контролем. Выживаемость животных значительно увеличилась.
Ингаляционный NO
Ингаляционный N0 является мгновенно действующим селективным легочным вазодилататором, который улучшает фракцию внутрилегочного шунтирования и имеет короткий период полураспада. Он идеально подходит для выполнения функциональных проб при катетеризации и у новорожденных с персистирующей ЛГ, находящихся на искусственной вентиляции легких в отделениях интенсивной терапии, а также у детей после операций по поводу ВПС. Следует отметить, что, несмотря на оксидативный стресс, проявляющийся повышенной пероксидацией липидов у пациентов с ЛГ, ингаляционный NО не способствует дальнейшему увеличению образования пероксинитритов. Оксид азота стал методом выбора при лечении легочных гипертонических кризов в педиатрической кардиохирургии. Однако серьезные технические сложности ограничивают его практическое применение для продолжительного лечения больных с хронической ЛГ.

Силденафил
Силденафил – селективный ингибитор V-фосфодиэстеразы, которая является ферментом деградации цГМФ и тем самым ограничивает опосредованную NО вазодилатацию. Хорошо известен эффект угнетения фосфодиэстеразы на сосуды пениса и его использование для лечения эректильной дисфункции. Известно также, что в легочных сосудах имеются высокие концентрации энзима V типа. Предварительные сообщения показали, что силденафил может оказать сосудорасширяющее действие при ЛГ, в частности, ослабить острый подъем давления в легочной артерии после прекращения ингаляции NО, а также может применяться в качестве препарата для лечения хронической ЛГ. Прием силденафила внутрь устраняет гипоксическую легочную вазоконстрикцию у людей. Силденафил хорошо переносится, доступен как оральный препарат и может стать альтернативой простациклину, особенно для пациентов, чья симптоматика не оправдывает постоянную внутривенную инфузию. Силденафил может выступать в качестве адъювантного препарата при лечении ингаляционным простоциклином или в сочетании с постоянным ингаляционным NО. Силденафил вызывает быструю и относительно селективную легочную вазодилатацию, которая удерживается достаточно продолжительное время. Синергическое и дополнительное к простоциклину действие обусловлено повышением содержания цАМФ и цГМФ. Интересно, что ингаляционный силденафил в эксперименте на животных уменьшает внутрилегочное шунтирование, а оральный силденафил уменьшает внутрилегочное шунтирование у больных с фиброзом легких и вторичной ЛГ. Силденафил является селективным легочным вазодилататором, в противоположность другим внутривенным и оральным препаратам того же назначения.
Блокада рецепторов ЭТ
Эндотелин является мощным вазоконстриктором, способствующим пролиферации гладкой мускулатуры сосудов. Есть данные о том, что аномально высокий уровень циркулирующего ЭТ углубляет сосудистые нарушения в легких. Повышенный уровень ЭТ, сопровождающийся снижением синтеза NO, причастен к патофизиологии ЛГ, возникающей после искусственного кровообращения, персистирующей ЛГ новорожденных и синдрому Эйзенменгера. Постоянная терапия простоциклином у пациентов с первичной ЛГ улучшает легочный клиренс ЭТ вместе с гемодинамическими и клиническими параметрами. Действие ЭТ опосредуется через рецепторы двух типов – ЭТА и ЭТВ. ЭТА представлен на гладкомышечных клетках и опосредует вазоконстрикцию и пролиферацию, в то время как ЭТВ-рецептор находится преимущественно на эндотелиальных клетках. Когда ЭТ связывается с ЭТВ-рецептором, он вызывает вазорелаксацию через освобождение NO и простоциклина. Это объясняет парадокс, обнаруженный в ранних работах, в которых инфузия ЭТ здоровым млекопитающим вызывала легочную вазодилатацию даже в дозах, которые обычно приводят к системной вазоконстрикции. Эти данные привели к мысли о важной роли эндотелиальных клеток в поддержании легочного сосудистого гомеостаза. Возможно, в поврежденном легочном сосудистом русле рецепторы ЭТА преобладают. Пока остается неясным, следует воздействовать фармакологическими средствами на рецепторы ЭТА или ЭТВ. Неселективная блокада рецепторов ЭТ может снизить положительные эффекты ЭТВ. Однако наиболее обещающий блокатор рецепторов ЭТ воздействует на оба типа рецепторов. Внутривенное введение босентана снижает давление в легочной артерии и сопротивление у пациентов с первичной ЛГ, но этот эффект не селективный. Несмотря на неселективное действие внутривенного босентана, таблетированная форма препарата в двух плацебо-контролированных исследованиях у пациентов с первичной и вторичной ЛГ, обусловленной склеродермией, улучшала физическую работоспособность, гемодинамику и смягчала симптомы.
Кроме сосудорасширяющего действия, босентан подавляет развитие фиброза и пролиферации. Его использование способствует увеличению продолжительности жизни. Согласно опубликованным в 2005 г. данным, 86% пациентов, получавших босентан, пережили 3-летний период, в группе сравнения – 48%. Преимуществом препарата является также его оральное применение, исключающее трудности и осложнения парентерального введения.
Препарат хорошо переносится, не оказывает побочного действия, за исключением дозозависимого повышения уровня легочных ферментов, который снижался до нормы через 2-6 нед. после его отмены.
Антикоагулянты
Наблюдение за группой пациентов в течение 15 лет показало лучшую выживаемость больных, получавших варфарин, в сравнении с теми, кто его не получал. Имеются гистологические доказательства роли тромбоза сосудов при первичной ЛГ.
Ножевая атриосептостомия
Известен факт, что пациенты с синдромом Эйзенменгера и открытым овальным окном живут дольше, чем пациенты с интактной межпредсердной перегородкой. Принимая во внимание это наблюдение, ряд кардиологов сообщили о выполняемой ими ножевой септостомии у больных с тяжелыми формами ЛГ.
Исследования на животных и опыт операций Fontan с фенестрацией венозного канала показывают, что межпредсердное сообщение обеспечивает декомпрессию перегруженных правых отделов сердца и поддержание сердечного выброса ценой падения артериального насыщения кислородом, одновременно с улучшением системной доставки кислорода и уменьшением симптомов правожелудочковой недостаточности. Ножевая атриосептостомия увеличивает сердечный выброс и системный транспорт кислорода, несмотря на падение насыщения кислородом артериальной крови. Выживаемость в течение 1,2 и 3 лет была 80%, 73% и 65% соответственно, что значительно лучше в сравнении с кривой предсказанной выживаемости, построенной по уравнению, разработанному на основании регистра первичной ЛГ Нью-Йоркской ассоциацией кардиологов.

Ножевая атриосептостомия улучшает состояние больных с обморочными состояниями. Процедура сопряжена с некоторым риском. Для предупреждения ранней летальности в периоперационном периоде рекомендуются объемная нагрузка, повышение гематокрита и инотропная поддержка. С технической точки зрения более безопасна постепенная, в несколько приёмов, баллонная дилятация септостомии.
Трансплантация легких
Несмотря на достижения в понимании ЛГ, трансплантация легких является последним средством для пациентов, исчерпавших возможности лечения. Количество детей, перенесших трансплантацию, пока невелико. Выживаемость детей в течение года составляет 73%. Смертность после трансплантации обусловлена четырьмя факторами:
-
цитомегаловирусной инфекцией;
-
облитерирующим бронхиолитом;
-
посттрансплантационной лимфопролиферативной болезнью;
-
стенозами бронхов.
Десятилетняя выживаемость у детей составляет 30-40%.
Время трансплантации остается неоднозначным. При эффективной медикаментозной терапии придерживаются выжидательной тактики. Показаниями к трансплантации являются правожелудочковая недостаточность или IV класс по МУНА, когда ожидаемая продолжительность жизни – менее 6 мес. Отсутствие эффекта от вазодилатационной терапии, супрасистемное давление в легочной артерии, обмороки или низкий сердечный выброс являются сигналами для трансплантационной бригады. Разработаны также простые количественные гемодинамические критерии выживаемости при естественном течении заболевания. Если среднее давление в правом предсердии, умноженное на индекс ЛСС, меньше 160, выживаемость лучше, чем после трансплантации легких.
Персистирующая ЛГ у новорожденных
Персистирующая легочная гипертензия новорожденных встречается у 1 из 1500 родившихся живыми и характеризуется сохраняющейся ЛГ и цианозом из-за право-левого шунта через ОАП или открытое овальное окно. Порок сердца отсутствует.
Причины возникновения ПЛГН разделяют на 3 группы в зависимости от структуры легочного сосудистого русла:
-
Выраженная легочная вазоконстрикция при нормально развитом легочном сосудистом русле. Может возникнуть при перинатальной асфиксии, аспирации мекония, циркуляторном шоке, стрептококковой пневмонии, повышении вязкости крови, гипогликемии и гипокальциемии. В механизмах вазоконтракции важную роль играют альвеолярная гипоксия и ацидоз, вазоактивные агенты – тромбоксан, сосудосуживающие простагландины, лейкотриены, эндотелин.
-
Гипертрофия медии легочных артериол может развиться при хронической гипоксии плода, может быть следствием приема матерью во время беременности нестероидных противоспалительных лекарственных средств.
-
Недоразвитие легочных артерий, сопровождающееся уменьшением поперечного сечения легочного сосудистого русла при врожденной диафрагмальной грыже и первичной гипоплазии легких.
Легочная гипертензия функционального характера легко обратима при устранении причин, ее вызвавших: ЛГ 2-й группы требует интесивного лечения; ЛГ 3-й группы, как правило, необратима.
ПЛГН сопровождается снижением сократимости миокарда и трикуспидальной недостаточностью, обусловленными общей или субэндокардиальной ишемией миокарда. Гипогликемия и гипокальциемия усиливают гипоксию мокарда.
Клинические проявления в виде цианоза, тахипноэ, стонущего дыхания с втяжением начинаются через 6-12 ч после рождения. Осложнения в родах, анамнестические данные о приеме матерью нестероидных противоспалительных препаратов в III триместре помогают предположить ПЛГН.
Характерны усиленный сердечный толчок, громкий нерасщепленный II тон, ритм галопа, мягкий систолический шум трикуспидальной недостаточности, в тяжелых случаях – гипотензия.
Насыщение артериальной крови в пробах, полученных из пупочной артерии, снижено при нормальном насыщении в предуктальных артериях. Иногда отмечается различие в окраске верхней и нижней половине туловища. При большом сбросе крови справа налево через открытое овальное окно отсутствует разница насыщения в верхнем и нижнем артериальных бассейнах.
ЭКГ обычно соответствует возрастной норме, иногда обнаруживается перегрузка правого желудочка или аномальный зубец Т, свидетельствующие о дисфункции миокарда.
На рентгенограмме можно обнаружить кардиомегалию, усиленный легочной рисунок, ателектаз. Однако эти признаки могут отсутствовать.
При ЭхоКГ-исследовании отсутствуют признаки цианотического порока. Единственной находкой является большой ОАП с право-левым или двухнаправленным сбросом. Правый желудочек расширен, межпредсердная перегородка выбухает влево, имеется открытое овальное окно. Аортальная дуга нормальная, без признаков коарктации аорты или перерыва дуги аорты. Левый желудочек может быть увеличенным, со сниженной фракцией выброса.
Катетеризация обычно не показана, однако если диагноз неясен или больной не поддается лечению, катетеризация и артериографию выполняют, чтобы избежать ошибочного диагноза.
Лечение преследует 3 цели:
-
снижение ЛСС и давления в легочной артерии путем ингаляции кислорода, создания респираторного алкалоза и применения легочных вазодилататоров;
-
коррекцию нарушения функции миокарда;
-
стабилизацию больного и лечение сопутствующей патологии.
Проводят общую поддерживающую терапию: коррекцию гипогликемии, гипокальциемии, гипомагнезиемии, полицитемии. Температуру тела поддерживают в пределах 36,5-37,2 0С.
Для достижения артериальным рО2 100 мм рт. ст. проводят ингаляцию 100% кислорода без интубации. При отсутствии эффекта проводят интубацию с созданием положительного давления в дыхательных путях, составляющего 2-10 см вод. ст. при спонтанном дыхании.
Если эти меры неэффективны, проводят механическую вентиляцию для улучшения оксигенации и достижения дыхательного алкалоза. Используют следующий режим вентиляции: 100% концентрация кислорода, частота дыхания 40-80 в минуту, давление на вдохе 40 см вод. ст., положительное давление на выдохе 4-10 см вод. ст., соотношение времени вдох-выдох 1:1. Больной релаксирован. При достижении нормального насыщения артериальной крови кислородом в течение 12-24 ч, проводят постепенное отлучение от аппарата.
Вазодилататоры, как правило, неспецифичны и расширяют не только легочные, но и системные резистивные артериолы, поэтому в последнее время их не используют.
Наиболее эффективным методом, направленным на снижение ЛСС, является добавление в дыхательную смесь малых доз газообразного NО – селективного легочного вазодилататора. Этот эффективный метод, получивший широкое распространение в западных лечебных учреждениях, пока не внедрен в Украине и находится на стадии клинической апробации.
Лечение сердечной недостаточности проводят, используя общепринятые средства: допамин в дозе 10 мг/кг/мин путем внутривенного введения, добутамин ф-адренергическое средство в начальной дозе 5-8 мг/кг/мин путем постоянного внутривенного введения, дигоксин при хронической застойной сердечной недостаточности на более поздней стадии, диуретики.
Коррекция ацидоза, гипокальциемии, гипогликемии помогает улучшить функции миокарда.
В арсенале средств ведущих западных клиник в отдельных тяжелых случаях ПЛГН имеется такой агрессивный метод, как экстракорпоральная мембранная оксигенация. Однако внедрение ингаляции NО ограничило область ее применения.
Прогноз
При умеренной ПЛГН лечебные действия обычно эффективны и прогноз благоприятный. Большинство новорожденных выздоравливают без легочной или неврологичнской патологии. Среди больных, требующих длительной вентиляции, выживаемость хуже, развивается бронхолегочная дисплазия и другие осложнения. При недоразвитии легочно-сосудистого русла больные резистентны к лечению и прогноз у них плохой. У многих проявляются признаки недоразвития ЦНС, высока частота потери слуха. Эти осложнения прямо связаны со степенью алкалоза, длительностью вентиляции, применением фуросемида и аминогликозидов. У 80% больных отмечаются отклонения на энцефалограмме и у 45% – мозговые инсульты.
Синдром Эйзенменгера у детей
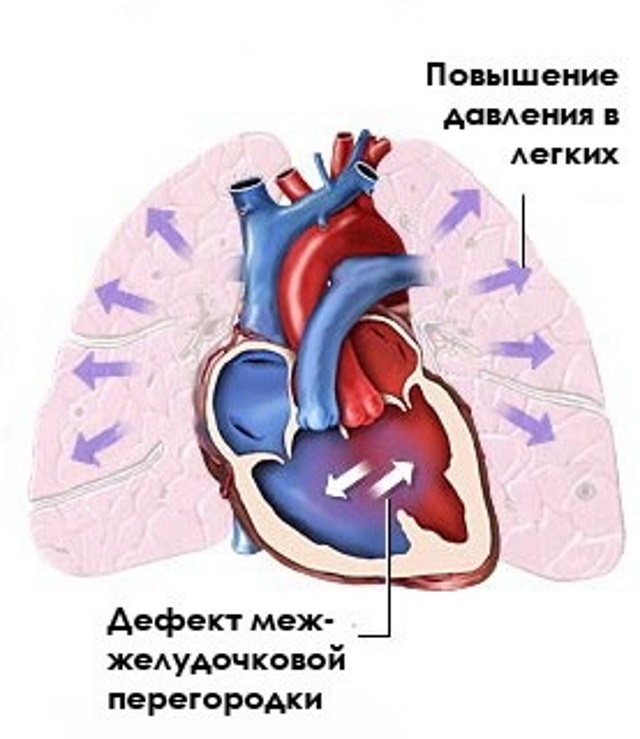
В 1897 г. Eisenmenger описал патолого-анатомические находки у 32-летнего мужчины с большим ДМЖП и ЛГ. Только 60 лет спустя, в 1958 г. Wood в обстоятельном сообщении дал определение заболеванию, которое соответствует нашему пониманию этого клинического синдрома сегодня. Wood использовал термин «синдром Эйзенменгера» для описания больных с давлением в легочной артерии, равном системному, обусловленному высоким ЛСС и право-левым или двунаправленным шунтом на уровне магистральных сосудов, межжелудочковой или межпредсердной перегородок. Термин «комплекс Эйзенменгера» применяется, когда основным пороком является ДМЖП.
С развитием кардиохирургии раннего возраста частота возникновения синдрома Эйзенменгера уменьшается. Она определяется уровнем культуры населения и первичного звена здравоохранения. Синдром Эйзенменгера встречается даже в возрасте 2 мес.
Клиника
Типичными признаками заболевания являются цианоз, полицитемия, правожелудочковая недостаточность. У пациентов с комплексными врожденными пороками – ОАС, АВСД, одножелудочковым атриовентрикулярным соединением и транспозицией – симптоматика синдрома Эйзенменгера развивается рано и хуже прогноз. У пациентов с трисомией 21 заболевание также протекает тяжело. Обычно симптоматика прогрессирует медленно и ярко проявляется в юношеском возрасте и у взрослых. У всех пациентов снижена физическая работоспособность.
Цианоз вначале проявляется при нагрузке и затем становится постоянным, что отражает величину право-левого сброса. Насыщение артериальной крови кислородом – 80-85 %. Постоянным признаком у цианотичных больных является утолщение концевых фаланг пальцев в виде барабанных палочек. Гипертрофическая остеоартропатия может прогрессировать с появлением артралгии и суставных синовитов.
Артериальная гипоксемия является причиной эритроцитоза. Повышение содержания гемоглобина увеличивает кислородную емкость крови. Сопутствующее полицитемии повышение вязкости крови не проявляет себя, пока уровень гемоглобина не превышает 18-20 г/л. Симптоматика повышенной вязкости крови:
-
головная боль;
-
головокружение;
-
нарушение зрения, обусловленное окклюзией центральной вены сетчатки.
Повышение вязкости крови является фактором риска тромбоза и кровоизлияний в мозг. Из-за тромбоцитопении, удлинения времени свертывания, дефицита факторов свертывания и фибринолиза больные склонны к кровоточивости при хирургических вмешательствах и экстракции зубов. У 20 % пациентов возникают легочные кровотечения в результате разрывов бронхиальных артерий или аневризм легочных артерий, развивающиеся вследствие прогрессирующей дилатации центральных легочных артерий.
Причиной кровохарканья могут стать эмболия и тромбоз расширенных легочных артерий.
Часто наблюдающаяся уремия обусловлена повышенной продукцией и сниженным почечным клиренсом мочевой кислоты. У 13-23 % пациентов развивается подагра. Усиленный эритропоэз и деструкция эритроцитов приводит к билирубинемии и повышению билирубина в желчи, поэтому у 15 % больных наблюдаются холелитиаз и холецистит. У 65 % больных отмечается дисфункция почек с протеинурией и развитием нефротического синдрома с повышением сывороточного креатинина. Это служит дополнительным фактором, снижающим выживаемость.
Характерными являются церебральные осложнения: инсульт в возрасте около 30 лет и абсцессы мозга в 20-25 лет. Нередки нарушения ритма в виде суправентрикулярной и желудочковой экстрасистолии, трепетания и фибрилляции предсердий. У каждого пятого больного возникают обморочные и пресинкопические состояния, связанные с желудочковой тахикардией.
Эндокардиты встречаются с частотой около 4%. У некоторых пациентов отмечаются охриплость и кашель, связанные с компрессией гортанного нерва, дилатированными легочными артериями. Расширенные легочные артерии могут сдавливать левую коронарную артерию с возникновением ангинозных болей. 30 % пациентов умирают внезапно. Хотя наличие шунта удлиняет жизнь пациентов с синдромом Эйзенменгера в сравнении с больными с первичной ЛГ, 40—50 % из них умирают от сердечной недостаточности. Последняя особенно часта при сложных базовых пороках и обусловлена стенозом или недостаточностью атриовентрикулярного или полулунного клапанов.
Больные с синдромом Эйзенменгера нуждаются в квалифицированном ведении. Около 20 % смертей связаны с ошибками, которые можно избежать. Не связанные с сердцем хирургические вмешательства являются причиной 24 % смертей. Венесекции необходимо выполнять с осторожностью. Больные должны быть предупреждены о риске беременности, пребывания на высоте, приёма эстрогенов, наркоза.
Применение вазодилататоров и антикоагулянтов следует проводить под квалифицированным контролем с учетом баланса между сопротивлением легочных и системных сосудов и риска развития кровотечения и тромбоза. Исходы беременности, как правило, неблагоприятные:
-
спонтанный аборт или преждевременные роды наблюдаются у 25 %;
-
терапевтический аборт – у 27 %;
-
недоношенность или малая масса ребенка – у 26 %;
-
материнская смерть – у 16 %;
-
ухудшение состояния матери – у 54 % больных.
Консервативное лечение малоэффективно. Однако в последнее время появились сообщения о частичном сохранении реактивности легочных сосудов и некоторой регрессии запущенной ОБЛС, что возобновило интерес к лечению вазодилататорами последних поколений. Gorenflo и соавторы провели сравнительное изучение эффективности различных вазодилататоров у детей с ВПС, ЛГ и средним индексом Wood 10 ед/м2. Давление в легочной артерии и ЛСС снижались в ответ на ингаляцию кислорода у 2 из 14 пациентов, на ингаляцию NO – у 4 из 14, на дополнительное к NO внутривенное введение простациклина – у 2 из 7 пациентов. Ингаляция кислорода не отражалась на уровне вазоактивных медиаторов. Оксид азота в дозе до 80 ppm повышал уровень цГМФ в среднем в 2 раза, однако связь уровня цГМФ с гемодинамическим ответом отсутствовала.
Rosenzweig и соавторы применили длительную инфузию простациклина для смягчения симптоматики синдрома Эйзенменгера и показали снижение среднего давления в легочной артерии на 20%, увеличение сердечного индекса с 3,5 до 5,9 л/мин/м2, улучшение функционального класса с 3,2 до 2,0, увеличение переносимости нагрузок и доставки кислорода, однако насыщение артериальной крови кислородом не повысилось.
Закрытие ДМЖП после предварительного суживания легочной артерии при синдроме Эйзенменгера впервые описано в 1971 г. у Azzolina и вызвало активные дебаты. В эксперименте и в клинике были хорошо документированы регрессия гипертрофии медии и пролиферация интимы после прессорной разгрузки легочных сосудов, однако осталось неясным, подвергаются ли регрессии далеко зашедшие изменения – фиброз интимы, фибриноидный некроз или плексиформные поражения после суживания легочной артерии. Интересно, что ЛСС может снизиться после закрытия артериального протока, несмотря на плексиформную артериопатию.
Nowick и соавторы предложили закрывать ДМЖП у больных с высоким сопротивлением легочных сосудов двойной заплатой-клапаном с отверстием для обеспечения право-левого сброса крови при подъеме давления в правом желудочке выше системного. У 18 оперированных пациентов сосудистое сопротивление составляло в среднем 11,4 ед/м2, и у всех отмечался цианоз, несмотря на преимущественно лево-правый шунт. В публикации не были представлены данные о реактивности легочных сосудов, поэтому трудно оценить выраженность обструктивной болезни сосудов у этих пациентов.
Трансплантация легких
Трансплантацию легких редко применяют у детей с синдромом Эйзенменгера. Результаты этих вмешательств у детей и взрослых с ВПС и ЛГ идентичны. Госпитальная летальность составляет 23%, 5-летняя выживаемость – 57%. Легочная трансплантация без пересадки сердца возможна у больных с ДМПП и ОАП. При комплексе Эйзенменгера выживаемость лучше, если пересаживаются одновременно сердце и легкие, в противоположность трансплантации только легкого и закрытия ДМЖП. У взрослых 1-, 5- и 10-летняя выживаемость соответственно равна 73%, 51% и 28%.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания










Комментарии