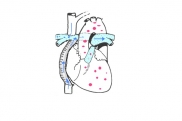
Отхождение коронарных артерий от легочного ствола
Отхождение левой коронарной артерии от легочной артерии является редкой патологией, ведущей к ишемии миокарда и инфаркту. Впервые она была описана Brook в 1886 г. и позднее Abbott в 1908 г. В отечественной литературе она впервые представлена Абрикосовым в 1911 г. Однако эта проблема не вызывала большого интереса до публикации Bland, Garland и White в 1933 г., которые описали ребенка с этой патологией и записали ЭКГ, зарегистрировавшую переднебоковой инфаркт миокарда. Синдром стали называть именами этих авторов.
Аномалия составляет 0,25-0,50% всех ВПС. Чаще встречается как самостоятельный порок, но также может сочетаться с другими пороками сердца, включая ОАП, ДМЖП, коарктацию аорты, синдром Shone, тетраду Фалло, ТМА, синдром гипоплазии левого сердца, аномалию Эбштейна, ДМПП, синдром турецкой сабли, частичный аномальный дренаж легочных вен, стеноз легочной артерии, дефект аортолегочной перегородки, атрезию аорты и др..
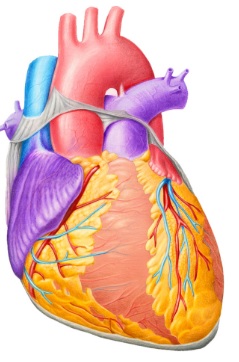
Анатомия
Аномальная левая коронарная артерия обычно отходит от прилежащего к аорте легочного синуса. Она также может отходить от легочного ствола, от проксимальной левой или правой легочной артерии, реже из неприлежащего синуса Вальсальвы легочной артерии. В эмбриональном периоде эпикардиальные коронарные артерии развиваются с отклонением в сторону легочной артерии, а не в сторону корня аорты, со временем врастая в стенку легочной артерии. У некоторых пациентов возникает стеноз устья коронарной артерии на месте соединения с легочным стволом или ветвью легочной артерии. После годовалого возраста в связи с увеличением кровотока через правую коронарную артерию, которая становится главным источником кровоснабжения сердца, она значительно дилатируется. Именно этот признак используется в эхокардиографической диагностике данной патологии и дает возможность дифференцировать ее от дилатационной кардиомиопатии. В редких случаях обнаружения этой патологии у взрослых правая коронарная артерия аневризматически расширена. Отхождение левой коронарной артерии от правой легочной артерии часто сочетается с другими пороками сердца. Иногда начальная часть аномально отходящей артерии проходит в толще стенки аорты, что не сопровождается значительными нарушениями со стороны сердца.
Очень редко левая передняя нисходящая ветвь отходит от легочной артерии.
Прогрессирующая ишемия приводит к:
-
дилатации сердца, преимущественно левого желудочка;
-
выраженному фиброэластозу эндокарда;
-
гипертрофии и деформации папиллярных мышц вследствие инфаркта и склероза;
-
аневризме на переднебоковой стенке левого желудочка или в области верхушки, т.е. в местах, кровоснабжающихся из левой коронарной артерии.
Нередко обнаруживаются свежие субэндокардиальные или трансмуральные инфаркты миокарда левого желудочка. Инфаркт папиллярных мышц является причиной недостаточности митрального клапана, которая во многих случаях становится доминирующей патологией.
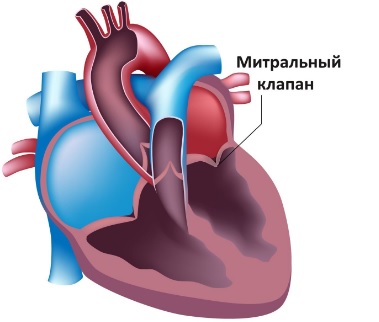
Патофизиология
Во внутриутробном периоде эта аномалия не оказывает отрицательного эффекта, так как давление и насыщение кислородом крови в аорте и легочной артерии одинаково. Перфузия миокарда нормальная, и нет стимулов для развития коллатеральных сосудов. После рождения в легочной артерии циркулирует десатурированная кровь. Несмотря на это в первые 2 месяца жизни смертность существенно ниже, чем в последующем на протяжении младенческого возраста. Это обусловлено физиологическим состоянием сердечно-сосудистой системы в перинатальном периоде. Высокое, практически равное диастолическое давление в аорте и легочном стволе обеспечивает достаточное перфузионное давление в коронарных артериях. Кроме того, наличие фетального гемоглобина и характерной для него кривой диссоциации способствует защите от ишемии. По мере естественной регрессии мышечного слоя стенки легочных сосудов и падения давления в легочной артерии до нормального уровня левый желудочек кровоснабжается десатурированной кровью при низком давлении. К этому времени кровоток по коллатералям еще незначительный. В качестве первой адаптивной реакции сосуды миокарда левого желудочка расширяются, чтобы снизить их сопротивление и увеличить кровоток. Однако сосудистый резерв скоро истощается и ишемия миокарда усиливается. Вначале ишемия носит перемежающийся характер и возникает только при напряжении, связанном с кормлением и плачем. Дальнейшее увеличение потребности миокарда в кислороде приводит к инфаркту переднебоковой стенки левого желудочка, сердечной слабости и митральной недостаточности вследствие дилатации левого желудочка или инфаркта передней папиллярной мышцы.
Количество коллатералей, с которыми рождается ребенок, предопределено генетически. Правая коронарная артерия и коллатеральные сосуды, связывающие ее с левой коронарной артерией, расширяются за счет градиента давления между ними. Градиент давления и гипоксия миокарда являются стимулами для развития коллатерального кровообращения. Обходной кровоток в основном формируется в трех областях:
-
в области выводного тракта правого желудочка;
-
в области верхушки сердца;
-
в межжелудочковой перегородке за счет увеличения сети коронарных сосудов.
В связи с тем, что левая коронарная артерия связана с легочной артерией, коллатеральный кровоток направляется больше в сосуд низкого давления, чем в сосуды миокарда с высоким сопротивлением.
С помощью коронарографии можно видеть, что кровь в левую коронарную артерию поступает не из легочной артерии, а через межкоронарные анастомозы из правой коронарной артерии, отходящей от аорты. Происходит лево-правый сброс через коронарное сосудистое ложе из аорты в легочную артерию. Кровоснабжение миокарда левого желудочка зависит от степени развития коллатералей, давления в левой коронарной артерии и выраженности феномена утечки крови в легочную артерию. Эта утечка относительно невелика, чтобы повлиять на сердечный выброс, но является существенной потерей для перфузии миокарда. При выраженном синдроме обкрадывания особенно страдает субэндокардиальный кровоток. Это одна из причин фиброэластоза эндокарда.
У 15% пациентов коронарного кровотока достаточно, чтобы обеспечить функцию миокарда в покое и даже при нагрузке. Они могут дожить до взрослого возраста.
Клиническая картина
Клинические проявления зависят от выраженности коллатералей между двумя коронарными системами. Выделяют два клинико-гемодинамических типа, отражающих возрастную динамику коронарного кровообращения при этой патологии: инфантильный и взрослый. Позже был выделен промежуточный тип как гемодинамическая фаза этого порока. В IV фазе кровоснабжение миокарда вновь уменьшается из-за развития синдрома обкрадывания.
У большинства пациентов заболевание проявляется в течение первых 3 мес. жизни, реже – во 2-м полугодии. Первыми признаками являются нарушение общего состояния, вялость, бледность кожных покровов, повышенная потливость, рвота, срыгивания, одышка, тахикардия. У половины больных отмечаются приступы внезапного резкого беспокойства с усилением одышки, бледности, потливости, которые иногда становятся первым признаком болезни. Приступы беспокойства возникают обычно после или во время кормления и длятся несколько минут. В это время выражение лица ребенка страдальческое, он пронзительно кричит, вытягивает ноги, пульс становится нитевидным. Иногда приступы сопровождаются повышением температуры, поносом. Одышка и диарея являются типичными симптомами этого порока. Между приступами ребенок ведет себя спокойно и только одышка говорит о наличии застойной сердечной недостаточности. Описанная картина является детским эквивалентом стенокардии у взрослых.
Многие дети в стадии декомпенсации заболевания отстают в физическом развитии. У них рано развивается левосторонний сердечный горб. Верхушечный толчок разлитой, ослабленный, смещен в VI межреберье. Границы сердца расширены преимущественно влево и свидетельствуют о кардиомегалии. Тоны сердца чаще приглушены, нередко выслушивается систолический шум недостаточности митрального клапана. Непрерывный мягкий систолодиастолический шум во II межреберье слева напоминает шум при ОАП или при артериовенозной фистуле и чаще начинает выслушиваться на 2-3-м году жизни. Сердечная недостаточность выражена больше по левожелудочковому типу.
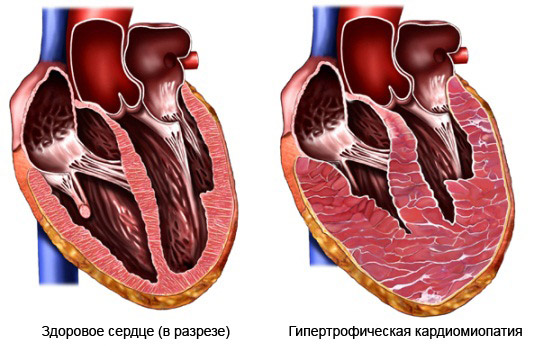
В стадии субкомпенсации самочувствие больных удовлетворительное, приступы отсутствуют и появляются жалобы на боли в сердце. Размеры сердца увеличены умеренно влево. В стадии компенсации жалоб нет, при аускультации выслушивается шум недостаточности митрального клапана и/или систолодиастолический шум. Эта стадия в одних случаях формируется постепенно, начиная с выраженной декомпенсации, в других – с рождения ребенка состояние остается стабильным, жалоб нет, из-за чего заболевание сердца долго не диагностируется. В таких случаях внезапно, среди «полного здоровья», в различном возрасте появляются одышка, загрудинная боль при нагрузке, затем в покое, реже приступы стенокардии, возможна внезапная смерть.
Диагноз аномального отхождения левой коронарной артерии от легочной артерии может быть заподозрен при сочетании приведенной выше клиники с кардиомегалией на обзорной рентгенограмме грудной клетки и признаками ишемии миокарда на ЭКГ.
-
Электрокардиография.
Почти в половине случаев обнаруживается выраженное отклонение электрической оси сердца влево из-за блокады передней левой ветви пучка Гиса. Характерный симптом на ЭКГ – глубокий, уширенный зубец Q в отведениях I, аVb, V5-6. В стадии декоменсации такие изменения нередко сочетаются с подъемом сегмента БТ выше изолинии на 3-6 мм и уменьшением амплитуды зубца Я, что соответствует картине острого инфаркта миокарда. В то же время у детей с застывшими глубокими зубцами Q, но без подъема сегмента БТ на аутопсии находят следы ранее перенесенного инфаркта миокарда, распространенный кардиосклероз и гипертрофию межжелудочковой перегородки. Диагностическую значимость имеет «провал» амплитуды зубца Я в отведениях V3 и V4, свидетельствующий о перенесенном инфаркте миокарда. В стадии субкомпенсации и компенсации сохраняются признаки гипертрофии миокарда левого желудочка с субэндокардиальной ишемией, зубец О остается глубоким в отведении аVb, реже I, V5-6.
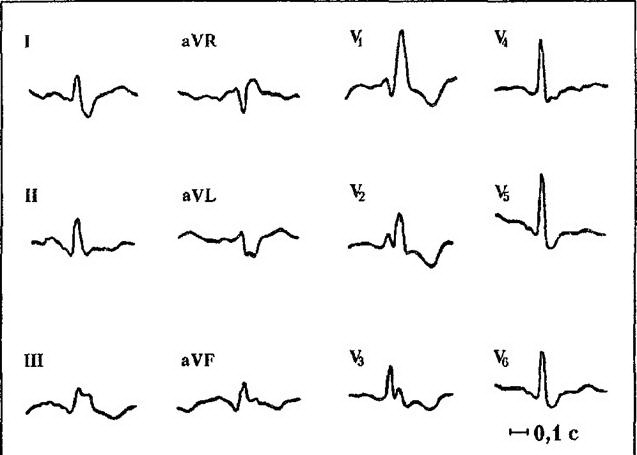
-
Рентгенография.
На рентгенограмме органов грудной клетки у критически тяжелых младенцев обнаруживаются выраженная кардиомегалия, преимущественно за счет левых отделов, и признаки легочной венозной гипертензии. Иногда выбухает левый контур сердца, образованный аневризмой левого желудочка. Рентгенологическая картина соответствует таковой при различных формах кардиомиопатии, поэтому в каждом случае очевидной кардиомиопатии необходимо исключить отхождение левой коронарной артерии от легочного ствола и тем самым дать пациенту надежду на хирургическое исцеление. При компенсированном пороке сердце может быть почти нормальных размеров.
-
Эхокардиография.
Основным методом диагностики данной аномалии является ЭхоКГ. Двухмерная ЭхоКГ позволяет установить только предположительный диагноз, поскольку не во всех случаях удается определить устья коронарных артерий. Она может дать ложное выпадение эхо-сигнала в стенке, отделяющей просвет аорты от левой коронарной артерии. При выведении клапанов легочной артерии сразу над ними можно увидеть левую коронарную артерию. Пульсирующее волновое и цветное допплер-исследования позволяют с большой достоверностью выявить ретроградный кровоток в сегменте аномальной артерии и диастолическую струю внутри легочного ствола, а также расширенную правую коронарную артерию. Эхокардиографическая диагностика ненадежна. Когда давление в легочной артерии повышено, как у новорожденных и у детей с недостаточностью левого желудочка, кровоток по левой коронарной артерии может быть антеградным и правая коронарная артерия не будет дилатированной, пока не упадет диастолическое давление в легочном стволе. В этих случаях только ангиография может разрешить сомнения.
Исследование позволяет определить размер и функцию левого желудочка, уменьшение экскурсии задней стенки левого желудочка и недостаточность митрального клапана. Можно увидеть повышенную эхогенность папиллярной мышцы и прилежащего эндокарда вследствие фиброза и фиброэластоза.
-
Катетеризация сердца и ангиокардиография.
Если исчерпаны возможности неинвазивных методов исследований, выполняют катетеризацию и ангиографию. При зондировании полостей сердца отмечают увеличение давления в легочной артерии и повышение в ней насыщения крови кислородом: сброс крови из левой коронарной артерии в легочную составляет 10-35 % минутного объема большого круга кровообращения. Уточненный диагноз можно поставить с помощью комплекса контрастных исследований:
-
левой вентрикулографии;
-
ангиографии корня аорты;
-
селективной коронарографии;
-
заполнения контрастным веществом легочного ствола.
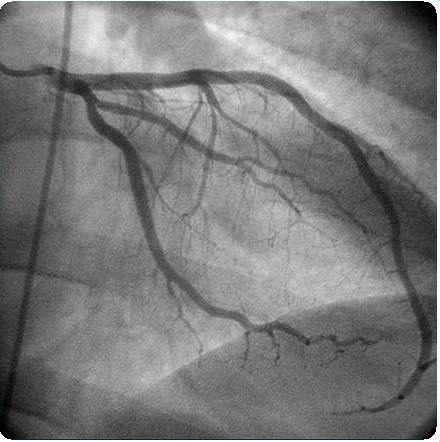
Селективная артериография правой коронарной артерии наиболее информативна. При аортографии или селективной коронарографии контрастное вещество вводят в расширенный ствол правой коронарной артерии, из нее видно ретроградное заполнение системы
Контрастирование ствола легочной артерии информативно только при антеградном кровотоке в левой коронарной артерии, т.е. при легочной гипертензии. При левой вентрикулографии заполняется расширенный левый желудочек, возможна его аневризма.
Естественное течение
У новорожденных данная патология себя не проявляет, поскольку для них характерно повышенное давление в легочной артерии, обеспечивающее нормальный антеградный кровоток в аномально отходящую коронарную артерию. В младенческом возрасте клиника неопределенная и диагноз ставится достаточно поздно – при очевидном инфаркте миокарда, поэтому 80-90% больных умирают в течение первого года жизни. У некоторых пациентов наступает спонтанное улучшение состояния, что связано с развитием межкоронарных коллатералей. В редких случаях заболевание проявляется позже – в детстве, подростковом периоде или у взрослых – нарастающим шумом, митральной регургитацией, загрудинной болью или нарушениями сердечного ритма. Такие пациенты, очевидно, имеют достаточно хорошо развитые коллатерали. Известны случаи бессимптомного течения этого порока в возрасте 60-90 лет. Описаны случаи отсутствия симптоматики у лиц с аномальным отхождением левой коронарной артерии и сужением ее устья, зафиксированном при ЭхоКГ и ангиографии. Очевидно, что стеноз устья препятствует утечке крови в легочную артерию и позволяет ребенку дожить до взрослого возраста.
Хирургическое лечение
При выборе лечебной тактики в каждом случае необходимо рассмотреть ряд ключевых вопросов. Следует определить:
-
Необходимость установления системы двух коронарных артерий.
-
Оптимальный тип хирургического вмешательства.
-
Специфические приемы для улучшения результата.
-
Возможность восстановления сократимости левого желудочка.
-
Возможность улучшения функции митрального клапана.
-
Целесообразность повторной операции.
Несколько авторов проанализировали различные вмешательства, предложенные на протяжении хирургической истории этого порока и направленные на улучшение состояния младенцев с недостаточным развитием коллатеральных артерий и ишемией миокарда. В настоящее время многие из них представляют лишь исторический интерес. Одним из первых вмешательств было создание аортолегочного анастомоза, задуманного для повышения давления в легочном стволе. С самого начала эта идея оказалась порочной, так как увеличение объёмной нагрузки приходилось на уже скомпроментированный левый желудочек. Попытки сузить легочный ствол также не имели успеха. Химический эпикардиолиз или припудривание полости перикарда тальком с расчетом на образование сращений предназначались для увеличения коллатерального притока к миокарду левого желудочка и давали незначительное улучшение. Попытки соединить пересеченную левую коронарную артерию с левой общей сонной артерией приводили к гибели большинства пациентов.
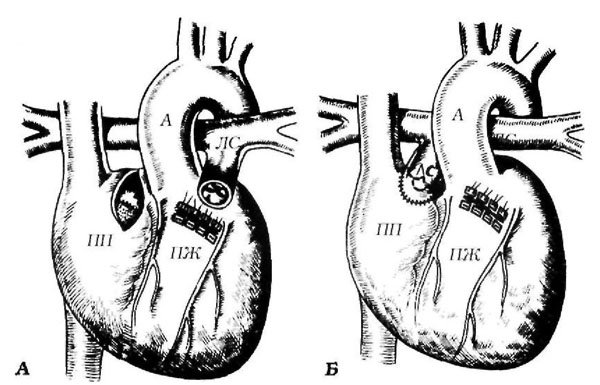
Следующим поколением хирургических операций было перекрытие шунта в легочную артерию и восстановление антеградного кровотока в левой коронарной артерии. В 1958 г. Edvards, Case и соавторы предложили перевязку левой коронарной артерии, которая преследовала цель ликвидировать синдром обкрадывания и улучшить коронарное кровообращение путем повышения перфузионного давления. Однако эта операция превращает коронарную систему сердца в систему единой коронарной артерии с хирургической летальностью 30% или более и сохранением риска внезапной смерти в отдаленном периоде в 14-25% случаев. У некоторых младенцев наблюдалось улучшение состояния, однако с годами развивалась явная ишемия миокарда. Наблюдения за пациентами в возрасте от 3 лет до 21 года, выживших после перевязки, показали, что некоторые из них предъявляют жалобы на боль за грудиной, у других выявлены патологические 5Т-сегменты на ЭКГ или признаки ишемии миокарда на сцинтиграфии при физической нагрузке. В покое фракция выброса левого желудочка была в пределах нормы у всех пациентов. Но адекватного подъема фракции выброса во время дозированной физической нагрузки не было, что отражало ухудшение функции желудочка. Однако некоторые пациенты чувствовали себя хорошо в течение многих лет. Эти результаты стимулировали разработку методов создания двухкоронарной системы.
История формирования двухкоронарной системы проходила в два этапа. Вначале были предложены различные типы непрямых анастомозов между системными артериями и левой коронарной артерией с использованием левой подключичной артерии, внутренней грудной артерии, сосудистых протезов или большой подкожной вены. Физиологический характер этих операций обеспечивал хороший клинический эффект. Однако эти операции не воссоздают нормальных анатомических и гемодинамических условий и имеют недостатки, характерные для всех межартериальных анастомозов, поэтому дальнейшее совершенствование хирургической технологии шло в направлении прямой реимплантации устья левой коронарной артерии в восходящую аорту. Заслуга в разработке операций прямой реимплантации левой коронарной артерии в аорту принадлежит Neches и соавторам. Внедрение в середине 70-х годов операции Jatene по пересадке коронарных сосудов при коррекции ТМА послужило толчком для хирургической реимплантации аномальной левой коронарной артерии. При наличии неблагоприятных условий для реимплантации Takeuchi разработал альтернативный метод – создание внутрилегочного туннеля между аортой и устьем коронарной артерии in situ.
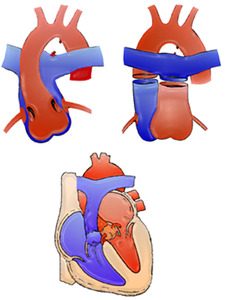
Невзирая на преимущества двухкоронарной системы, перевязка левой коронарной артерии при наличии в ней ретроградного кровотока используется в качестве неотложной помощи.
Техника операций
Реимплантация коронарной артерии в аорту. Левый желудочек обычно дилатирован, с внешними признаками дисфункции вследствие ишемии миокарда и недостаточности митрального клапана. Манипуляции на миокарде должны быть минимальными до начала искусственного кровообращения, чтобы избежать фибрилляции желудочков.
Аорту канюлируют дистально возле безымянной артерии. Перфузию проводят с одной венозной канюлей, введенной в правое предсердие. Операцию выполняют в условиях постоянной перфузии и умеренной гипотермии с низкой объемной скоростью, у очень маленьких грудных детей – в период остановки кровообращения при глубокой гипотермии. Дилатированный левый желудочек дренируют через правую верхнюю легочную вену.
Вне зависимости от техники коррекции важнейшим элементом операции является защита миокарда левого желудочка. Кардиоплегический раствор вводят отдельно в аорту и в легочную артерию.
Выделяют легочный ствол и исследуют прохождение левой коронарной артерии по эпикарду. Если аномальная коронарная артерия отходит далеко слева или спереди легочного ствола, прямая реимплантация может оказаться невозможной. Полностью выделяют аорту и обе легочные артерии. Перевязывают и пересекают артериальную связку для улучшения мобильности легочной артерии. После начала искусственного кровообращения левую и правую ветви легочной артерии пережимают турникетами для предупреждения утечки кардиоплегического раствора в легкие. Вместо этого коронарную артерию можно прижать пальцем.
Легочный ствол открывают поперечным разрезом непосредственно выше синотубулярного соединения, находят устье коронарной артерии и пересекают легочный ствол. Устье коронарной артерии иссекают вместе со стенкой синуса, как при операции артериального переключения. Если устье расположено рядом с комиссурой, ее отсекают, чтобы получить «пуговицу» достаточного размера. Проксимальную часть коронарной артерии выделяют из окружающих тканей с помощью электрокоагулятора, стараясь не повредить мелкие ветви. Перфорируют левую стенку аорты в месте предполагаемой имплантации «пуговицы» коронарной артерии, которую анастомозируют с аортой без натяжения.
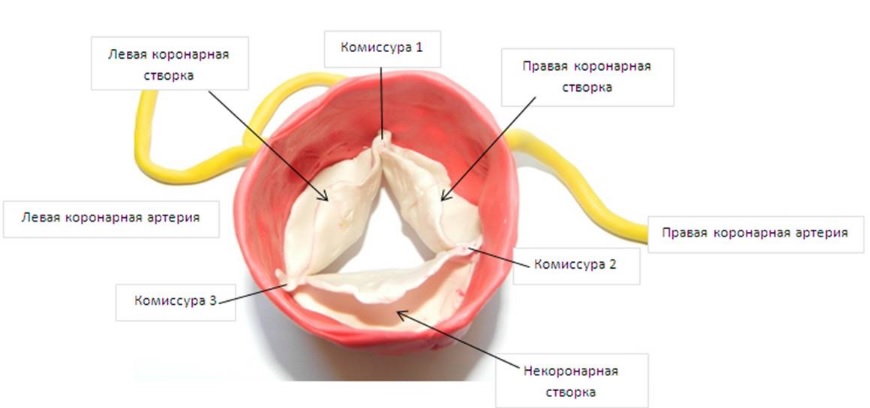
Если аномальная коронарная артерия отходит от легочного ствола спереди или слева, ее иссекают в блоке с кольцом стенки легочной артерии и удлиняют трубкой, сшитой из стенки легочной артерии. В модификации Jonas для удлинения коронарной артерии используют два лоскута – из передних стенок легочной артерии и аорты. Устье аномальной коронарной артерии иссекают с длинным лоскутом передней стенки легочного ствола. Последний лучше полностью пересечь. Оба лоскута сшивают между собой в виде трубки. Ее имплантируют в аорту с помощью заплаты из аутоперикарда. Легочный ствол восстанавливают прямым реанастомозированием после перевязки и пересечения артериального протока.
Для исключения возможности повреждения аортального клапана при перфорации аорты по выбору хирурга применяют альтернативный метод. Аорту открывают поперечным разрезом над синотубулярным соединением. Разрез продлевают кзади над левым коронарным синусом. Синус разрезают вертикально для формирования места имплантации «пуговицы» коронарной артерии.
«Пуговицу» приспосабливают к разрезу, чтобы избежать перекручивания и перегиба артерии. Для этой цели может быть использован прием «открытой двери», как при операции артериального переключения.
Линию шва начинают в наиболее низкой точке коронарной «пуговицы» 7/0 проленом. Шов продолжают к вершине разреза кпереди и кзади. Аорту закрывают непрерывным швом 7/0 проленом, который связывают с концами нитей шва «пуговицы». После закрытия аорты в ее просвет вводят кардиоплегический раствор. Оценивают адекватность заполнения пересаженной коронарной артерии.
Дефект в стволе легочной артерии закрывают заплатой из аутоперикарда. Реконструированную проксимальную часть легочного ствола анастомозируют с бифуркацией легочных артерий 7/0 проленом. Иногда легочный ствол удается восстановить прямым анастомозом без реконструкции выреза. Если комиссура была отделена от стенки синуса во время иссечения коронарной «пуговицы», легочная артерия должна быть реконструирована аутоперикардом, а комиссура должна быть укреплена на прежнем уровне.
После завершения реконструкции снимают зажим с аорты и больного согревают. Для сокращения времени ишемии зажим может быть снят перед реконструкцией легочной артерии. Во время согревания, как и в период охлаждения, необходимо дренирование левых отделов сердца. Первые сокращения сердца стимулируют введением кальция. Дренирование прекращают под контролем давления в левом предсердии. Если давление повышается, дренирование левого предсердия продолжают.
На завершающем этапе оценивают состояние перфузии и функции левого желудочка, а также линию шва на предмет гемостаза. Подшивают электроды водителя ритма. После согревания пациента отлучают от искусственного кровообращения и проводят модифицированную ультрафильтрацию. Необходим ЭКГ-контроль во время реперфузии и после отключения насоса для диагностики ишемии. У больных с тяжелой дооперационной дисфункцией левого желудочка необходима инотропная поддержка или в отдельных случаях ЭКМО. При ее проведении дренаж в левом предсердии соединяют с системным венозным дренажом для декомпрессии левого желудочка. Значительное улучшение функции левого желудочка наступает через 48-72 ч. В эти сроки дренаж может быть удален. До полного восстановления сократимости сердца продолжают проводить ЭКМО по схеме «правое предсердие-аорта». Отключение механической поддержки обычно возможно на 5-6-е сутки.
-
Операция Takeuchi.
Альтернативным методом коррекции отхождения левой главной коронарной артерии от легочной артерии является создание туннеля внутри легочного ствола, или операция Takeuchi. Согласно оригинальному методу, создают аортолегочное окно и с помощью лоскута передней стенки легочного ствола формируют туннель, направляющий кровь из аорты в устье аномальной коронарной артерии. Эту операцию выполняют при отсутствии благоприятных условий для прямой реимплантации левой коронарной артерии в аорту. Первым этапом является выкраивание лоскута. Для этого вначале производят короткий поперечный разрез легочного ствола, чтобы убедиться в невозможности прямой реимплантации, затем формируют лоскут необходимой длины и ширины. Перфорируют прилежащие друг к другу отверстия в легочной артерии и аорте и анастомозируют их непрерывным швом 7/0 проленом. Создавая аортолегочное окно, избегают прямого повреждения или деформации створок полулунных клапанов и комиссур. Лоскут передней стенки легочного ствола пришивают к его задней стенке и вокруг устья коронарной артерии в синусе легочного клапана. Обращают внимание на предупреждение деформации и суживания устья коронарной артерии. Кровь из аорты через аортолегочное окно по туннелю поступает в аномальную коронарную артерию. Оставшийся дефект передней стенки легочного ствола реконструируют обработанным глютаральдегидом аутоперикардом или политетрафлюороэтиленом. Заплата должна быть достаточных размеров, чтобы не возник надклапанный стеноз легочной артерии.
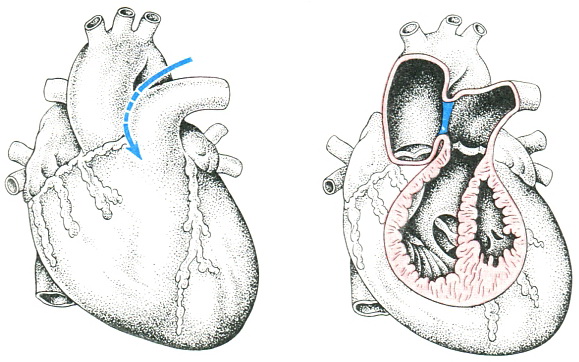
Данный метод можно использовать вне зависимости от расстояния между аортой и устьем коронарной артерии. Он создает двухкоронарную артериальную систему с помощью собственных тканей, способных к росту.
-
Модифицированная операция Takeuchi.
Модифицированная техника предусматривает конструирование туннеля с помощью заплаты из политетрафлюороэтилена. Эта модификация особенно полезна, если устье коронарной артерии расположено по левому краю легочного ствола. Создание туннеля может оказаться невозможным, если устье расположено около комиссуры или если коронарная артерия отходит от ветви легочной артерии. Осложнениями операции Takeuchi являются обструкция туннеля, его негерметичность и надклапанное сужение выводного тракта правого желудочка.
Операцию выполняют в условиях сниженной объемной скорости перфузии при температуре 25-30 0С или во время гипотермической остановки кровообращения. Канюлирование осуществляют так же, как при прямой реимплантации. Кардиоплегический раствор вводят при пережатых ветвях легочной артерии. После остановки сердца производят продольный разрез легочного ствола. Находят устье аберрантной коронарной артерии. С помощью 5-миллиметрового перфоратора прокалывают отверстие в аорте выше синотубулярного соединения с левой стороны. Если имеются сомнения в выборе места перфорации, производят разрез аорты и под контролем зрения проделывают отверстие, не повреждая аортальный клапан.
Перфорируют легочный ствол напротив аортального отверстия и создают аортолегочное окно непрерывным швом 7/0 проленом. Сосудистый протез диаметром 4 мм и соответствующей длины из Gore-Tex разрезают вдоль и используют для создания внутрилегочного туннеля между аортолегочным окном и устьем коронарной артерии. Шов начинают от устья артерии и продолжают вдоль легочного ствола к аортолегочному окну. Вторую линию шва ведут в том же направлении. Оба конца нити связывают.

Разрез легочной артерии закрывают заплатой из аутоперикарда для обеспечения свободного выхода из правого желудочка. Снимают зажим аорты и завершают обычным образом.
Шунтирующие способы создания антеградного кровотока по левой коронарной артерии. Артериально-коронарное шунтирование выполняют с помощью левой подключичной артерии, большой подкожной вены или внутренней грудной артерии. Наиболее типичным показанием для использования левой внутренней грудной артерии является предшествующая перевязка левой коронарной артерии или наличие стеноза и окклюзии вследствие попытки коррекции. Подкожную вену используют как исключение, когда артериальные сосуды недоступны.
Если передняя нисходящая артерия имеет отдельное устье, его иссекают вместе с частью стенки легочной артерии, чтобы дотянуть до места имплантации. Однако артерия часто отходит от передней поверхности легочного ствола, и этот маневр трудно осуществить. Альтернативным приемом является перевязка проксимального участка коронарной артерии и шунтирование левой внутренней грудной артерией. Изолированное отхождение левой огибающей коронарной артерии встречается редко, и оптимальный метод операции не опубликован. Аномальная правая коронарная артерия отходит от передней стенки легочного ствола, и методом выбора является прямая реимплантация.
Результаты
В литературе широко представлена эволюция хирургического алгоритма. Backer и соавторы проанализировали свой опыт хирургических вмешательств, проведенных 20 пациентам в двух учреждениях в 1970-1990 гг. Возраст оперируемых колебался от 3 нед. до 11 лет. У 12 пациентов была застойная сердечная недостаточность, у 3 – кардиогенный шок. Применены различные типы вмешательств:
-
перевязка аномальной артерии;
-
анастомоз подключичной артерией;
-
прямая имплантация;
-
анастомоз внутренней грудной артерией;
-
внутрилегочное туннелирование;
-
трансплантация сердца.
Трое пациентов умерли через 3 нед, 2 мес. и 9 лет после перевязки артерии. Летальных исходов не было после формирования двухкоронарной системы и после трансплантации. У 2 из 5 пациентов, которым был наложен анастомоз между аномальной коронарной артерией и подключичной артерией, развились выраженный стеноз и компенсаторные коллатерали. Авторы считают прямую имплантацию аномальной левой коронарной артерии в аорту лучшим методом лечения. Внутрилегочное туннелирование или шунтирование внутренней грудной артерией рекомендованы в случаях, когда аортальная имплантация невозможна по анатомическим причинам. Некоторым пациентам, выжившим после перевязки артерии, целесообразно провести формирование двойной коронарной системы в связи с риском смерти. Осложнениями операции Takeuchi явились надклапанный стеноз легочной артерии, фистулы в туннеле между коронарной артерией и легочной артерией и недостаточность аортального клапана. Dodge-Khatmai и соавторы показали, что почти 30% пациентов нуждаются в эндоваскулярном или хирургическом вмешательстве для устранения этих осложнений.
Согласно совокупным данным, охватывающим 109 вмешательств, 68 операций были выполнены детям в возрасте до 1 года и 41 – пациентам более старшего детского возраста. Общая смертность в группе младенцев составляла 28,4 %. Распределение младенцев по типу операций был следующим: пересадка левой коронарной артерии была осуществлена у 39 пациентов, перевязка – у 5, создание внутрилегочного туннеля – у 13, наложение анастомоза между левой подключичной артерией и левой коронарной артерией – у 16 пациентов. В период с 1985-1989 гг. летальность после пересадки левой коронарной артерии составляла 18% и после создания туннеля – 50%. В период с 1990 по 1994 гг. смертность после пересадки коронарной артерии составляла 21% и после туннелирования – 57%. Среди детей старшего возраста общая смертность составила 4,8%.
Уровень смертности в начале 1980-х годов был чрезвычайно велик – 75-80%. В наше время он снизился до 0-20%, при этом смертность от прямой реимплантации составляет 0-16 %, в то время как при использовании метода Takeuchi – 0-23%. Moodie и соавторы 20 лет назад сообщили, что в небольшой группе взрослых пациентов проходимость большой подкожной вены в течение 5,8 лет сохранялась у 80% больных. По разным причинам шунтирование с использованием v.saphena стало непопулярным.
Детский госпиталь в Торонто недавно представил данные о результатах лечения 47 детей, которым выполнена реимплантация коронарных артерий. До операции 10 младенцев нуждались в искусственной вентиляции и у 38 – имела место сердечная недостаточность. У 44 детей на ЭКГ выявлена ишемия миокарда. Фракция выброса по данным ЭхоКГ в среднем составляла 33%, что свидетельствовало о выраженном снижении сократимости левого желудочка. У всех, за исключением одного ребенка, была недостаточность митрального клапана различной выраженности. Фиброэластоз эндокарда по данным ЭхоКГ обнаружен у 92% больных. Аневризма или дискинезия левого желудочка была выявлена у 48% обследованных. Одному ребенку выполнена реконструкция митрального клапана. Госпитальная летальность составила 8 %. Пятеро детей нуждались в послеоперационной ЭКМО в течение 2-8 дней.
В отдаленном послеоперационном периоде в средние сроки 4,7 года не были зафиксированы отдаленные смерти. К 5 годам выжили 91% больных, в повторных операциях в течение 10 лет не нуждались 93%. В отдаленном послеоперационном периоде сократимость левого желудочка фактически нормализовалась: средняя фракция выброса повысилась до 64 ± 9% против 33 ± 21% до операции. Четверым пациентам была показана повторная операция: 3 – по поводу стеноза коронарного устья, 1 – по поводу надклапанного стеноза легочной артерии и выраженной митральной недостаточности.
Аналогичные данные опубликовали многие центры, которые констатировали нормализацию функции левого желудочка, тестов при физической нагрузке и решение проблемы выраженной миокардиальной гипоперфузии.
Sauer и соавторы исследовали факторы риска операций. Ими оказались малый возраст оперируемых, левый и сбалансированный тип коронарного кровообращения, ЭКГ-признаки обширного острого инфаркта миокарда и недостаточное развитие межартериальных анастомозов.
Некоторых младенцев не удается отлучить от искусственного кровообращения после создания двухкоронарной системы, так как левый желудочек скомпрометирован ишемическим процессом. Восстановление функции левого желудочка происходит в более поздние сроки после операции, что оправдывает настойчивые усилия по интраоперационной реабилитации сердца. Del Nido и соавторы из детского госпиталя в Бостоне показали, что механическая поддержка левого желудочка улучшает выживаемость детей с левожелудочковой дисфункцией после коррекции. Из 31 оперированного ребенка 26 были в возрасте от 6 нед до 9 мес. Семерых детей не удавалось отлучить от искусственного кровообращения. У этих детей была применена механическая поддержка левого желудочка центрифужным насосом в течение 2-70 ч. Один ребенок умер сразу после начала левожелудочковой поддержки, а 1 – от аритмии через 24 ч после деканюляции. У всех 5 выживших детей значительно улучшилась функция левого желудочка, из них 2 – нуждались в коррекции митральной недостаточности в отдаленном периоде.
Хирургическая тактика по отношению к недостаточности митрального клапана не выработана. По данным Института сердца Японии, из 29 пациентов с отхождением левой коронарной артерии от легочного ствола у 24 имела место недостаточность митрального клапана различной выраженности. Всем была произведена митральная анулопластика в области переднелатеральной комиссуры. Кардиоторакальный индекс и фракция выброса при выписке из стационара существенно не изменились, однако эти показатели нормализовались в отдаленном периоде. Дооперационная митральная недостаточность уменьшилась во всех случаях, кроме одного. Сходные отдаленные результаты получены хирургами, которые не проводили коррекцию митральной недостаточности.
Из приведенных выше данных можно сделать следующие выводы.
-
Отхождение левой коронарной артерии от легочного ствола является наиболее частой причиной инфаркта миокарда в детской популяции, а также одной из вероятных причин дилатационной кардиомиопатии.
-
Приоритетным хирургическим алгоритмом является формирование двухкоронарной системы.
-
Почти при всех вариантах аномального отхождения технически возможна пересадка коронарной артерии из легочной артерии в аорту.
-
В настоящее время хирургические результаты реимплантации коронарных артерий отличные, и только небольшая часть пациентов нуждается во вмешательстве на митральном клапане, поврежденном ишемией и инфарктом папиллярных мышц.
-
Функция левого желудочка почти полностью восстанавливается в ближайшие или средние сроки после операции.
-
Необходимо долгосрочное наблюдение за функциональным состоянием сердца и кровоснабжением миокарда.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания










Комментарии