Диагностика и лечение легочной гипертензии. Показания к операции.
Для больных с ЛГ характерны одышка, утомляемость, головокружение при нагрузке. У больных с синдромом Эйзенменгера в анамнезе выявляется застойная сердечная недостаточность в младенческом возрасте. Некоторые больные жалуются на головную боль и боль в сердце. На завершающей стадии естественного течения ЛГ появляются эпизоды кровохарканья и возникают фатальные профузные легочные кровотечения.
При ВПС симптомы ЛГ проявляются не сразу. У больных с ДМЖП, АВСД и шунтом слева направо клинически они характеризуются признаками объемной перегрузки легких и застойной сердечной недостаточностью. По мере прогрессирования ОБЛС наступает парадоксальное улучшение, обусловленное уменьшением лево-правого сброса крови. Со временем появляется и нарастает цианоз.
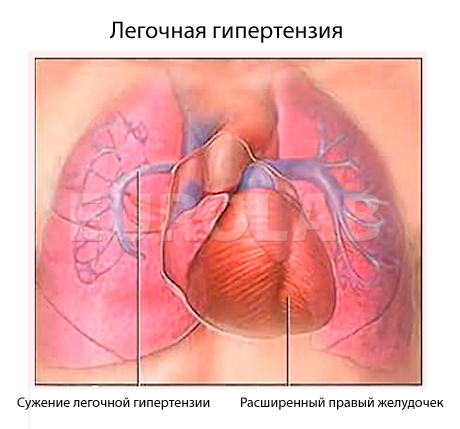
Диагностика легочной гипертензии
Неинвазивные методы
На ранней стадии развития ЛГ физические проявления могут быть слабо выражены. Обнаруживается увеличенный толчок правого желудочка, слышен Р2 компонент II тона. По мере прогрессирования гипертензии акцент II тона увеличивается, появляются шумы недостаточности трехстворчатого и легочного клапанов. Часто слышен ритм галопа и короткий шум систолического выброса над областью легочной артерии, а также щелчок выброса и широко расщепленный II тон.
На ЭКГ отмечается гипертрофия правого желудочка, которая точно указывает на повышение ЛСС при некоторых ВПС, таких, как ДМЖП. Однако при сложных пороках, например, единственном желудочке, по данными ЭКГ нельзя точно предсказать наличие ЛГ. ЭКГ часто в норме при умеренном повышении давления. При сопутствующем СЛА имеются признаки гипертрофии правого желудочка, которые переоценивают степень повышения давления в легочной артерии. При наличии блокады правой ножки пучка Гиса на ЭКГ диагноз гипертрофии правого желудочка затруднителен.
Повторные рентгенологические исследования дают наглядную информацию о динамике ЛГ. На примере большого ДМЖП можно видеть, что вначале, когда имеется застойная сердечная недостаточность из-за увеличенного легочного кровотока, сердце расширено, легочный сосудистый рисунок усилен. По мере прогрессирования ОБЛС размеры сердечной тени уменьшаются, легочный рисунок ослабевает. Тяжелая форма ЛГ характеризуется частичной нормализацией размеров сердца, выбуханием дуги легочной артерии и обеднением периферического сосудистого рисунка. Следует отметить, что у больных с ДМПП сохраняется кардиомегалия, несмотря на выраженную гипертензию. Это связано с расширением правого желудочка.
Эхокардиография является важным методом в оценке наличия и выраженности ЛГ. При двухмерной ЭхоКГ признаками ЛГ являются гипертрофия правого желудочка, уплощение межжелудочковой перегородки и смещение ее в сторону левого желудочка в систолу. Допплер-ЭхоКГ выводного тракта правого желудочка позволяет обнаружить у некоторых больных изменения времени изгнания правого желудочка. В легочной артерии отмечается увеличение степени систолического ускорения и укорочение времени ускорения при ЛГ. Измерение с помощью Допплер-исследования скорости трикуспидальной регургитации позволяет с большой точностью определить разницу пикового систолического давления между правым желудочком и правым предсердием на основе модифицированного уравнения Бернулли, и таким образом, судить о величине систолического давления в правого желудочка. Диастолическое давление в легочной артерии можно определить по скорости регургитации на клапане легочной артерии. При ДМЖП и ОАП модифицированное уравнение Бернулли позволяет по скорости кровотока на уровне лево-правого шунта определить градиент систолического давления. Вычитая величину градиента из систолического системного давления, можно получить численное выражение давления в легочной артерии.
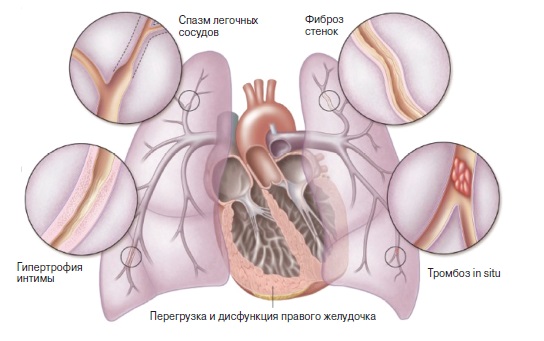
Инвазивные методы диагностики
Точная оценка тяжести ЛГ базируется на триаде методов исследований:
-
катетеризации сердца;
-
количественной ангиографии легочного микрососудистого русла;
-
биопсии.
Они позволяют определить степень ЛГ, реакцию на вазодилататоры и глубину структурных изменений легочных сосудов. Каждый из этих методов имеет ограниченную ценность, однако их комбинация дает достоверные данные о глубине ОБЛС, операбельности и обратимости ЛГ.
Катетеризация сердца проводится для уточнения анатомического диагноза ВПС, поставленного с помощью неинвазивныых методов, однако при ЛГ является обязательным элементом диагностического комплекса, особенно в случаях, когда предполагаемое давление в легочной артерии равно или приближается к системному. Катетеризация позволяет произвести точные гемодинамические измерения, включая сопротивление и реактивность легочных сосудов, оценить их структурные изменения. Катетеризация сердца у больных с тяжелой формой ЛГ сопровождается повышенным риском смерти во время процедуры.
В норме этот показатель составляет 1-3 ед/м2. Важно отметить, что измерение ЛСС заведомо неточно, так как компромиссно допускается, что вязкость постоянна, давление и кровоток являются непульсирующими и что объем притока в сосуд равен объему оттока. Эти допущения редко присутствуют в клинических условиях. Вязкость зависит от гематокрита, легочный кровоток обычно пульсирующий, и увеличенный бронхиальный коллатеральный кровоток сопровождает многие пороки. При измерении ЛСС необходимо учитывать влияние седации, гиповентиляции и гипоксии во время катетеризации. Легочно-сосудистое сопротивление, измеренное в этих условиях, не отражает истинного состояния легочного сосудистого русла вне лаборатории катетеризации.
Оценка реактивности легочных сосудов дает информацию об операбельности порока, возможности развития легочных гипертонических кризов в периоперационном периоде и сохраняющейся ЛГ после коррекции. Реактивность легочных резистивных сосудов и величину вазоконстриктивного компонента оценивают по изменению индекса легочного артериолярного сопротивления в ответ на применение вазодилататора. Имеется корреляция между пролиферацией интимы, полученной при биопсии легких, и ответом на вазодилататор. У пациентов с ЛГ обнаружены спонтанные вариации в течение 6-8 ч индекса ЛСС и давления в легочной артерии в пределах 6-13% и 8% соответственно.
Возможны 3 варианта реакции сосудов на вазодилатацию:
-
положительный ответ: снижение ЛСС и среднего давления в легочной артерии на 20% и более без изменения или с увеличением сердечного индекса;
-
отсутствие ответа: снижение ЛСС на 20% и более без заметного снижения среднего давления в легочной артерии;
-
отрицательный ответ: падение системного артериального давления более чем на 20% при снижении сердечного индекса или повышении давления в правом предсердии.
Классическим методом диагностики реактивности является оценка степени снижения давления в легочной артерии на ингаляцию высоких концентраций кислорода. Однако кислород может вызвать повышение системного сосудистого сопротивления и снижение сердечного выброса. Основные гемодинамические измерения выполняются при дыхании больного комнатным воздухом. В связи с этим заключение, основанное на реакции сосудов на ингаляционный кислород, бывает недостаточно объективным и используют также другие вазоактивные агенты – толазолин, изопротеренол, нифедипин, простациклин, амринон, АТФ.
Идеальный агент для краткого тестирования реактивности легочных артерий должен отвечать следующим требованиям:
-
преимущественно воздействовать на легочные сосуды;
-
иметь короткий период полураспада;
-
оказывать минимальное побочное действие;
-
обладать возможностью простой и быстрой доставки;
-
должен надёжно предсказать эффект длительного лечения оральными вазодилятаторами.
Таким идеальным агентом является ингаляционный NО, хотя последнее из перечисленных требований нуждается в подтверждении. Ингаляционный NО вызывает активную вазодилатацию без системной гипотензии путем увеличения уровня цГМФ. Могут быть использованы также другие агенты, повышающие содержание цГМФ, такие, как дипиридамол и предсердный натрийуретический пептид. К сожалению, фунциональные пробы, проводимые во время катетеризации сердца для определения эндотелийзависимой и независимой релаксации легочных сосудов с помощью сосудорасширяющих средств, недостаточно надежны, так как эндотелий не бывает нормальным у этих больных.
Некоторые центры в качестве теста создают кратковременную дыхательную гипоксию путем ингаляции 16% кислорода, так как отдельные больные с нормальным ЛСС в покое отвечают на гипоксию преувеличенной прессорной реакцией, свидетельствующей о вазоспастической готовности.
Ангиография периферического легочного артериального русла методом заклинивания вносит существенный вклад в оценку структурных изменений при гипертензионных состояниях. Этот метод был разработан в целях дооперационной оценки структурного состояния сосудистого русла легких. Он позволяет выявить и дать количественную оценку таким глубоким изменениям преацинарных артерий, например, в стадии Heath-Edwards III, как рассеянность арборизации легочного дерева, резкий обрыв сосудов, извитость и сужение мелких артерий, повышение прозрачности фона капиллярной фазы, скорость прохождения контрастного вещества через легкие, рефлюкс контраста. Баллонный катетер проводят в устье осевой артерии заднего базального сегмента нижней доли, вводят контрастное вещество и записывают на пленку в двух проекциях.
Оценивают степень заостренности артерий в форме свечи путем измерения длины сегмента, на протяжении которого диаметр просвета суживается с 2,5 мм до 1,5 мм. Резкое заострение артерии свидетельствует о более выраженных изменениях интраацинарных артерий, пропорциональных морфологическим и морфометрическим стадиям вышеприведенных классификаций. У некоторых больных в поздних стадиях ЛГ отмечается равномерное сужение просвета по ходу сосудов вместо резкого сужения, похожего на свечу. Хирургическое суживание легочного ствола или легочный стеноз снижают диагностическую ценность этого метода.
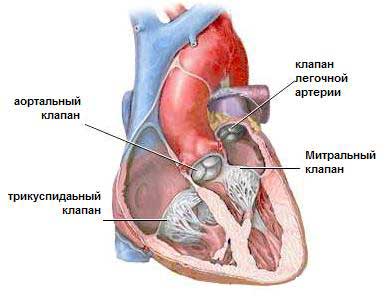
Корреляция гемодинамических и морфологических изменений
Тесная связь морфологических и функциональных показателей делает биопсию легких важным диагностическим методом, особенно при принятии решений в пограничных случаях.
Выделяют три морфогемодинамические стадии:
-
Стадия А характеризуется аномальным распространением мускуляризации на мелкие периферические артерии или утолщением стенки в норме мышечных сосудов не более чем в 1,5 раза в сравнении с нормой. У этих пациентов увеличены легочный кровоток и пульсовое давление, но среднее давление в легочной артерии остается нормальным. При электронной микроскопии легочного биоптата показано, что эти изменения обусловлены ранней дифференциацией незрелых гладкомышечных клеток в немышечных отделах артерий и промежуточных клеток в частично мышечных отделах.
-
В стадии В, как и в предыдущей стадии, мышечная ткань распространяется на периферию, однако при этом имеет место более выраженная гипертрофия медиального слоя нормальных мышечных артерий. Когда медиальный слой утолщается более чем в 1,5 раза, но менее чем в 2 раза по сравнению с нормой, всегда имеется ЛГ. Если толщина медиального слоя более чем в 2 раза превышает норму, давление в легочной артерии больше половины системного давления. Утолщение среднего слоя стенки артерий обусловлено как гипертрофией, так и гиперплазией гладкомышечных клеток, а также увеличением количества межклеточного соединительнотканного белка.
-
В стадии С плотность распределения артерий и их размер уменьшаются. У больных с этими морфологическими изменениями ЛСС превышает 3,5 ед/м2. В случаях, когда количество артерий уменьшено более чем вдвое, ЛСС превышает 6 ед/м2. Стадия С развивается вследствие нарушения роста новых артерий и уменьшения количества уже заложенных артерий. Морфометрические стадии А и В детализируют стадию Heath-Edwards I. Стадия С отражает отличные от классификации Heath-Edwards морфологические признаки, которые имеют важное функциональное значение. Стадия С может быть обнаружена у больных одновременно с изменениями Heath-Edwards I, часто имеет место при стадии II и всегда при стадии III.
Существует тесная связь между морфометрическими данными и степенью нормализации давления в легочной артерии после операции. У пациентов со стадией А и начальной стадией В в раннем послеоперационном периоде давление в легочной артерии нормальное или слегка повышенное. У большинства больных с более тяжелой степенью гипертрофии медии давление в легочной артерии повышенное и лабильное и почти всегда поддается лечению. Наличие и тяжесть ЛГ в раннем послеоперационном периоде абсолютно предсказуемы, когда имеются более выраженные изменения в биоптате, то-есть уменьшенное количество артерий и гиперплазия интимы.
Через год после операции у пациентов, оперированных в течение первых 8 мес. жизни, отмечается нормальное давление в легочной артерии вне зависимости от тяжести сосудистых изменений в легочных биоптатах, то же наблюдается у больных разных возрастов, имеющих выраженную стадию В и Heath-Edwards I. Когда хирургическая коррекция порока произведена между 9 мес. и 2 годами жизни у пациентов с изменениями легочных сосудов, соответствующих стадии С и Heath-Edwards II или III, после операции постоянно сохраняется повышенное ЛСС. После 2-летнего возраста остаточная ЛГ неизбежна.
Количественная оценка замороженных биоптатов применяется также в качестве экспресс-диагностики, чтобы помочь хирургу во время операции сделать выбор между паллиативной и корригирующей операциями, когда гемодинамические данные пограничные либо их трудно получить и интерпретировать. Метод позволяет также предсказать даже небольшое повышение ЛСС, что особенно важно при планировании операции Fotan у пациентов с трикуспидальной атрезией с ранее выполненным системно-легочным анастомозом или у больных с единственным желудочком сердца после суживания легочной артерии. Даже минимальные изменения сосудов в легочном биоптате могут стать причиной осложнений после операции Fotan, требующих продолжительного пребывания в стационаре из-за необходимости длительной вентиляции и дренирования плевральных полостей.
Показания к операциям при ВПС, осложненных ЛГ
Выживаемость больных после анатомической коррекции пороков с ЛГ во многом зависит от выраженности изменений легочных сосудов. Повышенная летальность отмечается в случаях, когда ЛСС превышает 8-10 ед/м2 индекса Wood, отношение ЛСС к системному сопротивлению больше 0,7:1 и ЛСС при гипероксическом тесте снижается менее чем на 3 ед/м2. У перенесших хирургические вмешательства больных, имевших приведенные показатели, ЛСС не снижается и даже имеет тенденцию к повышению в отдаленном периоде. При пороках с анатомически или функционально единственным желудочком, у которых выполняется операция Fotan, для обеспечения неосложненного послеоперационного и отдаленного течения больных, давление в легочной артерии не должно превышать 20 мм рт. ст. и ЛСС должно быть в пределах от < 2 до 4 ед/м2 KW.
Комплекс параметров, получаемых при катетеризации и даже биопсии, не является абсолютно надежным при принятии решений, тем более что не все методы инструментальных исследований всегда доступны по разным причинам. Например, морфологические данные достоверны лишь при взятии биоптатов из различных участков легких, что технически трудновыполнимо. Биопсия является агрессивным методом для маленьких детей. Если микроскопические исследования дают определенные критерии для определения операбельности больных, то они непригодны для диагностики реактивности легочных сосудов и прогнозирования послеоперационных легочных гипертонических кризов.
Данные катетеризации сердца также имеют относительную ценность из-за приведенных выше допущений при использовании уравнения Пуазейля. Кроме того, ЛСС вычисляется на основании недостаточно точных замеров нескольких показателей. Соединение неточных величин в одном уравнении может дать ложный результат, поэтому комплекс методов и комбинация многих параметров позволяют в пограничных случаях принять верное решение в пользу операции или отказа от нее.
С этой точки зрения большую информационную ценность имеют общеклинические признаки объемной перегрузки левого желудочка и операбельности:
-
застойная сердечная недостаточность;
-
отсутствие признаков цианоза в покое и при нагрузке, симптоме барабанных палочек, повышения содержания гемоглобина;
-
увеличение размеров сердца на рентгенограмме, застойные корни и усиленный рисунок легочных полей без признака «обрубленных» корней;
-
увеличение конечно-диастолического объема левого желудочка на ЭхоКГ. Важно вычислить ударный объем путем вычитания конечно-систолического объема из КДО и минутный объем. Сравнение минутного объема, отнесенного к поверхности тела, с нормой для идентичных возрастных и весовых параметров позволяет вычислить приблизительную величину сброса крови;
-
увеличение размеров левого предсердия, наличие лево-правого сброса на ЭхоКГ;
-
громкий систолический шум в отсутствие сопутствующих аортального, легочного стеноза и недостаточности митрального клапана указывает на наличие сброса крови и градиента давления между камерами сердца. Для операбельных больных характерен высокочастотный лентовидный или веретенообразный шум, занимающий всю систолу. Короткий убывающий тихий шум в первой половине систолы или его отсутствие – признак отсутствия градиента давления при большом дефекте. В этом случае необходимо уточнение операбельности по данным катетеризации и биопсии. У некоторых больных с ДМЖП на верхушке выслушивается мягкий диастолический шум, отражающий относительное сужение митрального клапана в условиях увеличенного притока крови в левое предсердие;
-
на ЭКГ – признаки гипертрофии левого желудочка или комбинированной перегрузки левого и правого желудочков при ДМЖП;
-
капиллярное насыщение по пульсоксиметру в покое и при дозированной нагрузке, превышающее 93%;
-
насыщение кислородом крови в пробе, взятой при пункции артерии не ниже 94-95%. К этому методу прибегают при сомнительных результатах катетеризации сердца и аорты;
-
повышение давления в левом предсердии при интактной межпредсердной перегородке и нормальном конечно-диастолическом давлении при катетеризации.
Важными клиническими признаками ЛГ и неоперабельности являются плохое питание и резкое отставание в весе, особенно характерное для пациентов с ЛГ и цианозом. Эти признаки должны насторожить врача и понудить его к получению свежей исчерпывающей информации.
Окончательное решение принимается в операционной. Внешним благоприятным признаком гиперволемии является расширение правых легочных вен при условии отсутствия сопутствующей недостаточности митрального клапана. Интубационный наркоз с вентиляцией смесью воздуха с кислородом позволяют провести дополнительное исследование способности легочных сосудов к дилатации. Для этого перед перфузией мы измеряем давление в легочной артерии и набираем пробы крови из правого предсердия и легочного ствола. В операбельных случаях давление в легочной артерии на 10-15 мм рт. ст. ниже, а артериовенозная разница по кислороду выше дооперационного уровня. В сомнительных случаях применяем пробное суживание легочной артерии. Снижение давления периферийнее тесемки и повышение системного давления при неизмененном капиллярном насыщении кислородом по пульсоксиметру оправдывает закрытие дефекта.
Ранние вмешательства улучшают выживаемость детей с ВПС, осложненными ЛГ. Наиболее благоприятный возраст для операций зависит от характера порока. Так, коррекцию общего артериального ствола безопаснее всего осуществить в течение 1-го месяца жизни, при большинстве пороков операция должна быть выполнена до 9-месячного возраста, при ДМЖП – до 2-летнего возраста, хотя в отдельных случаях ОБЛС может развиться уже в течение первых месяцев жизни. При ДМПП легочная гипертензия в детском возрасте развивается редко. Тем не менее, наблюдаются отдельные случаи неоперабельной ЛГ уже в возрасте 8-9 лет. Для взрослых пациентов с ДМПП и такими осложнениями естественного течения порока, как аритмии, застойная сердечная недостаточность и ЛГ, отсутствуют абсолютные противопоказания к операциям. Для больных с АВСД характерно раннее развитие необратимых изменений легочных сосудов. Операции должны быть выполнены раньше, чем при ДМЖП, особенно при сопутствующем синдроме Дауна. Пациентам с ЛГ, подлежащим операции Fontan, уже в течение 1-го месяца жизни должно быть выполнено суживание легочной артерии, так как низкое ЛСС является принципиальным условием успеха на последующих этапах лечения.
Решение об оптимальном времени коррекции порока следует принимать индивидуально.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания









Комментарии