Оланзапин и Хлорпромазин: применение препаратов при шизофрении
Несмотря на широкое применение хлорпромазина, опубликовано довольно мало сравнительных исследований хлорпромазина и атипичных антипсихотических препаратов. Проведенные сравнения хлорпромазина с клозапином, оланзапином и кветиапином не зафиксировали явного превосходства атипичных препаратов. В ходе исследования пациентов, страдающих терапевтически резистентной формой шизофрении, число больных, продемонстрировавших улучшение суммарного балла по краткой психиатрической оценочной шкале на 20, 30 и 40%, в разных терапевтических группах не различалось. Кроме того, не наблюдали также различий между группами по изменениям усредненного суммарного балла за неделю по шкале BPRS или другим основным критериям оценки эффективности препаратов.
Сравнение эффективности препаратов при шизофрении
В рамках этого исследования оланзапин переносился лучше, при этом достоверно большее число пациентов, получавших хлорпромазин, испытывали такие побочные эффекты, как сухость во рту, ЭПС, ортостатические изменения и неустойчивая походка.
Материалы и методы
Проведен полный анализ четырех 6-недельных рандомизированных открытых параллельных исследований.
Обследуемая группа пациентов
В исследовании принимали участие амбулаторные и стационарные пациенты, страдающие шизофренией, мужского и женского пола в возрасте от 18 до 55 лет. Все пациенты были психически способны пройти все тесты и осмотры согласно протоколу, при этом их состояние соответствовало суммарному баллу по шкале BPRS>42 и баллу >4 по шкале общей клинической оценки тяжести заболевания как в ходе визита 1, так и в ходе визита 2. Исходный суммарный балл по шкале BPRS был извлечен из шкалы позитивных и негативных синдромов, показателям которой были присвоены баллы от 1 до 7.
Были приняты следующие критерии исключения:
- серьезное, нестабильно протекающее заболевание или диагноз злоупотребления психоактивными веществами или зависимости от них по DSM-IV в течение последних 3 мес;
-
соображения безопасности;
-
участие в клиническом испытании другого лекарственного препарата в течение 1 мес. перед регистрацией в данном исследовании;
-
лечение инъекционными депо-формами нейролептических препаратов, если с момента последней инъекции до регистрации в данном исследовании прошло менее 1 интервала дозы.
Протоколы данного исследования были утверждены наблюдательными советами по этике, исследование проведено в соответствии с Хельсинкской декларацией. После подробного разъяснения хода исследования и возможных побочных явлений каждый пациент подписал документ о согласии на участие в данном исследовании.
План исследования и медикаменты
Исследование состояло из таких частей:
1) от 2 до 9 дней – период скрининга и выведения принимавшегося ранее нейролептика;
2) срочная 6-недельная открытая терапия продолжение открытого маркированного исследования на неопределенный срок для респондеров к терапии оланзапином.
В течение первого периода исследования пациенты должны были пройти минимальный срок “отмывки” для выведения нейролептического препарата, который они принимали ранее. В ходе срочного открытого маркированного периода исследования, допущенные к нему пациенты были рандомизированы по группам в соотношении 2:1 на прием оланзапина или хлорпромазина. Пациенты, которым был назначен оланзапин, начали получать этот препарат в дозировке 10 мг/сут. В случае недостаточной клинической эффективности препарата суточная доза оланзапина могла быть скорректирована с помощью 5 мг приращений в пределах установленного диапазона дозировки, но не чаще, чем через 7 дней после последнего изменения дозировки. Для коррекции дозы хлорпромазина установленное максимальное увеличение дозы в неделю составляло 200 мг. Снижение дозировки вследствие возникновения побочных явлений могло иметь место в любое время на любое число 5 мг уменьшений дозы для оланзапина и любое число 25 мг уменьшений дозы для хлорпромазина. Пациентов, у которых была выявлена непереносимость минимальной дозы оланзапина или хлорпромазина, исключали из дальнейшего участия в исследовании. В целом применение сопутствующих медикаментов, действующих главным образом на центральную нервную систему, в ходе данного исследования не допускали. Использование бензодиазепинов было разрешено при условии, что их суточная доза не превышала эквивалент 60 мг диазепама и несколько препаратов этой группы не принимались одновременно.
Респондеры к терапии оланзапином, завершившие период 2 данного исследования, могли продолжить лечение оланзапином на неопределенный срок – пока препарат будет зарегистрирован и поступит в продажу в стране их проживания, либо до тех пор, пока финансирующая сторона примет решение о завершении исследования.
Оценка эффективности
Все сотрудники клинических баз исследования, проводившие оценку состояния пациентов, были обучены пользованию всеми оценочными шкалами, применяемыми в данном исследовании.
Оценка переносимости
Частоту возникновения и тяжесть проявления нежелательных побочных явлений, развившихся в ходе лечения, оценивали в ходе каждого посещения со слов пациента, а также при помощи структурированной шкалы оценки побочного действия, Udvalg for Kliniske Undersgelser.
В ходе каждого посещения фиксировали:
данные клинической биохимии, показатели жизнедеятельности и массу тела;
данные электрокардиоконтроля регистрировали в начале и конце исследования;
содержание электролитов в крови, гематологические показатели и анализ мочи – при регистрации, назначении препаратов и по окончании исследования.
Статистический анализ
Основной задачей данного исследования являлась оценка эффективности и переносимости оланзапина в сравнении с хлорпромазином в лечении пациентов, страдающих шизофренией. Основным критерием оценки эффективности являлось среднее изменение результирующего суммарного балла по шкале BPRS по сравнению с исходным.
Для анализа категориальных данных использовали точный тест Фишера, при этом во внимание принимались исходные демографические характеристики, распределение пациентов, побочные явления и изменения ЭКГ, развившиеся в ходе лечения, а также качественные изменения данных лабораторных анализов. Метод LOCF применяли для анализа основных и дополнительных критериев оценки эффективности препаратов, а также средних изменений между исходными и результирующими данными лабораторных анализов, показателей жизнедеятельности и массы тела, в то время как для выявления изменений суммарного балла по шкале BPRS в ходе каждого посещения был использован метод анализа наблюдаемых случаев. Все средние показатели динамики баллов по шкалам оценки эффективности препаратов, а также ее зависимости от страны проведения исследования оценивали с помощью модели дисперсионного анализа, включавшей в себя препарат, страну проведения исследования и взаимосвязь “препарат-страна”. Модель ANOVA, включающая в себя препарат и страну проведения исследования, использовалась для оценки постоянных демографических данных, изменения суммарного балла по шкале BPRS в ходе каждого посещения, а также средних изменений в данных лабораторных анализов, показателей жизнедеятельности и массы тела. Тест Кокрана-Мантеля-Гензеля, скорректированный в соответствии со спецификой каждой страны, использовали для сравнения уровня реакции на исследуемые препараты и изменения массы тела более чем на 7% по сравнению с исходной. Для анализа разности результирующих и максимальных баллов по сравнению с исходными по показателям шкалы или были проведены тесты Мантеля-Гензеля для порядковых данных. Описанный подход позволил:
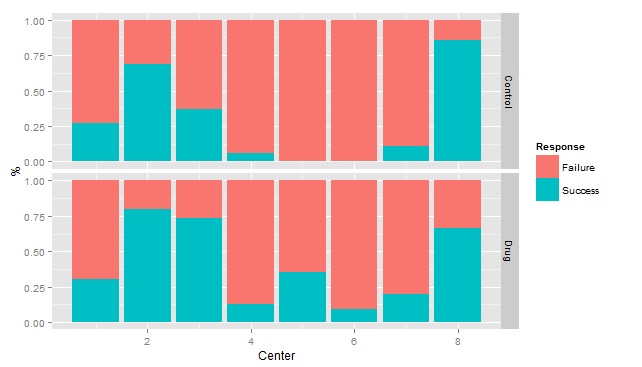
-
исследовать связь между принимаемым препаратом и разностью максимальных показателей по сравнению с исходными и оценить величину изменения показателей;
-
сравнить изменения максимальных баллов по шкале UKU с исходными в обеих терапевтических группах.
Во всех случаях для проверки гипотез использованы двусторонние критерии при 5% уровне значимости, за исключением гипотез относительно взаимосвязи “препарат-страна”, для проверки которых использованы двусторонние критерии при 10% уровне значимости. Для проведения всех анализов использовали программное обеспечение SAS.
Результаты
Исследование проводили в медицинских центрах университетов и стационарах в Турции, Объединенных Арабских Эмиратах, Египте и Марокко. Основные результаты исследования HGCQ были опубликованы Kostacoglu и соавт., в то время как промежуточные результаты исследования HGDT были представлены Loza и соавт. и упомянуты в обзоре.
Для участия в исследовании были зарегистрированы 126 пациентов, 123 из которых были рандомизированы на прием оланзапина или хлорпромазина. Эффективность препаратов оценивали по результатам наблюдения 117 пациентов. В исходных демографических характеристиках пациентов существенных различий не наблюдалось. Большинство пациентов, данные которых удалось проанализировать, имели диагноз “шизофрения параноидного типа”.
Число пациентов, полностью прошедших курс лечения в рамках данного исследования, в исследуемых группах не было существенно различным; хлорпромазин, 32/40; p=0,065. В целом 4 пациента выбыли из исследования вследствие возникновения побочных явлений.
Средние модальные дозы препаратов составляли 14,9 мг/сут оланзапина и 433,1 мг/сут хлорпромазина. 54 пациента получали сопутствующие медикаменты; хлорпромазин, 17/40. Единственным существенным различием между группами в отношении использования сопутствующих медикаментов было применение тригексилфенидила; хлорпромазин, 0/40; р=0,030.
Эффективность
Пациенты, принимавшие оланзапин, продемонстрировали достоверно более значительное улучшение по основному критерию оценки эффективности – среднему изменению результирующего суммарного балла по шкале BPRS по сравнению с исходным, чем пациенты, принимавшие хлорпромазин. Пациенты группы оланзапина показали достоверно более значительное улучшение по суммарному баллу шкалы BPRS, чем пациенты группы хлорпромазина уже через 2 нед после начала лечения, и в течение всего исследования в группе оланзапина эти баллы продолжали достоверно улучшаться.
Кроме того, у пациентов, принимавших оланзапин, зафиксировано достоверно более значительное улучшение по позитивным и негативным показателям шкалы BPRS, суммарному баллу шкалы РАБ и всем ее подшкалам, а также по показателям шкалы CGI-S, чем у пациентов, принимавших хлорпромазин. Состояние, оцениваемое баллами подшкалы CGI-I “значительное улучшение” и “существенное улучшение”, наблюдали у большего числа пациентов группы оланзапина, чем у пациентов группы хлорпромазина. Реакцию на получаемый препарат наблюдали у значительно большего числа пациентов группы оланзапина, чем у пациентов, принимавших хлорпромазин.
Взаимосвязь “препарат-страна” оказалась значимой для динамики негативной симптоматики как по шкале РАЖБ, так и по шкале BPRS. Для других критериев эффективности взаимосвязь “препарат-страна” не прослеживалась. Пациенты группы оланзапина в Египте, ОАЭ и Марокко продемонстрировали улучшение по негативным показателям шкал BPRS и РАБ по сравнению с пациентами, принимавшими хлорпромазин, при этом результаты лечения пациентов в Марокко показали достоверное различие между этими группами. В Турции наблюдали обратный эффект в отношении баллов по негативным показателям шкал BPRS и РАБ, так как пациенты группы хлорпромазина показали численно большее улучшение, чем пациенты группы оланзапина.

Переносимость
Общая оценка побочных явлений, развившихся в период лечения
Из всех побочных явлений, наблюдавшихся у более 5% пациентов обеих групп, только постуральная гипотензия проявлялась достоверно различно в разных терапевтических группах, при этом пациенты группы хлорпромазина испытывали этот побочный эффект чаще, чем пациенты группы оланзапина. Увеличение массы тела было единственным распространенным побочным явлением, наблюдавшимся чаще в группе оланзапина. Кроме того, распространенные побочные явления включали тремор и сухость во рту, акатизию и постуральную гипотензию. В целом 4 пациента испытывали серьезные побочные явления:
-
у 1 пациента, принимавшего оланзапин, зафиксированы депрессия, суицидальная попытка и намеренная передозировка оланзапина;
-
2 других пациента группы оланзапина испытывали враждебность или психоз.
Серьезные побочные явления – гипогликемия и инфаркт миокарда – наблюдали лишь у 1 из пациентов, получавших хлорпромазин.
Оценка побочных явлений, развившихся в ходе лечения, по шкале UKU
По результатам исследования зафиксированы достоверные различия между группами пациентов в изменениях результирующих баллов по сравнению с исходными или по следующим показателям шкалы UKU:
-
нарушения концентрации;
-
астения/вялость/повышенная утомляемость;
-
сниженное слюноотделение;
-
ортостатизм и усиленное потоотделение.
Увеличение этих показателей по завершении исследования наблюдали у меньшего числа пациентов группы оланзапина, чем у пациентов группы хлорпромазина. Кроме того, достоверные различия между двумя исследуемыми группами пациентов наблюдались и в разности между исходными и максимальными баллами по шкале UKU: сниженное слюноотделение, ортостатизм и уменьшение продолжительности сна. У меньшего числа пациентов, принимавших оланзапин, по сравнению с пациентами группы хлорпромазина, наблюдали увеличение баллов по следующим показателям: сниженное слюноотделение и ортостатизм. Большее число пациентов группы оланзапина показали снижение максимального балла по сравнению с исходным по уменьшению продолжительности сна, чем пациенты группы хлорпромазина.
Экстрапирамидные симптомы
Изменение максимального балла по сравнению с исходным по показателям подшкалы оценки неврологических побочных эффектов шкалы ики в обеих группах достоверно отличалось по акатизии. Снижение баллов по акатизии наблюдали у 6/74 пациентов, получавших оланзапин, и у 1/36 пациентов, получавших хлорпромазин, в то время как рост этого показателя был отмечен у 3/74 пациентов группы оланзапина и 7/36 пациентов группы хлорпромазина. Разность исходных и результирующих баллов по показателям подшкалы оценки неврологических побочных эффектов шкалы UKU в двух исследуемых группах пациентов достоверно не отличалась.
Обсуждение
Проведенный обобщенный анализ четырех 6-недельных рандомизированных открытых маркированных исследований показал, что по сравнению с пациентами группы хлорпромазина пациенты группы оланзапина продемонстрировали достоверно большее улучшение показателей как по основному, так и по большинству дополнительных критериев оценки эффективности препарата. Кроме того, оланзапин хорошо переносился пациентами и по показателям большинства критериев оценки переносимости препаратов сравним с хлорпромазином.
Эффективность
В ходе данного исследования установлено, что у пациентов, принимавших оланзапин, наблюдали достоверно более значительное улучшение по показателям основного критерия оценки эффективности препарата, чем у пациентов группы типичного препарата сравнения. Этот результат сопоставим с данными метаанализа, в ходе которого сравнивали оланзапин с типичным антипсихотическим препаратом галоперидолом. Результаты указанного метаанализа свидетельствуют о том, что пациенты, принимавшие оланзапин, показали достоверно более значительное улучшение по всем критериям оценки эффективности препарата, а именно суммарным баллам по шкалам BPRS и PANSS, а также по 5 показателям шкалы PANSS. Кроме того, согласно недавно опубликованной статье, в которой приводятся результаты Клинического исследования эффективности антипсихотической терапии, оланзапин оказался в численном выражении более эффективным, чем типичный антипсихотик перфеназин, по основному параметру исхода – выбыванию пациентов из исследования по различным причинам, и значительно более эффективным по параметру выбывания из исследования по причине недостаточной эффективности препарата. Хотя результаты исследования CATIE и метаанализа не могут быть непосредственно сравнены с результатами данного исследования, они тем не менее являются свидетельством в пользу большей эффективности оланзапина по сравнению с типичными антипсихотическими средствами в лечении пациентов, страдающих шизофренией.
Переносимость
Аналогично результатам нашего исследования такие нежелательные побочные явления, как увеличение массы тела и сонливость, отмечены и в ходе проведения метаанализа, сравнивавшего оланзапин с галоперидолом и плацебо. Такие побочные явления, как гипотензия и тремор, наблюдавшиеся у пациентов группы хлорпромазина, зафиксированы как в ходе данного исследования, так и в обзоре Cochrane, сравнивающем хлорпромазин и плацебо. Наблюдения относительно увеличения массы тела среди пациентов группы оланзапина сопоставимы с общеизвестным профилем безопасности оланзапина и подтверждают итоги предшествующих исследований. Согласно обзору данных по увеличению массы тела, обусловленному приемом антипсихотических препаратов, среднее увеличение массы тела среди пациентов, получавших оланзапин, составило 4,15 кг после 10 нед лечения. По данным недавно опубликованного исследования CATIE, средняя прибавка массы тела среди пациентов группы оланзапина составила 0,9 кг/мес, что превышало аналогичные показатели в других группах. Кроме того, в ходе исследования CATIE у большей части пациентов, получавших оланзапин, зарегистрировано увеличение массы тела более чем на 7% по сравнению с исходной, чем у пациентов, принимавших другие препараты. В данном исследовании у 26,3% пациентов группы оланзапина зарегистрирована прибавка массы тела на более чем 7% по сравнению с исходной. С другой стороны, исследования, проведенные еще в 1964 г., свидетельствуют о том, что значительное увеличение массы тела может быть связано и с применением хлорпромазина.
По результатам представленного исследования единственным достоверным различием между группами пациентов по ЭПС была разность максимального и исходного баллов по акатизии. Возможные объяснения отсутствия других достоверных различий в проявлении ЭПС между исследуемыми группами пациентов могут состоять в том, что шкала UKU не является наиболее чувствительным инструментом оценки ЭПС, или же в том, что оптимальные дозы хлорпромазина, низкопотентного типичного антипсихотического средства, не могут быть связаны с более выраженным проявлением ЭПС, чем применение атипичных антипсихотических средств.
В ходе данного исследования у пациентов, получавших оланзапин, зафиксированы достоверно меньшие средние изменения результирующих показателей содержания глюкозы в крови по сравнению с пациентами группы хлорпромазина. Это наблюдение идет вразрез с результатами предшествующих исследований, предметом которых были атипичные антипсихотические препараты и их возможное влияние на изменения обмена веществ, и может быть связано с относительно малой продолжительностью данного исследования, а также с ограничениями, налагаемыми спецификой анализа содержания глюкозы в крови.
Результаты данного исследования свидетельствуют о том, что лечение оланзапином по сравнению с хлорпромазином может быть более эффективным и иметь более благоприятный профиль безопасности при лечении пациентов, страдающих шизофренией. Принимая во внимание широкое применение хлорпромазина в странах Ближнего Востока и Северной Африки, а также других регионов мира, данное исследование имеет большое значение для психиатрической практики, так как при индивидуальном назначении терапии лечащему врачу необходимо учитывать соотношение факторов риска и терапевтического эффекта назначаемых медикаментов.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания










Комментарии