Смерть мозга. Критерии смерти мозга. Смерть мозга у детей
Первое описание прекращения функций головного мозга, использующее концепцию, схожую с современным определением смерти мозга, появилось в 1959 г., хотя тема стала более неоднозначной после развития трансплантации органов. Критерии для констатации смерти мозга были впервые опубликованы в 1968 г., год спустя после первой трансплантации сердца. При том, что культурное и религиозное разнообразие может приводить к большим различиям в отношении к смерти мозга, и нет глобального согласия по диагностическим критериям, широко принята концепция смерти мозга, как определяющая смерть человека. Многие страны опубликовали рекомендации или юридические требования для диагностики смерти мозга, в частности, как необходимое условие при донорстве органов.
Традиционная концепция смерти использовала в качестве своей основы прекращение сердечной и дыхательной функций из-за принятия простых и немедицинских понятий: что жизнь начинается с первым вдохом после рождения, что смерть наступает после последнего выдоха и что сердечная деятельность прекращается в течение нескольких минут после последнего выдоха. Напротив, современная концепция смерти мозга принимает выводы современной биологической науки (теория мозга, как центрального интегратора):
-
что центральная нервная система (ЦНС), включающая ствол мозга, является контролирующим центром для живого организма;
-
что прекращение функций ЦНС представляет прекращение гармонии жизни;
-
что без контроля ЦНС живой организм – это не более чем скопление живых клеток.
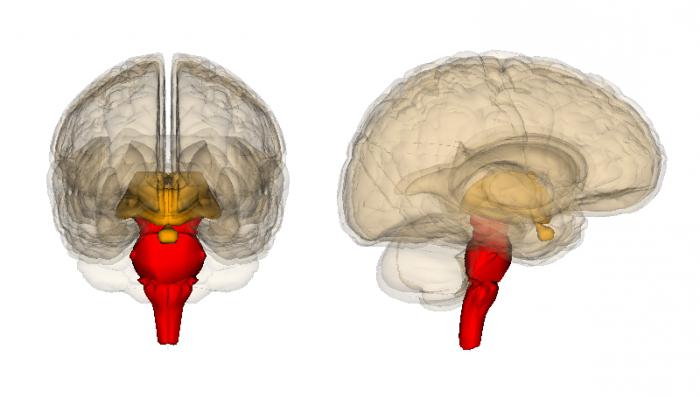
Однако это понятие стало спорным, потому что не все пациенты со смертью мозга неизбежно ухудшаются до остановки кровообращения за короткое время, и они могут усваивать питательные вещества, бороться с инфекцией, заживлять раны и вынашивать беременность.
Травма мозга или цереброваскулярное повреждение вызывают отек мозга. Из-за того, что мозг покрыт твердыми костями черепа, отек сопровождается повышением внутричерепного давления, которое, если достаточно высокое, превышает артериальное давление. Когда прекращается мозговое кровообращение, наступает асептический некроз мозга. В течение от 3 до 5 дней мозг становится сжиженной массой. Такое повышенное внутричерепное давление сдавливает весь мозг, включая ствол мозга, и следует тотальный ишемический инсульт.
Клинические исследования указывают, что функции гипоталамуса и передней доли гипофиза до некоторой степени сохранены в течение определенного периода после наступления смерти мозга. После тотальной и необратимой потери функций ЦНС ответ иммунной системы на стимуляцию значительно изменяется. Гормональные изменения и воспалительные ответы после смерти мозга являются теоретической и научной основой гормональной терапии для гемодинамической стабилизации доноров органов с умершим мозгом.
В течение процесса смерти мозга после травмы головы или внутричерепного кровоизлияния внутричерепное давление повышается, и компрессия ствола мозга приводит к значительной гипертензии и брадикардии (феномен Кушинга). В самом начале смерти мозга вследствие образования тонзиллярной грыжи встречается внезапное снижение артериального давления, но артериальное давление постепенно возвращается к норме с помощью спинного мозга, проявляющего автоматизм.
Определение смерти мозга подтверждает необратимое прекращение всех функций всего мозга, включая ствол. Необратимость означает, что нельзя обоснованно ожидать, что какое-либо лечение изменит состояние. Хотя тестирование всех функций мозга концептуально невозможно, в практике прекращение всех функций мозга определяется отсутствием сознания, отсутствием ответов ствола мозга, апноэ и подтверждающими тестами.
Церебральная смерть, так называемое персистирующее вегетативное состояние, относится к прекращению функций коры мозга. Это не эквивалент смерти.
Верно, что культурные и религиозные различия могут влиять на понятие смерти. Существует значительная вариабельность политики и практики для определения смерти мозга на международном уровне и даже среди штатов и больниц.
Тесты для подтверждения смерти мозга включают электроэнцефалограмму, вызванные потенциалы и измерение кровотока.
Анестезиологи должны понимать медицинские и юридические определения смерти так же хорошо, как и этические понятия, стоящие за ними.
Поскольку достижения в медицине изменили определение и понятие смерти, законодательство также должно меняться соответствующим образом. Эта проблема следует за прогрессом в трансплантации органов и растущим числом пациентов с живым организмом, но нефункционирующим мозгом, которое является результатом открытий в методах реанимации и поддержания жизни. Такие усовершенствования в реаниматологии означают, что неврологи, нейрохирурги и анестезиологи должны быть в состоянии поставить соответствующий диагноз смерти. Хотя культурное и религиозное разнообразие может приводить к большим различиям в отношении к смерти мозга, и нет всеобщего согласия по диагностическим критериям, широко принята концепция смерти мозга, как определяющая смерть человека, и много стран опубликовали рекомендации или юридические требования для диагностики смерти мозга, как необходимого условия для донорства органов.
В 1902 г. Cushing первым сообщил о прекращении мозгового кровообращения, когда у обезьян внутричерепное давление превышало артериальное давление. Он также описал использование искусственной вентиляции с целью продления сердечной функции в течение 23 ч после прекращения спонтанного дыхания у пациента с опухолью головного мозга. В 1959 г. Bertrand и колл. сообщили о поддержании дыхания механическими средствами в течение 3 дней после смерти пациента со средним отитом, который перенес циркуляторный коллапс. Повторные судороги предшествовали глубокой коме. Аутопсия показала обширный некроз коры полушарий головного мозга и коры мозжечка, базальных ганглиев и ядер ствола мозга, который был приписан прекращению мозгового кровообращения во время искусственной вентиляции. Также в 1959 г. появилось первое описание прекращения функций мозга, использовавшее концепцию, схожую с современным определением смерти мозга (т.н. le coma depasse), сделанное Mollaret и колл.
Эти исторические сообщения поддерживают аргумент, что концепция смерти мозга независима от и была установлена до начала трансплантации органов от пациентов с умершим мозгом. Однако все еще идет спор о том, имеет ли смерть мозга прямое отношение к трансплантации органов или нет. Жаркое обсуждение смерти мозга началось после первой пересадки сердца, сделанной Barnard в 1967 г. Один год спустя специальный комитет Гарвардской Медицинской Школы для Изучения Определения Смерти Мозга издал свои критерии для смерти мозга и определил «необратимую кому, как новый критерий для смерти». Обсуждения комитета для определения смерти сосредоточились на формулировке «целый (весь) мозг», включающей все его отделы. В 1981 г. Президентская комиссия для исследования этических проблем в медицине, биомедицинских и поведенческих исследованиях определила мозг как «основной орган» и подтвердила использование определения «целого мозга» при смерти мозга в Соединенных Штатах. Формулировка «целого мозга» при смерти мозга была признана уставом в Законе об Универсальном Определении Смерти (UDDA), заявляя, что «человек, у которого сохраняется:
-
или необратимое прекращение функций кровообращения и дыхания;
-
или необратимое прекращение всех функций всего мозга, включая ствол мозга, мертв.”
Эта формулировка одна из обычно применяемых во всем мире и формирует основу для юридической кодификации во многих Западных странах. Многочисленные критерии по смерти мозга были предложены учреждениями, государственными органами, экспертными группами и правительствами.
Напротив, определение «ствола мозга» для смерти мозга было впервые объявлено в 1976 г. Конференцией Медицинских Королевских Колледжей и их Факультетов в Великобритании. Документ в 1995 г., названный «Критерии для Диагноза Смерти Ствола мозга», призывал использование более правильного термина смерть ствола мозга вместо смерть мозга и дал определение смерти, заявляя, что «смерть определяется как необратимая потеря способности к сознанию в сочетании с необратимой потерей возможности дышать».
Традиционная концепция смерти организма
В старину в Греции существовали две концепции относительно полости тела, где была размещена «основа жизни», теперь известная как «функция мозга». Одна от Платона, другая от Аристотеля. Платон первым постулировал тройственность души в «Государстве» и «Тимее». Первая часть – разум, вторая – эмоция, и третья – аппетит или желание. Разум, который мы можем сегодня назвать «сознанием», является повторным появлением души Бога (Всевышнего), размещен в сосуде идеальной формы, в котором все расстояния от центра одинаковые (т.е. в голове). Вторая душа, эмоция, расположена в сердце. Она оказывает влияние на кровообращение, и ее проявления, такие как частота пульса, являются функциями, которые коррелируют с тем, что мы представляем как вегетативную нервную систему. Шея построена как своего рода перешеек или граница между головой и грудной клеткой, чтобы гарантировать, что разум не окажется под влиянием эмоции. Третья часть души, т.е. аппетит к еде и питью или половое желание, является наименее благородной частью. Она была размещена в желудке, отделенная от сердца диафрагмой, и, как думали, была наказана горечью желчи. Однако мы не можем интерпретировать это слишком буквально, потому что это должна была быть своего рода аналогия для использования обычным гражданином. Платон представлял «смерть» отделением разума от смертного тела, тогда как Сократ в своей «Апологии» признался, что не знает судьбу разума после смерти. «Вегетативное состояние» в сегодняшней нейрофизиологии, согласно Платону, эквивалентно смерти.
В отличие от Платона Аристотель, который известен как отец-основатель генетики, подчеркивал опыт или эмпирическое знание вместо абстрактного мышления. Аристотель постулировал, что все функции головного мозга были размещены в сердце, которое он рассматривал как самый важный орган тела – место интеллекта и происхождения движения и ощущения. Другие органы, окружающие его, как мозг и легкие, существовали просто для охлаждения сердца. Аристотель вскрывал собак, лошадей, кузнечиков, сверчков и других живущих существ, чтобы понять причины, почему, например, собаки не могут родить лошадей. Он думал, что животные «готовят» продукты питания в их пищеварительных путях и, что кровь транспортирует питательные вещества к каждому органу от сердца. В современной нейрофизиологии этот транспорт соответствует электрическим сигналам в нервах. Согласно Аристотелю легкие охлаждают сердце, и череп служит охлаждающимся аппаратом для сжижения передатчика, своего рода «пневмы».
В системе Аристотеля носитель, который передает команды от центра контроля к периферическим органам и тканям, примерно эквивалентный электрическим сигналам нервной системы в сегодняшней нейрофизиологии, как предполагалось, был чем-то вроде пара или газа. Эта концепция является основой, из которой происходит идея «пневмы» (дыхание или дух). Бог создал человека (Адама) из пыли земной и вдохнул в его ноздри Дыхание Жизни, и стал человек живой душой. Позже Ева была создана из ребра Адама и с дыханием Бога также стала живой душой. Эта история может напомнить первый крик новорожденного, который является первым действием в жизни, вызванным «вдохом» Бога. Это созидающее дыхание или вдох, является предметом картины Боттичелли «Рождение Венеры», в которой Зефир, западный ветер, энергично дует, в то время как его жена Хлорис мягко несет свое теплое дыхание к Венере, которая стоит на раковине. Идея Аристотеля, постулирующая сердце как основное место духа, оказывала глубокое влияние на западную научную мысль в течение длительного периода. Открытие Уильяма Гарвея, описанное в его «Циркуляции Крови» (1628), рассматривается как заключительное научное развитие идей Аристотеля, а Аристотель – мыслитель, наиболее цитированный в книге Гарвея.
Во времена до известной истории мира потеря верхних конечностей означала потерю способности бороться и, следовательно, смерть человека. На протяжении этого доисторического периода могла развиваться концепция «смерти при потере конечности». То же самое верно для понятия «почечная смерть», поскольку в эпоху до появления гемодиализа/пересадки почки, тяжелая почечная дисфункция вызывала уремию, и смерть была неизбежна, так же как необратимое прекращение иммунных функций могло вызвать «иммунную смерть». Эти примеры показывают, что человеческое понимание смерти не обязательно должно быть однородным или универсальным и не было таковым на протяжении всей истории. Оно изменялось с различными периодами, областями, этикой и этапами продвижения технологического и научного прогресса. Смерть мозга должна обсуждаться отдельно от трансплантации органов, хотя последняя – важная проблема при рассмотрении понятий жизни и смерти.
Все живые организмы получают кислород с дыханием, доставляют кислород к периферическим тканям при помощи циркуляции крови, а затем удаляют метаболиты посредством кровообращения и через дыхание. Дыхание и кровообращение жизненно важны для живого организма. Дыхание – функциональная экспрессия ствола мозга, и прекращение функций ствола мозга приводит к прекращению дыхания. Поскольку ствол мозга поддерживает свою функцию за счет доставки кислорода и питательных веществ, прекращение кровообращения в конечном счете приводит к прекращению дыхания. Функции головного мозга, сердца и легких зависят друг от друга и разделяют основную роль в поддержании жизни. Организм умирает, когда одна из этих поддерживающих жизнь систем органов прекращает функционировать. Традиционная концепция смерти организма подчеркивала прекращение дыхания или кровообращения без рассмотрения роли головного мозга. Это происходило потому, что исследование функции мозга было нелегко выполнить. Когда искусственная вентиляция широко не использовалась, прекращение функций мозга было связано непосредственно с прекращением дыхания, и исследование функций ствола мозга было ненужным.
Концепция смерти мозга
Смерть мозга представляет смерть всего организма, а не просто смерть или некроз головного мозга в живом теле. Организм – это скопление живых клеток, хотя скопление живых клеток не обязательно составляет организм. Организм существует только тогда, когда совокупность клеток находится под контролем модулирующих систем, таких как:
-
центральная нервная система (ЦНС);
-
эндокринная система;
-
иммунная система.
После прекращения функционирования любой из этих систем смерть неизбежна, если не могут быть приняты искусственные меры. Физиологическое значение смерти мозга и смерти сердца по существу равно, и оба представляют необратимую потерю связи между контролирующим центром и периферическими клетками и тканями, так же как и потерю модуляции скопления клеток. Без этих систем прекращается гармоничное функционирование отдельных клеток как элементов целого организма. Поскольку полное и необратимое устранение иммунной или эндокринной функции не имеет практического значения, понятие эндокринной или иммунной смерти не развилось.
Ранее прекращение дыхания было эквивалентно немедленной смерти организма, но теперь искусственная вентиляция легких может продлить жизнь тела в течение определенного периода. Как полагают, у гипоталамуса и ствола мозга имеются различные функции – эндокринные, автономные и иммунные, так же как и другие, которые неизвестны. В стволе мозга также проходят главные тракты невральной коммуникации между контролирующим центром и периферическими тканями. Все двигательные эфферентные пути от полушарий должны пройти через ствол мозга, также как и все сенсорные афферентные пути, идущие к мозгу, кроме зрения и обоняния. Каждая из этих функций гипоталамуса и ствола мозга может быть точно проверена и обеспечена искусственно. Автономная дыхательная функция нижнего отдела ствола мозга представляет собой границу между жизнью и смертью, и потребность в механических устройствах для обеспечения функции дыхания определена как отражающая смерть человека. Возможно, большинство функций головного мозга, необходимых для жизни, может быть заменено компьютерами и лекарственными препаратами, и функции кровообращения сохранятся в течение многих месяцев или лет. Единственная функция, которая не может быть обеспечена передовыми технологиями, та, что составляет человечность или индивидуальность, которая, возможно, является продуктом конечного мозга.
Традиционная концепция смерти использовала прекращение сердечной и дыхательной функций как свою основу из-за принятия простых и немедицинских представлений – что жизнь начинается с первого вдоха после рождения, что смерть приходит с последним выдохом, и что сердечная деятельность прекращается в течение нескольких минут после последнего выдоха. В отличие от нее современная концепция смерти мозга принимает выводы современной биологии – что ЦНС, включая ствол мозга, является контролирующим центром для живого организма, что прекращение функций ЦНС представляет прекращение гармонии жизни, что без контроля ЦНС живой организм – не более чем скопление живых клеток.
Механизм смерти мозга
Повреждение головного мозга вызывается многими причинами, такими как травматическое или цереброваскулярное поражение и генерализованная гипоксия, все из которых приводят к отеку головного мозга. Основываясь на вовлеченных патологических механизмах, отек мозга классифицируется как вазогенный или цитотоксический. Поскольку редко работает исключительно только один механизм, обозначение «вазогенный» или «цитотоксический» относительно. Вазогенный отек вызывается увеличением цереброваскулярной проницаемости после утечки сывороточных белков в мозговую паренхиму (т.е. после деструкции гематоэнцефалического барьера). Химические медиаторы, такие как гистамин, серотонин, ангиотензин, брадикинин и простагландины, могут разрушить функцию гематоэнцефалического барьера. Цитотоксический отек мозга встречается при гипоксическом и ишемическом состояниях ,и следует из-за нарушения клеточной осморегуляции, процесс которой зависит, прежде всего, от функционирования энергозависимых ионных насосов. Нарушение осморегуляции увеличивает выход воды в мозговую паренхиму. Несмотря на то, что при чистой форме цитотоксического отека мозга гематоэнцефалический барьер остается в основном интактным, цитотоксический отек нарушает кровоток и вызывает гипоксию и вазогенный отек.
Отек головного мозга может быть сначала фокальным, но затем он распространяется по всему мозгу в прогнозируемой последовательности. Поскольку мозг находится в ригидной черепной коробке, его отек сопровождается увеличением внутричерепного давления, которое, если достаточно высокое, превышает артериальное давление. Когда прекращается мозговое кровообращение, наступает асептический некроз мозга. В течение 3-5 дней мозг становится сжиженной массой, данное состояние известно как респираторный мозг. Такое повышенное внутричерепное давление сжимает весь мозг, включая ствол, и следует полный ишемический инсульт.
Нейрофизиологическая основа смерти мозга
По определению смерть мозга – полное необратимое прекращение функционирования головного мозга. Однако смерть «целого мозга» не требует необратимого прекращения функционирования каждого нейрона мозга. Скорее, она требует только необратимого прекращения всех клинических функций мозга, а именно определяемых у постели больного при клиническом осмотре. Головной мозг включает все структуры ЦНС, кроме спинного мозга. Общепризнанно, что смерть мозга не включает нижние части спинного мозга (каудальнее от C2), так как их расположение вне черепа спасает от компрессии во время отека мозга. Гистологические исследования спинного мозга человека в случаях смерти головного мозга показали различающиеся патологические результаты, начиная от гистологически интактных тканей до полного разрушения.
Великобритания и некоторые другие страны поддерживали довольно исключительный критерий для смерти мозга, тот, который исключает причастность билатеральной мозговой коры. Это состояние, известное как «смерть ствола мозга», не требует записи электроэнцефалограммы (ЭЭГ) для его диагностики. В Великобритании никакие подтверждающие тесты (включая ЭЭГ) не требуются. Grigg и колл. сообщили, что у 11 из 56 пациентов с клинически умершим стволом мозга (19,6%) была электроэнцефалографическая активность, и 2 пациента (3,6%) даже продемонстрировали электроэнцефалографическую активность, подобную корковому сну на протяжении 168 ч, хотя ни один из пациентов не выздоровел. Обоснование для исключения коры головного мозга основано на фактах, что ствол мозга, а не кора, играет главную роль в контролировании жизненно важной деятельности организма, такой как дыхание, кровообращение и другие гомеостатические функции, и что ретикулярная формация формирует основу сознания. Однако некоторые исследователи настоятельно рекомендуют подтверждающие тесты (ЭЭГ, транскраниальная допплерография или вызванные слуховые потенциалы ствола мозга) в поддержку диагноза смерти ствола мозга, особенно когда невозможно выполнить все из тестов на функционирование ствола мозга (например, при наличии травмы верхней части спинного мозга или если не может быть исключен остаточный эффект седативных средств).
Сознание и электроэнцефалограмма
Moruzzi и Magoun продемонстрировали существенную роль ретикулярного ядра ствола мозга в активации коркового ЭЭГ. Segundo и колл. показали, что деструкция ретикулярного ядра ствола мозга приводит к потере сознания у лабораторных животных. Эти наблюдения дали рождение концепции восходящей ретикулярной активирующей системы (ВРАС). Хотя центральное понимание этой концепции, что структуры в стволе мозга регулируют состояние сознания, все еще сохраняется, ВРАС больше не расценивается как монолитная единица и при этом не ограничивается классически определенными ретикулярными ядрами ствола мозга. Поддержание бодрствования или контроль цикла сон-бодрствование не зависят исключительно и неизменно от какой-то единственной области мозга. При смерти мозга, как полагают, у пациента отсутствует сознание, интеллектуальная активность и, следовательно, истинная человечность. Это состояние определяется как глубокая кома, и является основой для концепции смерти ствола мозга.
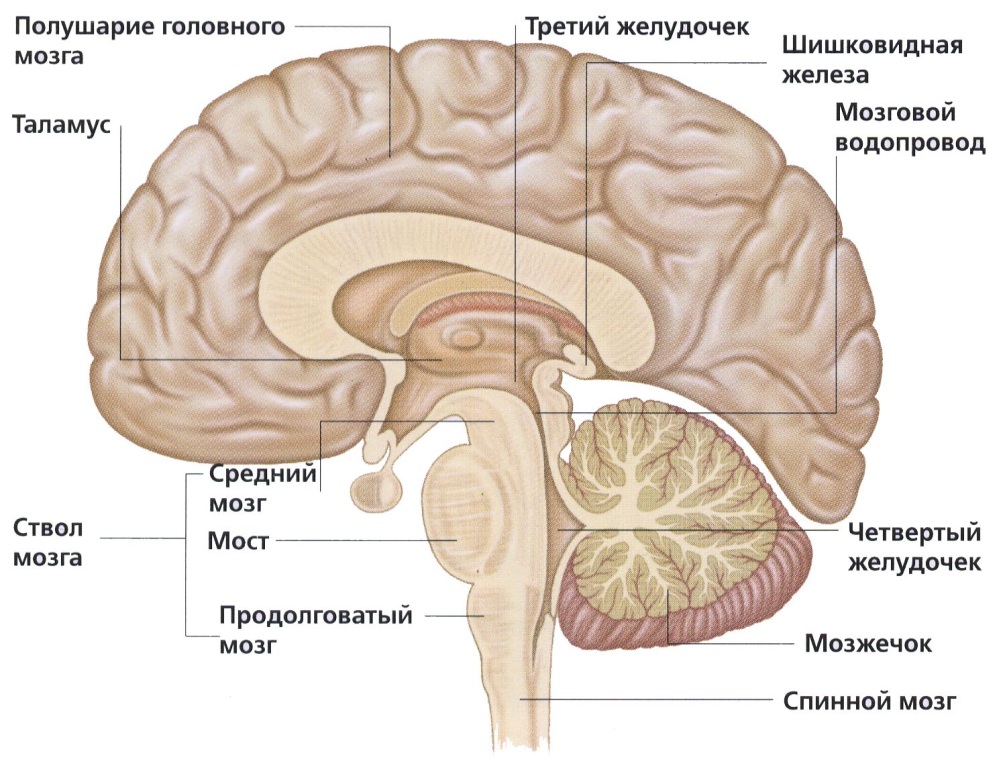
Hockaday и колл. и Schwab и сотр. изучили ЭЭГ 550 коматозных пациентов, проанализировали ЭЭГ после 26 случаев внезапной остановки сердца и 13 случаев остановки дыхания и классифицировали расстройства при ЭЭГ на пять классов согласно конечному результату. Прогноз для пациентов, принадлежащих к I классу, был благоприятным. Определение прогноза для пациентов II и III классов требовало повторной записи ЭЭГ. Когда ЭЭГ показывала положительную динамику на 2 или 3 день записи, прогноз был благоприятен. Когда ЭЭГ имела тенденцию ухудшаться, прогноз был неблагоприятный. В этой системе класс Vb, где вообще нет никакой ЭЭГ-активности, представлял собой ЭЭГ при смерти мозга. Значительные электроэнцефалографические изменения встречаются, когда кровоток падает ниже 18 мл/100 г/мин, и она становится изоэлектрической, когда кровоток находится в диапазоне от 12 до 15 мл/100 г/ мин. Однако Paolin и партнеры сообщили, что у 7 из 15 пациентов с клиническим диагнозом смерти мозга отмечалась постоянная электрическая активность, хотя измерения мозгового кровотока с использованием ксенона-133 и селективная мозговая ангиография показали прекращение внутричерепного кровообращения.
Дыхание
Основной дыхательный центр, состоящий из инспираторных и экспираторных нейронов, расположен в ретикулярном ядре продолговатого мозга. Различные расстройства дыхания (например, гаспинг, патологическое дыхание с удлиненным вдохом и укороченным выдохом, нерегулярное поверхностное дыхание) наблюдаются у лабораторных животных и людей с повреждениями ствола мозга. При смерти мозга спонтанное дыхание не встречается у больных, даже когда PaCO2 достигает 55-60 мм рт. ст. Механическая стимуляция киля трахеи, вызывающая кашлевой рефлекс, может быть полезной в обнаружении остаточного функционирования дыхательных нейронов продолговатого мозга.
Сердечно-сосудистые функции
Центральные нейроны, которые контролируют кровеносную систему, диффузно распределяются в варолиевом мосту и ретикулярном ядре продолговатого мозга. Из этих нейронов вазомоторные и ускоряющие ритм сердца нейроны подвергаются контролю отрицательной обратной связи через каротидный и аортальный нервные синусы, которая передается в ядро солитарного тракта. Активация этих клеток вызывает симпатический нервный ответ, тем самым увеличивая частоту сердечных сокращений и артериальное давление. Артериальная гипертензия затем подавляет эти клетки через механизм обратной связи, и кровообращение возвращается к уровню, предшествующему активации.
Во время процесса смерти мозга после черепно-мозговой травмы или внутримозгового кровоизлияния повышается внутричерепное давление, и компрессия ствола мозга приводит к заметной артериальной гипертензии и брадикардии (т.е. феномену Кушинга). В модели смерти мозга на животных был изучен точный механизм сердечно-сосудистых реакций при прогрессировании ишемии ЦНС в результате расширения супратенториальной массы. Когда весь головной мозг был ишемизирован, наблюдалась вагусная активация с последующим уменьшением частоты сердечных сокращений, среднего артериального давления и сердечного выброса. В то время как ишемия прогрессировала рострально, достигая варолиева моста, к вагусной стимуляции добавлялась симпатическая стимуляция, приводя к брадикардии и артериальной гипертензии (феномен Кушинга). Когда весь ствол мозга становился ишемизирован, ишемизировалось и вагусное кардиомоторное ядро, и происходила без всякого сопротивления стимуляция симпатической системы, приводя к тахикардии, артериальной гипертензии и высоким уровням катехоламинов в крови (т.е. вегетативная буря). Некоторые авторитетные специалисты думают, что на этой стадии вегетативной бури может встречаться повреждение миокарда, которое может способствовать раннему повреждению некоторых трансплантатов и скрывать или осложнять гистологические проявления отторжения у других. Тем не менее, у людей эта стадия тахикардии и артериальной гипертензии может быть короткой, и попытки снизить артериальное давление могут не понадобиться или даже не рекомендованы.
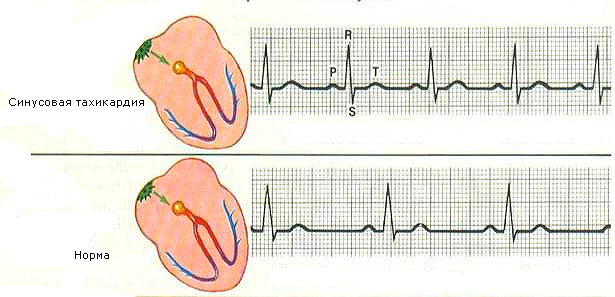
Когда внутричерепное давление повышается, артериальное давление внезапно понижается. Это внезапное понижение – признак тонзиллярного грыжеобразования (т.е. образования грыжи мозжечковых миндалин) через большое затылочное отверстие в шейном отделе спинного мозга, при котором внезапно прерывается выход кардиоускоряющих и вазомоторных нейронов к спинному мозгу. Это один из типичных вариантов начала для смерти мозга. Такие разительные изменения артериального давления не наблюдаются при других типах смерти мозга, которые вызваны гипоксией или которые вовлекают другие сложные факторы. Требуется соответствующая инфузия сбалансированных солевых или коллоидных растворов, а в некоторых случаях переливание крови. Чтобы поддерживать соответствующее артериальное давление, иногда требуются инотропные средства, такие как:
-
Допамин;
-
Адреналин;
-
Норадреналин.
Вазомоторные и ускоряющие ритм сердца нейроны спинного мозга (расположенные в боковом роге) получают автоматизм в течение нескольких дней после разъединения от супраспинальных структур, и артериальное давление возвращается к нормальному без добавления вазопрессоров. Эта ситуация знакома анестезиологам, потому что у пациентов с тетраплегией фоновое артериальное давление обычно нормальное.
После установления смерти мозга развиваются различные типы автономных рефлексов спинного мозга, такие как повышение артериального давления из-за растяжения мочевого пузыря. Артериальная гипертензия и тахикардия, вызванные хирургической стимуляцией, хорошо известны анестезиологам у пациентов с тетраплегией. Подобный феномен наблюдался у пациентов с умершим мозгом. Вазодилататоры или общую анестезию, или и то и другое, следует использовать во время операции по забору органов. Хотя ускоряющие ритм сердца и вазомоторные нейроны расположены в стволе мозга, изменение артериального давления не используется в качестве показателя функции ствола мозга.
Регуляция температуры тела
Rodbard предположил, что нейрональные механизмы, управляющие контролем температурного гомеостаза, развились в гипоталамусе из нейронов, контролирующих кровообращение, в процессе эволюции от рептилий к млекопитающим. Температура тела регулируется, когда изменения температуры крови стимулируют теплочувствительные нейроны в гипоталамусе. Нервные импульсы от холодовых рецепторов кожи также могут активировать теплопродуцирующие нейроны. Самые важные источники тепла – это:
-
скелетные мышцы;
-
головной мозг;
-
печень;
-
сердце.
Наибольший излучатель тепла – кожа, особенно на руках. Локальная электрическая стимуляция теплопродуцирующего центра вызывает дрожь и сужение кровеносных сосудов кожи, активирующих вазомоторные нервы и снижающих кровоток. Нагревание центра теплоотдачи подавляет активность сосудодвигательных нервов и вследствие этого повышает кровоток в коже.
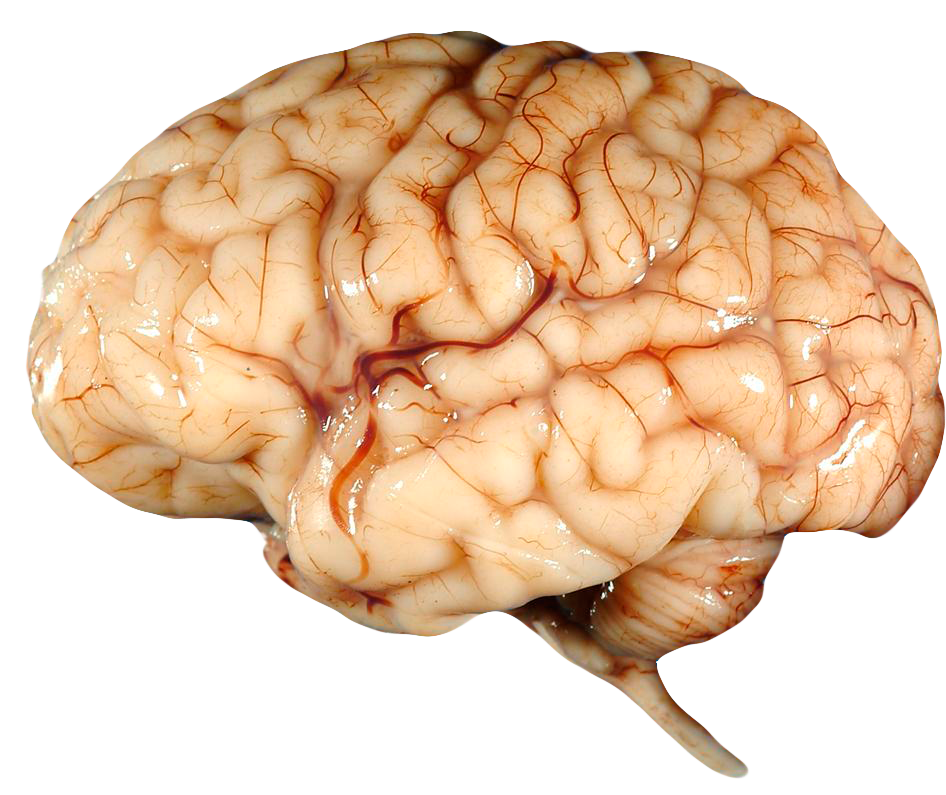
При смерти мозга нейрональная связь между температурорегулирующим центром и периферическими тканями тела теряется, и пациент становится пойкилотермным. Когда критерии Национального института неврологических заболеваний и инсульта (NINDS) были применены для установления смерти мозга, такие пациенты показали только «тенденцию температур быть субнормальными». В противоположность, когда смерть мозга была установлена, используя критерий прекращения всех функций ствола мозга, «пойкилотермия была обнаружена у всех пациентов позже 24 ч после смерти мозга». Даже если встречается инфекция, в случаях смерти мозга лихорадка не должна развиться, потому что теплорегулирующий центр больше не функционирует. После смерти мозга температура тела имеет тенденцию к гипотермии даже при энергичном применении внешнего тепла.
Гипоталамо-гипофизарные эндокринные функции
Никакие критерии, используемые, чтобы установить смерть мозга, не пытаются определить, сохранены ли функции гипоталамуса. Клинические исследования указывают, что функции гипоталамуса и передней доли гипофиза сохранены до определенной степени на определенный период после наступления смерти мозга. Schrader и партнеры сообщили о нормальных уровнях гормонов передней доли гипофиза, таких как тиреотропин, пролактин, соматотропин и лютеинезирующий гормон, период полужизни которых меньше чем 1 ч, так же как и о положительных результатах тестов на гормоны гипоталамуса (гонадотропин-рилизинг гормон и тиреотропин-рилизинг гормон) в течение от 2 до 24 ч после определения смерти мозга. Sugimoto и колл. подтвердили, что концентрации этих гормонов были нормальными более чем 1 неделю.
Напротив, уровень вазопрессина, гормона продуцируемого в гипоталамусе и хранящегося в задней доле гипофиза, резко снижается после смерти мозга. Однако наличие несахарного диабета варьировало. В одном исследовании у многих пациентов после смерти мозга не было несахарного диабета. Другое исследование обнаружило, что у 24 из 31 пациентов (77%) со смертью мозга имелся клинический несахарный диабет. Когда аргинин-вазопрессин добавляется к инфузии в случаях смерти мозга с несахарным диабетом, сердечная деятельность может поддерживаться на протяжении нескольких месяцев. Сообщалось, что плазматические уровни гормонов щитовидной железы, трийодтиронина (Т3) и тироксина (Т4), были значительно снижены после смерти мозга.
Диафрагма турецкого седла защищает гипофиз от компрессии, вызванной отеком мозга. Кровоснабжение гипофиза по большей части осуществляется по верхней, средней и нижней гипофизарным артериям и капсулярным артериям. Портальная венозная система – другой источник кровоснабжения для передней доли. При смерти мозга кровоснабжение через верхнюю гипофизарную артерию и портальную вену может быть легко заблокировано. Однако может спасти кровоснабжение через кавернозную часть внутренней сонной артерии и ее ветви, такие как нижняя гипофизарная артерия и капсулярная артерия. Морфологические исследования смерти мозга указывают, что повреждение передней доли неполное, но серьезное, в то время как задняя доля относительно сохранена. Тем не менее, так как вазопрессин синтезируется в гипоталамусе и переносится в заднюю долю гипофиза через аксоплазматический ток вдоль длинного аксона, истощение этого гормона может быть больше, чем могло бы ожидаться при незначительном морфологическом повреждении, наблюдаемом в задней доле.
В исследованиях по смерти мозга гормоны гипоталамуса, такие как соматотропин-рилизинг гормон, кортикотропин-рилизинг гормон, тиреотропин-рилизинг гормон и гонадотропин-рилизинг гормон, были найдены от следовых до субнормальных уровней. Schrader и колл. сообщили о нормальном ответе соматотропина на гипогликемическую стимуляцию. Arita и колл. также продемонстрировали, что инсулин и аргинин повысили уровни соматотропина у пациентов со смертью мозга. Гипогликемия воздействует на глюкорецепторы в вентромедиальном ядре, стимулируя высвобождение соматотропин-рилизинг гормона и кортикотропин-рилизинг гормона, и стимулирует высвобождение соматотропина или адренокортикотропного гормона, это указывает, что некоторые функции гипоталамуса могут быть сохранены. Однако происхождение гормонов гипоталамуса, высвобождаемых при смерти мозга, не может быть определено. Результаты морфологических исследований гипоталамуса противоречивы. Walker и колл. сообщили, что нейроны с литическими изменениями были смешаны с соответственно нормальными клетками, полученный результат может быть причиной длительной секреции гормонов гипоталамуса. Напротив, Sugimoto и партнеры обнаружили обширный некроз гипоталамуса после 6 дня смерти мозга и постулировали об образовании этих гормонов вне головного мозга, в таких органах, как поджелудочная железа, кишечник или надпочечники. Так как гипоталамус получает кровоснабжение от ветвей верхней гипофизарной и задней соединительной артерий, кровоток в гипоталамусе, по крайней мере, в базальной его части, может быть сохранен при сравнительно умеренных случаях внутричерепной гипертензии.
Для гемодинамической стабилизации доноров органов с умершим мозгом была разработана и рекомендована гормональная терапия. Кардиологическая рабочая группа Конференции в Crystal City, руководимая Объединенной организацией по распределению органов (UNOS), рекомендовала алгоритм ведения донорского сердца, который включал четырехкомпонентную гормональную терапию (Т3, вазопрессин, метилпреднизолон и инсулин) для доноров с фракцией выброса левого желудочка меньше 45% или с нестабильной гемодинамикой, и многофакторные исследования Службы по заготовке и трансплантации органов (OPTN)/UNOS по гормональному лечению доноров со смертью мозга (Т3/Т4, метилпреднизолон и аргинин-вазопрессин) показали значительные увеличения частоты трансплантации органов и первогодичную выживаемость трансплантированных почек и сердец.
Иммунная система
ЦНС оказывает значительное влияние на деятельность иммунной системы. Даже если иммунная система интактна, ее реакция на стимуляцию значительно изменяется после полной и необратимой потери функций ЦНС. У пациентов с умершим мозгом наблюдаются повышенные уровни воспалительных медиаторов, таких как цитокины (IL-1fi, IL-6, TNF-a) и молекул адгезии (Е-селектин, CAM-1, VCAM-1) в крови и в органах, и считается, что эти цитокины ответственны за некоторые эндокринные расстройства и нарушения образования реагентов острой фазы, обнаруживаемые у этих пациентов, и за низкую частоту положительных исходов после пересадки органов.
Рефлексы ствола мозга
Чтобы диагностировать смерть мозга, используются различные рефлексы ствола мозга, такие как:
-
зрачковый;
-
окулоцефалический;
-
окуловестибулярный;
-
кашлевой.
Сохранение кашлевого рефлекса указывает на сохранение дыхательного центра ствола мозга. Нет необходимости присутствия всех рефлексов ствола мозга (кроме тех, которые связаны с дыхательными центрами), чтобы определить организм живым, но они проверяются, чтобы подтвердить сохранение функций ствола мозга.
Критерии и тесты для определения смерти мозга
Определение смерти мозга подтверждает необратимое прекращение всех функций всего мозга, включая ствол мозга. Необратимость означает, что никакое лечение, как можно обоснованно ожидать, не изменит состояния. Нарушение, являющееся причиной, может считаться структурным, и оно не является результатом функциональных и потенциально обратимых причин, таких как интоксикация лекарственными средствами, гипотермия или метаболическое или эндокринное расстройство. Течение времени также представляет собой существенный компонент в определении, что повреждение непоправимо. Хотя тестирование всех функций мозга концептуально невозможно, практически прекращение всех функций головного мозга определяется потерей сознания, потерей реакций ствола мозга, апноэ и подтверждающими тестами, включая отсутствие электроэнцефалографической активности.
Потеря сознания и ареактивность
Пациент должен быть в коме и оцениваться в 3 балла по шкале комы Глазго. Двигательные ответы конечностей или мимических мышц на болезненное супраорбитальное давление должны отсутствовать. Двигательные ответы (т.н. симптом Лазаря) могут встречаться спонтанно при апноэтическом тестировании и рассматриваются как имеющие спинальное происхождение. Этот симптом часто наблюдается во время гипоксических или гипотензивных эпизодов. Наблюдаются другие спонтанные движения, имеющие спинальное происхождение.

3рачки
Форма зрачков может быть круглой, овальной или неправильной. Размер зрачков может варьировать от 4 до 9 мм, но в большинстве случаев он равен 4-6 мм. Симпатические шейные проводящие пути могут быть интактны в состоянии смерти мозга, соединиться с радиально расположенными волокнами мышцы-дилататора и расширить зрачок.
Реакции ствола мозга
Тесты, определяющие реакции ствола мозга, варьируют в различных странах. Критерии Американской академии неврологии включают зрачковый рефлекс, окулоцефалический рефлекс, калорический (окуловестибулярный) тест, роговичный рефлекс, челюстной рефлекс, фарингеальный рефлекс и кашлевой рефлекс.
Апноэтический тест
Тестирование апноэ обязательно для определения смерти мозга и рассматривается как самое важное тестирование, но о нем были споры. Его безопасность является основным вопросом. Во время апноэтического теста могут встречаться значительная гипотензия или тяжелые аритмии сердца, или и то и другое, пневмоторакс, а внутричерепное давление может существенно повыситься. Апноэтический тест должен быть выполнен как последний тест после того, как все другие тесты соответствуют критериям смерти мозга. Goudreau и колл. сообщили, что во время апноэтического теста такие осложнения, как заметное снижение артериального давления или желудочковая аритмия, развились у 27 (39%) из 70 пациентов с предшествующими неблагоприятными факторами, но только у 11 (15%) из 74 пациентов без них. Они указали, что несоответствующая преоксигенация и кислотно-щелочные или электролитные расстройства были главными неблагоприятными предшествующими факторами. Американская академия неврологии рекомендует преоксигенацию 100% кислородом в течение 10 мин перед тестированием апноэ, если PaO2 равно 200 ммрт. ст. или ниже, и доставку 100% O2, 6 л/мин в трахею или введение 100% O2 через катетер, расположенный на уровне киля трахеи во время тестирования апноэ.
Другая проблема – подходящий уровень PaCO2, который должен быть достигнут. После того, как оборудование для анализа газов крови стало широко распространено, была подтверждена важность значения PaCO2, а не времени наблюдения за апноэ. Повышение PaCO2 снижает pH цереброспинальной жидкости, которая стимулирует мозговой дыхательный химический центр. Нормальная дыхательная реакция у собак на повышение PaCO2 возрастает линейно до 80 мм рт. ст., а затем наклон становится менее крутым и достигает максимума приблизительно на 150 мм рт. ст. Повреждение в мозговом дыхательном центре может оказать влияние на уровень PaCO2 при развитии спонтанного дыхания. Уровень PaCO2, при котором восстанавливается спонтанное дыхание, также изменяется значением PaO.
Wijdicks сообщил, что хотя большинство всех мировых рекомендаций по смерти мозга требовали апноэтического теста (71 из 80 стран), только 41 из 71 рекомендаций определили точное целевое значение PaCO2, и он пришел к заключению, что, если была принята предпосылка документации апноэ, используя гиперкапнию для максимальной стимуляции дыхательных центров, можно сделать вывод, что в половине стран апноэтический тест не проводился соответствующим образом. Точный уровень PaCO2, который должен быть достигнут, до сих пор неизвестен, но критерии Американской академии неврологии определяют различные предпосылки и процедуру тестирования апноэ и принимают уровень PaCO2 выше или равным 60 мм рт. ст., а критерии Великобритании требуют значение PaCO2 равное 6,65 кПа (50 мм рт. ст.).
Предпосылки для диагностирования смерти мозга
Несколько расстройств имитируют смерть мозга и могут привести к ошибочному диагнозу. Отсутствие этих состояний должно быть подтверждено, и следующие факторы рассматриваются прежде, чем применяются критерии для смерти мозга.
Глубокая кома
Пациент должен находиться в глубокой коме, и причина комы должна быть установлена. Органическое повреждение головного мозга должно быть подтверждено как необходимое условие для диагностирования смерти мозга. Лекарственная интоксикация, тяжелые электролитные, кислотно-щелочные или эндокринные расстройства, гипотермия и другие, в целом излечимые нарушения должны быть исключены.
Температура тела
После прекращения функций ствола мозга и гипоталамуса и после полного разъединения спинного мозга от супраспинальных мозговых структур пациент становится пойкилотермным, и температура тела имеет тенденцию к гипотермии, даже при энергичном согревании. Поскольку гипотермия подавляет функцию ЦНС и приводит к ошибочному диагнозу смерти мозга, температура тела должна быть в пределах нормальных величин (т.е. гипотермия должна быть корректирована), до того как будут применены критерии для смерти мозга.
Отсутствие сердечно-сосудистого шока
Когда внутричерепное давление повышается, развивается системная артериальная гипертензия как результат феномена Кушинга. За этим следует внезапное снижение артериального давления из-за резкого прерывания вазомоторных эфферентных путей от ствола мозга и гипоталамуса к спинному мозгу. Гипотензия обычно разрешается спонтанно в течение нескольких дней с помощью восстановления спонтанной активности вазомоторных нейронов спинного мозга. Гипотензия может привести к нарушению церебральной перфузии, приводящей к потере электроэнцефалографической активности, тем самым вызывая ошибочный диагноз. Таким образом, следует рассматривать введение вазопрессоров для достижения относительной нормотензии; вазопрессорная терапия иногда восстанавливает электроэнцефалографическую активность при определении смерти мозга.
Клинический диагноз смерти мозга
Рекомендации и клинический диагноз для определения смерти мозга отличаются в разных странах и среди учреждений Соединенных Штатов и Канады. Однако принцип кажется схожим, и клиническая диагностика смерти мозга должна выполняться в 3 шага:
-
установление причины болезни;
-
исключение определенных потенциально обратимых синдромов, которые могут продуцировать симптомы, схожие со смертью мозга;
-
демонстрирование клинических признаков смерти мозга: кома, арефлексия ствола мозга и апноэ.
Подтверждающие тесты в определении смерти мозга не всегда обязательны, но они желательны, особенно когда клиническая картина запутана. В общем, чтобы установить диагноз смерти мозга, требуются 2 осмотра, разделенных между собой по крайней мере 6 ч. Большая часть кодексов устанавливает, что клинический диагноз должен быть подтвержден двумя или тремя врачами, которые не связаны с отделением трансплантации, и по крайней мере один из врачей должен быть специалистом в неврологии, нейрохирургии или анестезиологии.
Церебральная смерть: персистирующее вегетативное состояние
Церебральная смерть, так называемое персистирующее вегетативное состояние, относится к прекращению функций коры головного мозга. Сохранены функции ствола мозга, управляющие дыхательными центрами, автономной нервной системой, эндокринной системой и иммунной системой, которые жизненно важны для того, чтобы поддерживать жизнь. Хотя корковая ЭЭГ находится на изолинии, она обычно «загрязняется» электромиографической активностью лба - признак сохранения функции лицевого нерва в стволе мозга. Персистирующее вегетативное состояние представляет необратимую потерю сознания, но не необратимое лишение жизни или механизма жизни; пациенты в этом состоянии могут оставаться в живых в течение многих месяцев или лет. Термин церебральная смерть иногда используется по ошибке для обозначения смерти мозга, которая включает ствол мозга.
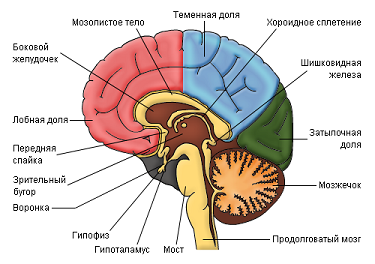
Церебральная смерть не была традиционно принята как эквивалент смерти. Однако некоторые выступают в защиту того, что церебральная смерть должна быть принята как смерть личности, потому что важнейшими элементами жизни являются организованное познание и «индивидуальность» как уникальные особенности человеческой жизни, которые происходят из головного мозга. Проблемы с этим понятием состоят в том, что постоянство мозговой дисфункции при большинстве клинических обстоятельств не может быть легко предсказано и угрожает развитием тяжелых сенильных расстройств и проявлениями умственной отсталости, при которых могут серьезно повреждаться высшие нервные функции. Из 40 пациентов, отнесенных к персистирующему вегетативному состоянию, у 17 (43%), как полагали, был поставлен неверный диагноз; они знали об окружающей обстановке и были способны общаться.
Нехватка младенческих органов, доступных для трансплантации, во всем мире вызвала растущее признание потенциального использования как доноров анэнцефалов, тех, кто рождается без переднего мозга и большого мозга, но с рудиментарным функциональным стволом мозга. Естественный ход событий состоит в том, что одна половина плодов умирает внутриутробно, а приблизительно 95% живорожденных анэнцефалов обычно умирают в течение 7 дней. В 1995 г. Совет по этике и судебным делам Американской медицинской ассоциации поддержал использование живых младенцев-анэнцефалов, как доноров органов, хотя такая позиция противоречит юридическому и этическому применению «правила мертвого донора». Он утверждал, что анэнцефалы-новорожденные определенно отличаются от людей, которые находятся в персистирующем вегетативном состоянии, младенцев с тяжелым неврологическим повреждением и пожилых людей с тяжелой деменцией, потому что анэнцефалы никогда не были в сознании и не имеют никакой возможности когда-то быть в сознании. Однако в 1996 г. приостановил свое мнение из-за беспокойства по поводу некоторых диагнозов анэнцефалии и понимания сознания у этих новорожденных. В 1961 г. была впервые выполнена пересадка почки от анэнцефала-новорожденного как донора, за которой последовали некоторые попытки пересадки сердца. Однако страны Запада, за исключением Германии, полагают, что младенец-анэнцефал юридически жив, пока функционирует ствол мозга.
Структуры ЦНС, важные для определения смерти мозга, не включают спинной мозг. Гистологические исследования показали, что спинной мозг является наиболее хорошо сохранившейся частью ЦНС в случаях смерти мозга, и результаты варьировали от абсолютно нормальной гистологии до отека, потери нейронов, нейролиза и редко инфаркта.
У пациентов с умершим мозгом обнаруживаются спонтанные и рефлекторные движения. Спонтанные движения тела могут наблюдаться во время проведения апноэтического теста, когда тело готовится к транспортировке, во время разреза кожи для извлечения органов или синхронно с дыханием, осуществляемым механической вентиляцией. В 5 из 60 случаев смерти мозга после окончательного выключения аппарата ИВЛ или на протяжении апноэтических тестов Ropper сообщил о странных, на вид целенаправленных движениях верхних конечностей, названных симптомом Лазаря, при которых руки, лежащие по бокам больных, быстро сгибались к грудной клетке, плечи сводились, и у некоторых пациентов кисти рук перекрещивались или приводились чуть ниже подбородка. Saposnik и колл. сообщили, что 15 (39%) из 38 пациентов, которые соответствовали критериям смерти мозга, осуществляли спонтанные или рефлекторные движения; наиболее распространенным движением были подергивания пальцев, а также отмечались волнообразное сгибание ног, тройная сгибательная реакция, симптом Лазаря, рефлекс пронации-разгибания и лицевая миокимия. Медицинский персонал должен помнить, что пациент может двигаться в ответ на стимуляцию и что требуется полная миоплегия для хирургических процедур при наличии смерти мозга.
Обсуждения относительно детей
Детский мозг – это развивающийся орган, и считается, что анатомическое развитие нервной системы продолжается до двухлетнего возраста или после первой декады жизни. На протяжении этого времени отмечаются также изменяющиеся паттерны уязвимости на повреждение и различные реакции на самоповреждение. Кроме того, наличие открытых родничков и открытых швов у детей младшего возраста делает череп растяжимой полостью. Внутричерепное давление может не превысить среднее артериальное давление, и мозговой кровоток продолжается. Общепринято, что детский мозг более устойчив к повреждениям, приводящим к смерти, хотя эта проблема спорна и испытывает недостаток в убедительной клинической документации.
Необходимость упрощения принятия решения о конце жизни и заборе органов у младенцев и детей увеличилась. В 1987 г. целевая группа для определения смерти мозга у детей поддержала «Закон об определении смерти» и предложила «Рекомендации для определения смерти мозга у детей». Отличиями от критериев для взрослых являются три отдельных, более продолжительных периода наблюдения, зависящих от детского возраста, и необходимость в двух подтверждающих ЭЭГ или одном ЭЭГ с подтверждающей радионуклидной ангиографией. Общесогласовано, что кроме очень недоношенных, преждевременно родившихся новорожденных, эти критерии смерти мозга могут применяться к доношенным новорожденным, младенцам старше 7 дней, детям и взрослым, если период наблюдения продлен для маленьких детей. Однако было несколько сообщений, приводящих доводы против этой идеи. Например, некоторые исследователи рекомендовали для апноэтического теста у младенцев и детей необходимость достижения РаСО2 выше 12,0 кПа, потому что порог углекислого газа, необходимый для определения апноэ, у детей иногда выше, чем у взрослых.
Ashwal и Sema-Fonseca подчеркнули, что смерть мозга могла быть диагностирована у новорожденных (даже младше 7 дней), если период наблюдения для подтверждения диагноза продлевался до 48 ч; но если ЭЭГ была изоэлектрической или исследование церебрального кровотока показывало его отсутствие, то период наблюдения мог быть сокращен до 24 ч. Они также предположили, что тот же самый период времени будет применим к недоношенным младенцам. Вместе с тем Специальная целевая группа исключила младенцев младше 7 дней из своих рекомендаций. Имеются некоторые опасения по поводу диагноза смерти мозга у новорожденных.
Сообщалось, что недоношенный младенец, у которого случилось внутрижелудочковое кровоизлияние на 2 день жизни, демонстрировал отсутствие рефлексов ствола мозга, апноэ и атоничность, но никогда клинически не был с умершим головным мозгом, и что 15 из 20 новорожденных, у которых было изоэлектрическое ЭЭГ, сохраняли частичную клиническую функцию головного мозга. С тех пор, как были выпущены эти рекомендации, сообщалось о широких вариациях в практической деятельности или о нарушениях этих рекомендаций. Mejia и колл. исследовали вариабельность в практике определения смерти мозга и изъятия органов в педиатрических отделениях интенсивной терапии. Хотя тестирование апноэ считали самым важным критерием для смерти мозга даже у детей, оно не выполнялось у 23 (25%) из 93 пациентов с умершим мозгом, и методы тестирования апноэ были не совместимы с «Рекомендациями по определению смерти мозга у детей» для 20 пациентов (22%). У четырех из 30 пациентов младше 1 года не было подтверждающего теста. Они пришли к выводу, что разнообразие в практике определения смерти мозга может отражать различия в документации, отсутствие знания рекомендаций или несогласие с руководящими принципами.
Теория о головном мозге, как центральном интеграторе
Понятие, что смерть мозга эквивалентна смерти человека, главным образом основано на теории «мозг как центральный интегратор организма». При смерти мозга тело больше не интегрированный организм, а просто и быстро распадающийся набор органов, которые навсегда потеряли способность работы как скоординированное целое. Раньше считали, что у больных со смертью мозга неизбежно возникает остановка сердца в течение короткого периода времени (обычно в течение 1 или 2 недель), независимо от интенсивности жизнеобеспечения.
Однако было признано, что не все пациенты с умершим мозгом неизбежно ухудшаются до сердечно-сосудистого шока за короткое время, и некоторые из них показывают достаточный уровень целостности организма на протяжении недель или месяцев (больше 14 лет в одном случае), если им предоставляется адекватное жизнеобеспечение. Кроме того, пациенты с умершим мозгом могут усваивать питательные вещества, удалять продукты метаболизма, бороться с инфекцией, излечивать раны, вынашивать беременность и т.д. без контроля мозга. Zapperetti и колл. утверждают, что теория «центрального интегратора» основывается больше на том, что, мы думаем, согласно определению, должно произойти с пациентами с умершим мозгом, чем на том, что может наблюдаться клинически.
Вариабельность в политике и практике при определении смерти мозга
Хотя понятие смерти мозга, как определяющее смерть человека широко принято, существует значительная вариабельность в политике и практике при определении смерти мозга среди стран и даже в пределах страны, т.е. среди штатов и больниц. Wijdicks сообщил, что из 80 исследованных государств, юридические стандарты по трансплантации органов присутствовали в 55 странах (69%), а практические рекомендации по смерти мозга для взрослых были в 70 странах (88%). Все рекомендации определенно указывали исключение вмешивающихся факторов, необратимую кому, отсутствие двигательной реакции и отсутствие рефлексов ствола мозга, но были значительные различия в методе тестирования апноэ, в сроке наблюдения, в количестве и требуемой компетенции об следующих врачей и в необходимости подтверждающих тестов. Кроме того, поскольку в Соединенных Штатах и Канаде деятельность по смерти мозга в основном определена отдельными больницами, были найдены значительные различия среди политики больниц и рекомендаций по смерти мозга. Wijdicks и другие исследователи подчеркивали необходимость стандартизировать практику неврологического определения смерти мозга. Также сообщалось о широком разнообразии практики в педиатрии и в определении критериев смерти ствола мозга в Великобритании, несмотря на существование четких рекомендаций для выполнения теста.
Подтверждающие тесты для смерти мозга
Тесты, которые подтверждают потерю биоэлектрической активности мозга или прекращение церебрального кровообращения, не всегда обязательны для взрослых, но строго рекомендуются для детей, особенно младше 1 года. В некоторых странах Европы, Центральной Америки, Южной Америки и Азии подтверждающие тесты требуются по закону. В Соединенных Штатах выбор тестов остается на усмотрение врача. Young и партнеры предложили критерии для идеальных подтверждающих вспомогательных тестов:
-
Не должно быть никаких «ложноположительных» случаев; т.е. когда тест подтверждает «смерть мозга», не должно быть выздоровевших или с потенциалом на выздоровление.
-
Тест должен быть независимо достаточным, чтобы установить имеется или отсутствует смерть мозга.
-
Тест должен быть невосприимчив к «факторам погрешности», таким как эффекты лекарственных препаратов или метаболические расстройства.
-
Тест должен быть стандартизирован в технологии, методе и классификации результатов.
-
Тест должен быть доступным, безопасным и легко применимым. Тестирование не должно быть ограничено только несколькими исследовательскими центрами; в идеале он может быть применен в любом отделении интенсивной терапии, и метод должен быть надежным и осваиваемым без труда.
-
Во всех случаях подтверждающие тесты должны использоваться вместе с соответствующей клинической оценкой.
Электроэнцефалографическая запись
ЭЭГ является наиболее широко доступным нейрофизиологическим тестом и используется во многих странах и учреждениях в качестве подтверждающего теста смерти мозга (смерть «всего головного мозга»). Потеря биоэлектрической активности головного мозга, как показано на ЭЭГ (т.е. изоэлектрическая ЭЭГ), является надежным подтверждающим тестом при смерти мозга. Однако должны быть рассмотрены некоторые проблемы. Изоэлектрическая ЭЭГ может быть обнаружена после лекарственной интоксикации (ложноположительная), например, при отравлении барбитуратами, и, наоборот, остаточная электрическая активность может сохраниться после смерти ствола мозга или даже у некоторых пациентов, которые соответствовали клиническим критериям смерти мозга (ложноотрицательная).
Отсутствие ЭЭГ активности, или ЭЭГ тишина, определяется как отсутствие электроэнцефалографической активности выше 2 мкВ/мм, когда запись производится накожными электродами, расположенными на расстоянии 10 см или более и с межэлектродными сопротивлениями меньше 10000 Ом, но больше 100 Ом.
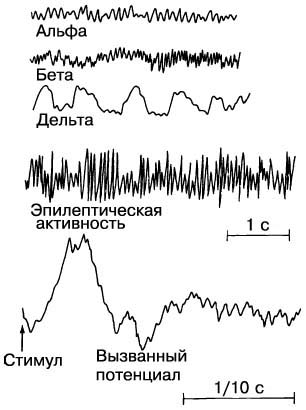
Вызванные потенциалы
Коротколатентные слуховые вызванные потенциалы ствола мозга (КСВП) и соматосенсорные вызванные потенциалы срединного нерва (ССВП) используются для диагноза смерти мозга. В отличие от сигналов ЭЭГ на ранние компоненты КСВП и ССВП минимально воздействуют седативные препараты и анестетики. Однако лекарства и метаболические расстройства оказывают влияние на средние и поздние компоненты КСВП и ССВП. КСВП – сигналы, генерируемые в слуховых нервах и стволе мозга после акустического стимула. КСВП состоят из 5 идентифицируемых волн, генерируемых из определенных структур ствола мозга вдоль слуховых проводящих путей:
-
волна I представляет потенциал действия восьмого нерва;
-
волна II – восьмой нерв и улитковые ядра;
-
волна III – нижний мост, включающий верхнюю оливу;
-
волны IV и V – верхний мост и средний мозг, вверх по нижнее двухолмие.
Расстройства ствола мозга могут быть обнаружены при помощи КСВП. Отсутствие волн с III по V или со II по V, или невоспроизводимые КСВП с обеих сторон расцениваются как смерть мозга, хотя волна I иногда остается. Существовавшая ранее глухота или тяжелое повреждение периферической слуховой системы могут привести к ложноположительному результату.
После электростимуляции периферического нерва волны ССВП генерируются из нервных структур вдоль афферентных соматосенсорных проводящих путей: плечевого сплетения, верхнего шейного отдела спинного мозга, дорсальныого ядра столба, вентрозадних ядер таламуса и сенсорной коры. «Практические Параметры для Определения Смерти Мозга у Взрослых», опубликованные в «Neurology», рекомендовали билатеральное отсутствие реакций N20-P22 при стимуляции срединного нерва как подтверждающий лабораторный тест. Facco и колл. сообщили, что отсутствие компонентов далее N13, который представляет постсинаптическую активность в центральном сером веществе шейного отдела спинного мозга, или N13/P13 диссоциация, были надежными для подтверждения смерти мозга. Эти исследователи также рекомендовали совместное использование КСВП и ССВП для определения смерти мозга. Sonoo рассматривал потерю потенциала N18, который предположительно генерируется в клиновидном ядре продолговатого мозга, как надежный признак для диагноза смерти мозга.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания








Комментарии