Первичный и вторичный гипогонадизм у женщин: сипмтомы, причины, фото
Женщины с кариотипами XXX, ХХХХ и ХХХХХ
-
Кариотип XXX.
Трисомия (аутосом или половых хромосом) — наиболее распространенная хромосомная аномалия у человека. Ее обнаруживают у 4 % плодов. Среди Х-хромосомных аномалий у женщин чаще всего встречается кариотип 47,XXX (примерно 1:1000 новорожденных девочек). В 68% случаев это состояние обусловлено нерасхождением материнских хромосом в мейозе (тогда как большинство случаев 45,X и 50 % 47.XXY — результат нарушения отцовских половых хромосом). Фенотип нормальный женский. В раннем детском возрасте какие-либо клинические проявления отсутствуют.
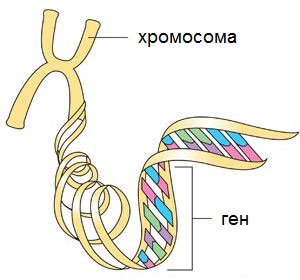
Половое развитие протекает нормально. Большинство беременностей заканчивается рождением здорового ребенка. К 2-летнему возрасту многие дети с этой аномалией еще не говорят. Позднее отмечается плохая координация движений и плохая успеваемость в школе. Характерно детское поведение. Девочки обычно высокие и худощавые, склонны к неправильным поступкам, и их приходится помещать в специальные школьные классы. При МРТ высокого разрешения у 10 девочек с кариотипом 47,XXX обнаружен меньший объем миндалевидного тела, чем в контроле, хотя и больший, чем при кариотипе 47.XXY. Проявления данного синдрома крайне непостоянны, и в отдельных случаях сохраняется прекрасная координация движений, социальная адаптация и высокая успеваемость.
-
Кариотипы ХХХХ и ХХХХХ.
У подавляющего большинства девочек с этими редкими кариотипами наблюдается умственная отсталость. Обычно имеются складки эпиканта, гипертелоризм, клинодактилия, поперечные ладонные складки, сращение лучевых и локтевых костей и врожденные пороки сердца. Половое развитие зачастую неполное и может вообще не наступить. Тем не менее, у 3 женщин с тетрасомией X имелись дети, но при синдроме 49,ХХХХХ беременности не наблюдались. Большинство женщин с кариотипом 48,ХХХХ отличаются довольно высоким ростом (средний рост 169 см), тогда как для кариотипа 49,ХХХХХ характерна низкорослость.
Синдром Нунан
У девочек с синдромом Нунан, несмотря на нормальный набор хромосом (46,XX), имеются некоторые признаки синдрома Тернера. Фенотип женщин отличается от тернеровского. Часто отмечается умственная отсталость, среди пороков сердца преобладают стеноз клапанов легочной артерии и дефект межпредсердной перегородки, а не коарктация аорты. Половое развитие протекает нормально, но запаздывает в среднем на 2 года. Наблюдается преждевременная недостаточность яичников.

Прочая патология яичников
У некоторых молодых женщин без хромосомных аномалий обнаруживаются тяжевидные гонады, в которых отсутствуют зародышевые клетки. Уровень гонадотропинов повышен. Причиной недостаточности яичников все чаще становится применение противораковых цитотоксических средств, особенно алкилирующих веществ (циклофосфамид, бисульфан, прокарбазин, этопозид), а также лучевая терапия злокачественных новообразований. Как показывает лечение болезни Ходжкина, при сочетании химиотерапии с облучением таза яичники повреждаются в большей степени, чем при использовании какого-либо одного из этих методов лечения. У подростков вероятность сохранения или восстановления функции яичников после облучения или химиотерапии выше, чем у женщин зрелого возраста, и они в дальнейшем могут забеременеть. Тем не менее, современные схемы лечения рака приводят к повреждению яичников у большинства девочек. LD50 для ооцитов человека составляет примерно 4 Гр. Облучение уже в дозе 6 Гр вызывает первичную аменорею. Транспозиция яичников перед облучением брюшной полости и таза помогает сохранить их функцию, снижая локальное лучевое воздействие до 4-7 Гр.
У 60% девочек с аутоиммунным полигландулярным синдромом типа 1 (первичная надпочечниковая недостаточность, гипопаратиреоз, кандидоз кожи и слизистых оболочек) после 13 лет развивается аутоиммунная недостаточность яичников. Аутоиммунный полигландулярный синдром типа 1 особенно распространен в Финляндии, где благодаря эффекту генетического основателя его частота составляет 1:25 000. Ген этого синдрома расположен на хромосоме 21 и ассоциирован с HLA-DR5. В случаях недостаточности яичников при этом синдроме обнаружена ассоциация с HLA-A3. У девочек может отсутствовать половое развитие, а у молодых женщин может развиваться вторичная аменорея.
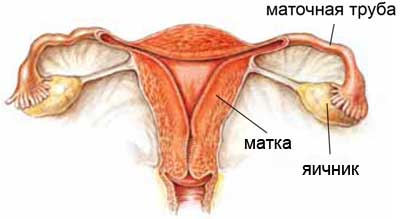
Яичники инфильтрированы лимфоцитами, но иногда они имеют вид простых тяжей. У большинства больных в крови присутствуют антитела к стероид-продуцирующим клеткам и к 21-гидроксилазе.
Аутоиммунная недостаточность яичников у молодых женщин может быть изолированной или сочетаться с другими аутоиммунными синдромами. В таких случаях развивается вторичная аменорея (преждевременная менопауза). Она встречается у 0,2-0,9% женщин моложе 40 лет. Преждевременная менопауза — гетерогенное состояние, имеющее множество причин (хромосомные аномалии, генетические дефекты, недостаточность ферментов, инфекционные заболевания или ятрогенные воздействия). При ее сочетании с аутоиммунным поражением надпочечников в крови больных всегда присутствуют антитела к стероид-продуцирующим клеткам, направленные против 20,22-десмолазы, 17а-гидроксилазы или 21-гидроксилазы. При сочетании преждевременной менопаузы с аутоиммунными заболеваниями других эндокринных и неэндокринных органов, но не с первичной надпочечниковой недостаточностью антитела к стероид-продуцирующим клеткам выявляются редко. Второе аутоиммунное заболевание (часто не проявляющееся клинически) находят у 10-39 % женщин с преждевременной менопаузой. Ранняя недостаточность яичников была обнаружена у 17-летней девушки с кариотипом 47,XXX и идиопатической тромбоцитопенической пурпурой.
Галактоземия, особенно в ее классической форме, обычно приводит к повреждению яичников, которое начинается еще во внутриутробном периоде. Уровень ФСГ и ЛГ в раннем постнатальном периоде значительно повышен. Причиной повреждения яичников является, вероятно, дефицит уридиндифосфатгалактозы. Дисгенезия яичников наблюдается при синдроме Дрэша, в основе которого лежит мутация гена WT1.
Причина гипоплазии яичников (с повышением уровней гонадотропных гормонов) при атаксии-телеангиоэктазии остается неизвестной. У отдельных девочек выявлены гонадобластомы и дисгерминомы.
Первичный гипогонадизм встречается при резистентности яичников к экзогенным и эндогенным гонадотропным гормонам (синдром Сэвиджа). Этот синдром наблюдается и у женщин с преждевременной менопаузой. Его причиной могут быть антитела к рецептору ФСГ или дефекты самого рецептора. Известна атосомно-рецессивно наследуемая мутация гена рецептора ФСГ. У немногих женщин с кариотипом 46,XX и первичной аменореей на фоне повышенного уровня гонадотропных гормонов обнаружены инактивирующие мутации гена рецептора ЛГ. Это свидетельствует о необходимости ЛГ для нормального развития фолликулов и овуляции.
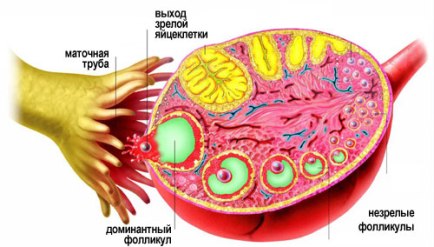
Гипогонадотропный (вторичный) гипогонадизм у женщин
К гипофункции яичников приводит недостаточная секреция гонадотропинов. Дефект в этих случаях локализуется на уровне гипофиза или, чаще, гипоталамуса.
Этиология
-
Гипопитуитаризм.
Врожденные или приобретенные повреждения области гипофиза почти всегда приводят к нарушению секреции гонадотропинов и других гипофизарных гормонов. У детей с множественной недостаточностью гормонов гипофиза, включая гонадотропины, обнаружены дефекты факторов транскрипции, в частности и PROP-1. При идиопатическом гипопитуитаризме нарушение обычно локализовано в гипоталамусе. Введение ГнРГ в таких случаях приводит к восстановлению гонадотропной функции гипофиза и повышению уровня ФСГ и ЛГ в плазме.
-
Изолированный дефицит гонадотропных гормонов.
Заболевания этой гетерогенной группы дифференцируют с помощью пробы с ГнРГ. У большинства детей гипофиз остается нормальным, а патология кроется в гипоталамусе.
Описано несколько спорадических случаев аносмии с вторичным гипогонадизмом. Такие нарушения характерны также для синдрома Каллмана, в ядерных семьях гипогонадизм чаще выявляется у мужчин. У больных обнаруживаются мутации генов, кодирующих Р-субъединицы ФСГ и ЛГ.
Дефицит гонадотропинов находят при некоторых аутосомно-рецессивных заболеваниях, таких как синдром Лоренса-Муна-Бидля, множественные лентиго и синдром Карпентера. Вторичный гипогонадизм наблюдался у девочек с синдромом Прадера-Вилли, а также при талассемии (отложение железа в гипофизе из-за частых переливаний крови). Дефицит гонадотропных гормонов нередко развивается при нервной анорексии.
Диагностика
При множественном дефиците гипофизарных гормонов диагноз очевиден но, как и у мальчиков, отличить изолированный вторичный гипогонадизм от физиологической задержки полового развития крайне трудно. Частые определения уровня ФСГ и ЛГ, особенно в ночное время, помогают обнаружить его возрастание, указывающее на приближение периода полового развития. Установлению диагноза способствуют пробы с ГнРГ или его аналогами.
-
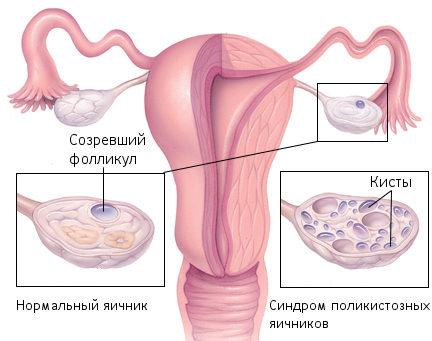
Поликистоз яичников (синдром Штейна-Аевентадя).
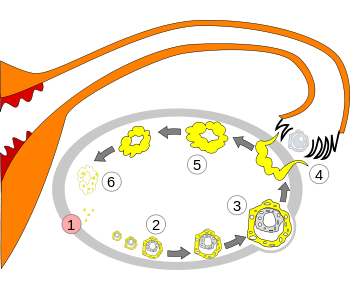
Классический синдром поликистозных яичников (СПКЯ) характеризуется ожирением, гирсутизмом и вторичной аменореей у женщин с увеличенными с обеих сторон яичниками, содержащими множество кист. Однако в каждом отдельном случае могут присутствовать не все эти признаки. Клинические признаки обычно появляются в пубертатном периоде или вскоре после него. Больные чаще всего жалуются на нерегулярность менструаций и гирсутизм. Этот синдром является наиболее частой причиной ановуляторного бесплодия у женщин детородного возраста. Его нередко называют функциональной гиперандрогенией яичникового происхождения и (особенно у женщин зрелого возраста) хронической гиперандрогенной ановуляцией. Развитие СПКЯ, по-видимому, связано с преждевременным адренархе. В увеличении яичников позволяют убедиться бимануальная пальпация (через прямую кишку и живот) или УЗИ.
Несмотря на тщательные исследования, причина поликистоза в большинстве случаев остается неясной. Ею может быть недостаточность 21-гидроксилазы, 3-гидроксистероиддегидрогеназы или яичниковой 17-кеторедутазы, которая превращает андростендион в тестостерон и эстроген в эсгладиол. Отщепление боковой цепи холестерина (под действием 20,22-десмолазы, кодируемой геном CYP11A) происходит в митохондриях, а поступление холестерина в них требует присутствия StAR. Функция гена StAR подавляется фактором транскрипции DAX-1, в регуляции гена участвует и SF-1. У женщин с гиперандрогенией и гирсутизмом независимо от нарушений менструального цикла найдены дефекты генов CYP11A или DAX-1. У большинства женщин с поликистозом яичников дексаметазин не снижает повышенного уровня свободного тестостерона и андростендиона в плазме, что позволяет исключить надпочечниковую причину данного состояния. В ряде случаев отмечается высокое содержание только свободного, но не общего тестостерона. Уровень глобулина, связывающего половые гормоны, заметно снижен.
Примерно у 75% больных повышено отношение ЛГ/ ФСГ в плазме, увеличена амплитуда и частота выбросов ЛГ и усилена его реакция на ГнРГ. Исходное содержание ингибина В в плазме также повышено, причем отсутствует нормальный импульсный характер его секреции. У девочек до наступления менархе уровень ЛГ возрастает по утрам, а не ночью, как в норме. Считается, что именно нарушение секреции ЛГ приводит к гиперплазии внешней оболочки фолликулов, остановке их развития и снижению продукции эстрадиола. Дефект в развитии фолликулов, один из кардинальных механизмов развития поликистоза яичников, может быть связан с нарушением действия фактора роста и дифференцировки ооцитов, но не фактора морфогенеза костей. Оба эти фактора стимулируют рост ооцитов. В результате развивается гиперандрогения и аменорея или нарушается менструальный цикл. У детей с врожденными синдромами вирилизации гипоталамо-гипофизарная система, по-видимому, запрограммирована на гиперсекрецию ЛГ во время полового развития, что приводит к гиперандрогении даже в отсутствие надпочечниковых андрогенов. При гиперандрогении часто находят полиморфизм промотора гена ИЛ-6.
Существует связь между гиперандрогенией и инсулинорезистентностью. При СПКЯ, особенно у больных с ожирением, наблюдаются гиперинсулинемия, инсулинорезистентность и acanthosis nigricans.
Поликистоз яичников — одно из наиболее частых состояний, сопровождающихся нарушением толерантности к глюкозе и сахарным диабетом типа 2. В одном из исследований, нарушение толерантности к глюкозе было обнаружено у 7 из 27 девушек с этим синдромом. Инсулинорезистентность связывают с повышенным фосфорилированием серина в составе инсулинового рецептора. Этот же процесс (фосфорилирование серина) играет важную роль в регуляции активности 17а-гидроксилазы — основного фермента биосинтеза андрогенов. Некоторые авторы считают данный дефект общей и единственной причиной инсулинорезистентности и гиперандрогении при поликистозе яичников. Предрасположенность к СД 2 может зависеть от полиморфизма гена, кодирующего цистеиновую протеазу (кальпаин-10). Среди белого и афроамериканского женского населения США повышенный уровень инсулина и двукратное возрастание риска СПКЯ ассоциируются с 112/121-гаплотипом.
СПКЯ диагностируют по содержанию в сыворотке ЛГ, ФСГ, пролактина, свободного тестостерона и глобулина, связывающего половые гормоны, а также ДЭА-сульфата. Уровень ДЭА-сульфата повышен и у братьев женщин с поликистозом, а у их сестер инсулинорезистентность (повышенный уровень инсулина и сниженное отношение глюкоза/инсулин в плазме натощак) ассоциируется с гиперандрогенией, но не с нарушением менструального цикла. Однако у самих больных инсулинорезистентность выражена в разной степени. Чтобы различить гиперандрогению надпочечникового и яичникового происхождения, применяется комплекс стимулирующих и ингибирующих фармакологических проб. Определение уровня надпочечниковых стероидов до и после стимуляции АКТГ способствует выявлению даже легких нарушений стероидогенеза в надпочечниках.
При обнаружении дефекта у братьев больной или при повышенном отношении эстрон/эстрадиол и андростендион/тестостерон в сыворотке крови предполагают недостаточность 17-кеторедуктазы. СПКЯ и повышенный уровень тестостерона нередко выявляется у молодых больных эпилепсией, получающих натрия вальпроат, однако содержание ЛГ у них остается нормальным.
Оптимальных способов лечения пока не существует. Основной способ — подавление функции яичников с помощью оральных контрацептивов, содержащих прогестагены, лишенные андрогенных свойств, например, дезогестрел (дезоген). Единственное средство, применяемое в США для уменьшения гирсутизма, помимо оральных контрацептивов — это спиронолактон. Дальнейшего эффекта можно добиться путем применения тестолактона, обладающего антиандрогенной и слабой прогестагенной активностью. Главные немедикаментозные способы лечения гирсутизма — электролиз и лазерная терапия. Особого внимания требует ожирение, поскольку нормализация массы тела часто устраняет инсулинорезистентность. Для ее ослабления в последнее время применяют и пероральные сахароснижающие средства, которые используются в лечении СД 2. Вещества, повышающие чувствительность к инсулину, например метформин и троглитазон, снижают гиперинсулинемию и гиперандрогению яичникового происхождения. Трехмесячное лечение метформином ослабляет инсулинорезистентность и увеличивает ответ надпочечниковых андрогенов на АКТГ. Действие инсулина при СПКЯ усиливает также D-хироинозитол, который снижает и уровень андрогенов в сыворотке крови. Это вещество активирует пострецепторные пути передачи инсулинового сигнала. Секрецию инсулина при поликистозе яичников снижает блокатор опиатных рецепторов налтрексон.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания










Комментарии