Аномалия Тауссиг-Бинг: диагностика, особенности, лечение, последствия
Термин «аномалия Taussig-Bing» применяют в двух разных значениях, которые нельзя смешивать. Если его применяют в физиологическом смысле, имеют в виду широкое обозначение любой формы ДВПЖ, которая гемодинамически соответствует транспозиции, а именно когда насыщение в легочной артерии выше, чем в аорте, из-за преимущественного поступления крови из левого желудочка в легочную артерию. Если в это название вкладывают анатомический смысл, то имеют в виду конкретный порок, описанный Taussig и Bing в 1949 г. Van Praagh уточнил анатомическое определение этого порока в 1968 г. Подаортальный и подлегочный конусы отделяют аортальный и легочный клапаны от AV-клапанов. Полулунные клапаны лежат «бок о бок» на одном уровне. Имеется большой подлегочный ДВПЖ, расположенный выше септальной ножки и мышечной межжелудочковой перегородки. Дефект межжелудочковой перегородки, будучи подлегочным, не сливается с легочным клапаном и отделен от него свободной стенкой подлегочного конуса. Это истинный ДВПЖ, при котором аорта отходит полностью от правого желудочка, в то время как легочный клапан нависает над межжелудочковой перегородкой, но не над полостью левого желудочка. При этом пороке выводной тракт из правого желудочка в аорту часто сужен. Порок нередко сопровождается коарктацией аорты, митральным клапаном-наездником. Встречается расщепление митрального клапана, но не как часть АВСД. Возможна недостаточность клапана. Он может стать причиной обструкции выводного тракта и компрометировать ДМЖП. Бивентрикулярная коррекция в этих анатомических условиях опасна.
Сопутствующие аномалии
Типичными сопутствующими аномалиями являются стеноз или АЛА, которые отмечаются у половины больных при всех, включая подлегочную, локализациях ДМЖП. Достаточно часты пороки аорты — клапанный и субаортальный стеноз, коарктация и перерыв дуги. Коарктация и гипоплазия аорты и другие формы обструкции выводного тракта левого желудочка чаще встречаются при аномалии Taussig-Bing. В частности, сужение выводного тракта аорты специфично для подлегочного ДМЖП. Выводной тракт как бы вклинен между вентрикулоинфундибулярной складкой с латеральной стороны и медиально выдающейся внутрь желудочка инфундибулярной перегородкой.
Сопутствущие пороки AV-клапанов представлены АВСД, стенозом или атрезией клапанов, расщеплением передней створки митрального клапана, клапанами-наездниками, нависающими клапанами, перекрестным AV-соединением.
Иногда встречаются варианты порока с дискордантным, одножелудочковым AV-соединением, с атрезией AV-клапана, с предсердным изомеризмом. Кроме того, отхождению магистральных сосудов от правого желудочка сопутствуют многие другие пороки сердца — ОАП, гипоплазия желудочков, аномалии системного венозного возврата, юкстапозиция предсердных ушек, situs inversus totalis, декстрокардия, дефект ДМПП, коронарный синус, открывающийся в левое предсердие.
В Национальном институте сердечно-сосудистой хирургии им. Н.М. Амосова АМН Украины с 1991 по 2004 гг. прооперированы 352 пациента с ДВПЖ.
Рестриктивный ДМЖП, потребовавший резекции части перегородки, встречался при всех типах ДВПЖ с разной частотой:
-
при тетрадном типе — 26%;
-
при изолированном ДМЖП — 33,3%;
-
при ТМА — 50%;
-
при удаленном ДМЖП — 79,2%.
Хордальный аппарат перегородочной створки трехстворчатого клапана, прикрепляющийся к краю ДМЖП и потребовавший его отсечения и последующей реимплантации, встретился у 5,1% больных.
Гемодинамика и клиника
Гемодинамика и клиника зависят от расположения дефекта, наличия или отсутствия легочного стеноза и сопутствующих аномалий.
-
Подаортальный ДМЖП без СЛА.
При подаортальном ДМЖП без СЛА оксигенированная кровь поступает прямо из левого желудочка в аорту, а венозная — в легочную артерию, поэтому цианоз отсутствует или слабо выражен. При отсутствии ОБЛС легочный кровоток усилен, давление в легочной артерии равно системному, имеются признаки застойной сердечной недостаточности. Клиническая картина аналогична таковой при изолированном большом ДМЖП. Характерны отставание в развитии, одышка, усиленный верхушечный толчок, усиленный II тон, систолический шум, иногда на верхушке — убывающий диастолический шум.
ЭКГ-признаки часто соответствуют АВСД. Угол a QRS — от 300 до 1700, гипертрофия правого или обоих желудочков, а также левого предсердия, иногда АV-блокада I степени.
Рентгенограмма: кардиомегалия, выступает дуга легочного ствола, усилен легочный рисунок.
-
ДВПЖ типа тетрады Фалло с легочным стенозом.
Несмотря на подаортальное расположение ДМЖП, при СЛА часть венозной крови поступает в аорту. Это приводит к цианозу и снижению объема легочного кровотока. Клиническая картина напоминает тетраду Фалло: задержка развития, цианоз, пальцы в виде барабанных палочек, усиленный II тон не расщеплен, систолический шум у верхнего левого края грудины.
ЭКГ: отклонение оси вправо, гипертрофия правого предсердия и правого желудочка, блокада правой ножки пучка Гиса.
Рентгенограмма: нормальные размеры сердечной тени с приподнятой верхушкой. Легочный рисунок ослаблен.
-
Обоюдосвязаннй и удаленный ДМЖП.
Отличительной особенностью является слабый цианоз с признаками усиленного легочного кровотока.
Эхокардиограмма у новорожденного и младенца почти всегда позволяет поставить диагноз с учетом всех интересующих хирурга подробностей. Она должна констатировать 3 признака отхождения магистральных сосудов от правого желудочка:
-
отхождение обоих магистральных сосудов от правого желудочка;
-
наличие единственного выхода из левого желудочка через ДМЖП;
-
отсутствие или наличие митрально-аортального контакта.
Одновременно выясняются все анатомические подробности, необходимые для принятия хирургических решений: взаимная ориентация, относительные размеры магистральных сосудов, диаметр и локализация дефекта, наличие СЛА, его выраженность и характер — динамический или фиксированный. Должны быть оценены расстояние между легочным и трехстворчатым клапанами, степень развития конусной перегородки, наличие прикрепления к ней хорд, анатомия коронарных артерий, наличие сопутствующих аномалий.
Ангиокардиография
Катетеризация и ангиокардиография могут понадобиться только у более старших детей для исключения ОБЛС и у пациентов с транспозиционным типом ДВПЖ для выполнения предоперационной баллонной атриосептостомии в целях улучшения смешивания крови и, следовательно, для повышения артериальной оксигенации и стабилизации состояния ребенка. Ангиокардиография еще не утратила своего значения для диагностики самого порока и деталей его анатомии. Классификация ангиокардиографических признаков построена на основе взаимного положения магистральных артерий и расположения ДМЖП.
Сосуды расположены «бок о бок», аорта — справа от легочной артерии, полулунные клапаны — на одном горизонтальном уровне. Во фронтальной плоскости хорошо видны подаортальный и подлегочный конусы, разделенные инфундибулярной перегородкой. Оба конуса отделяют полулунные клапаны от атриовентрикулярных, что также видно в боковой проекции. В боковой проекции определяется ДМЖП ниже аортального конуса.
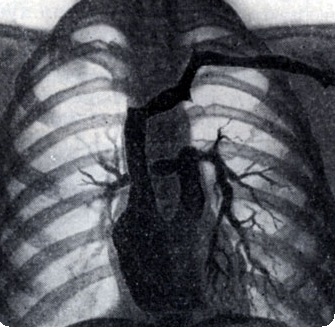
На ангиокардиограмме во фронтальной плоскости при введении контрастного вещества в правый желудочек видно, что сосуды расположены «бок о бок». Хорошо развиты билатеральные конусы. Внедрение в правый желудочек конусной перегородки обычно выражено меньше, чем при подаортальном дефекте. В ранней фазе правожелудочковой ангиокардиограммы обнаруживается высокий ДМЖП, непосредственно связанный с легочным клапаном. Между ДМЖП и легочным клапаном отсутствует конус.
Обоюдосвязанный ДМЖП ангиокардиографически трудно отличить от подлегочного дефекта. Классическими признаками при АВСД являются деформация выводного тракта левого желудочка, вызванная аномальным прикреплением левого АV-клапана, и дефицит межжелудочковой перегородки.
Переднезаднее расположение магистральных сосудов при ДВПЖ хорошо определяется в боковой проекции. Виден билатеральный конус. При мальпозиции магистральных артерий часто обнаруживается клапанный и подклапанный стеноз легочной артерии. В боковой проекции левожелудочковой ангиокардиограммы можно легко определить подлегочный ДМЖП.
Естественное течение
Вследствие морфологической гетерогенности течение различных подтипов ДВПЖ неодинаково. Наиболее показательные данные представили две группы исследователей. Hornberger и соавторы сообщили об исходах у 62 плодов, у которых до родов диагностирован ДВПЖ. Прерывание беременности имело место в 34 случаях, в 2 случаях наступила внутриутробная смерть, 5 детей умерли в неонатальном периоде и 4 — до года жизни. Семнадцать выживших детей составляют 27,4% полной эмбриональной когорты. Samanek и Voriskova сообщили о судьбе 69 детей, родившихся с ДВПЖ. Более 13% из них умерли в течение недели после рождения. В течение первого месяца жизни кривая выживаемости стабилизировалась на 78,6%. Снижение выживаемости продолжалось до 3-летнего возраста, и в среднем она составила 47,8%. Между 3-м и 5-м годами жизни кривая снизилась только на 2,9% и между 5-м и 10-м годами — на 1,5%. Выживаемость осталась на уровне 43,4%.

Большой неожиданностью для кардиологов стала находка у женщины в возрасте 65 лет ДВПЖ с незащищенным сосудистым ложем.
Естественное течение у больных без легочного стеноза может сопровождаться застойной сердечной недостаточностью с развивающейся впоследствии ОБЛС. У больных с аномалией Taussig-Bing тяжелая ОБЛС развивается в раннем возрасте. Сопутствующие аномалии ухудшают прогноз. В казуистических случаях происходит фетальное спонтанное закрытие ДМЖП.
При наличии СЛА отмечаются осложнения, характерные для всех цианотических ВПС.
Лечение
Медикаментозное
При застойной сердечной недостаточности дополнительно назначают дигоксин и диуретики, по показаниям проводят профилактику бактериального эндокардита.
Хирургическое
В передовых западных кардиохирургических центрах сложилось твердое убеждение в том, что полную коррекцию порока целесообразно выполнять в неонатальном периоде, даже в случаях, когда необходимо применить кондуит, требующий замены уже в ближайшие после операции годы. Несмотря на то, что системно-легочный анастомоз является разумной альтернативой, он не уменьшает количества вмешательств, которые предстоит перенести пациенту, и удлиняет период патологической физиологии, который может повлиять на качество окончательного результата.
Паллиативные операции
В настоящее время суживание легочной артерии у больных с застойной сердечной недостаточностью выполняется редко и главным образом при наличии удаленного от сосудов ДМЖП. Эта процедура является единственным паллиативным вмешательством при ДВПЖ с подаортальным дефектом без СЛА. Показания к ней должны быть обоснованными, прежде всего из-за высокой летальности, которая достигает 16%, и необходимости второй, радикальной коррекции порока. Надо отметить, что при ДВПЖ типа ТМА суживание легочной артерии является фактором риска при последующей операции артериального переключения. Более того, эта операция не гарантирует значительного улучшения состояния пациента и может осложниться развитием инфундибулярного и легочного стенозов, субаортального стеноза и миграцией тесьмы к бифуркации легочной артерии. Однако при хронической сердечной недостаточности на фоне высокой легочной гипертензии или таких сопутствующих пороков, как множественные ДМЖП, АV-клапаны-наездники и коарктация аорты, может быть выбрано этапное лечение.
Суживание легочной артерии выполняют через левую переднебоковую торакотомию или через трансстернальный доступ. После вскрытия перикарда выделяют ствол легочной артерии. Тесьму предварительно размечают согласно формуле Trusler: длина ее равна 20 мм + количество миллиметров, численно равное массе тела, при неосложненных вариантах, и 24 + количество миллиметров, численно равное массе тела — при осложненных. Тесьма должна иметь ширину 3-4 мм, ее проводят вокруг средней части ствола легочной артерии и сшивают по предварительно нанесенным меткам. Давление периферийнее тесьмы должно составлять менее 50% системного давления, а насыщение крови кислородом по показаниям пульсоксиметра не должно быть ниже 80-85%. Если эти параметры не достигнуты, тесьму ослабляют или суживают до получения необходимых показателей.

Для больных с подаортальными и обоюдосвязанными ДМЖП лучшим выбором считается первичная полная коррекция порока.
При аномалии Taussig-Bing паллиативная помощь пациентам заключается в суживании легочной артерии и расширении межпредсердного сообщения для улучшения смешивания венозной и артериальной крови и для декомпрессии левых отделов сердца. Во время последующей радикальной операции межпредсердное сообщение позволяет использовать одну венозную канюлю в правом предсердии, через которую дренируются левые отделы сердца. Благодаря этому обеспечивается сухое операционное поле, если вмешательство выполняется в условиях постоянной гипотермической перфузии с низким объемом кровотока. В зависимости от ситуации производят баллонную или ножевую септостомию или операцию Hanlon-Blalock.
Больные с выраженным цианозом, обусловленном СЛА, нуждаются в системно-легочном анастомозе.
Полная коррекция
В связи с выраженным полиморфизмом данного порока применяются различные виды хирургических вмешательств. Залогом их успеха является точная дооперационная оценка анатомического варианта и расчетливый выбор типа операции. При принятии тактических решений целесообразно воспользоваться хирургической классификацией порока, отражающей сложность хирургической задачи. Полная коррекция показана:
-
пациентам с неосложненными пороками — атриовентрикулярной конкордантностью, единственным ДМЖП, сбалансированными желудочками, без наличия AV-клапана-наездника, без аномалий легочного ствола и центральных ветвей;
-
больным с подлегочным стенозом;
-
пациентам, имеющим сложные дополнительные аномалии — клапан-наездник, АВСБ, гипоплазию клапана или желудочка, предсердный изомеризм, множественные ДМЖП, АЛА, петлю легочной артерии, несливающиеся легочные артерии, аномальный дренаж системных или легочных вен.
В настоящее время применяются 4 типа хирургических вмешательств:
1. Формирование внутрижелудочкового туннеля, соединяющего левый желудочек с аортой. При рестриктивном ДМЖП или с целью улучшения геометрии туннеля выполняют частичную резекцию конусной перегородки. Внутрижелудочковый туннель является своеобразным ресивером или демпфирующей камерой, которая может создавать эффект, аналогичный аневризме левого желудочка. Поэтому при ДВПЖ, на наш взгляд, объем левого желудочка должен приближаться к требованию, высказанному Kirklin, т. е. он должен быть равным или больше 30 мл/м2. В противоположность ДВПЖ, успешная коррекция тетрады Фалло у детей первого года жизни может быть выполнена при объеме левого желудочка 18—20 мл/м2.
2. Использование клапанных или бесклапанных кондуитов или альтернативной кондуитам операции Lecompte.
3. Операция артериального переключения с отведением с помощью заплаты легочного ствола в левый желудочек.
4. Один из вариантов операции Fontan. Дополнительным вмешательством является операция Damus-Kaye-Stansel, которая применяется при гипоплазии корня аорты, субаортальном стенозе и аномальном прохождении коронарных артерий.
-
Субаортальный или обоюдосвязанный ДМЖП.
Коррекция при этом типе ДВПЖ впервые опубликована Kirklin и соавторами в 1957 г. Сейчас первичную полную коррекцию порока выполняют в раннем возрасте, в пределах 6 мес. жизни. Она состоит в создании внутрижелудочкового туннеля между ДМЖП и субаортальным выводным трактом с помощью дакроновой или перикардиальной заплаты, обработанной глютаральдегидом.
При субаортальном ДМЖП летальность составляет около 5%, при обоюдосвязанном ДМЖП она выше.
-
Подлегочный ДМЖП.
Впервые коррекция этого порока была выполнена в 1962 г.. Хирургическое лечение следует проводить в ранние сроки из-за быстрого развития необратимых изменений в легочных сосудах. Гемодинамические нарушения соответствуют таковым при ТМА, поэтому принципы коррекции схожи. В основе их лежит переключение потоков артериальной и венозной крови на артериальном или предсердном уровнях.
-
Создание туннеля между ДМЖП и легочной артерией с предсердной инверсией.
Гемодинамическая коррекция на предсердном уровне стала возможной с 1963 г., когда была внедрена операция Mustard, предусматривающая предсердную инверсию и отведение легочной артерии через ДМЖП в левый желудочек с помощью заплаты.
В настоящее время эта операция не применяется из-за высокой госпитальной летальности и осложнений в отдаленном периоде: серьезных нарушений ритма, недостаточности трехстворчатого клапана, обструкции системного или легочного венозного возврата, функциональной недостаточность системного желудочка со снижением переносимости физических нагрузок.
-
Операция Damus-Kaye-Stansel, туннель между ДМЖП и устьем легочной артерии, кондуит между правым желудочком и легочной артерией.
Отведение легочной артерии в левый желудочек через ДМЖП, соединение пересеченной легочной артерии с аортой и имплантация клапанного экстракардиального кондуита между правым желудочком и дистальной легочной артерией, предложены для коррекции сложной формы ТМА, впервые применены для коррекции ДВПЖ с подлегочным ДМЖП в 1982 г..
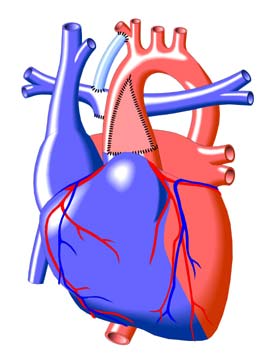
Эта операция создает вентрикулоартериальную конкордантность без необходимости перемещения коронарних артерий и в прошлом рассматривалась, как возможность избежать последствий сопутствующего субаортального стеноза. Причиной обструкции системного выводного тракта является смещение инфундибулярной перегородки вправо и кверху. Недостаток этой операции заключается в имплантации кондуита, вероятности тромбоза корня аорты и возникновении недостаточности аортального клапана. В настоящее время эта операция не применяется при лечении аномалии Taussig-Bing и вытеснена операциями артериального переключения или внутрижелудочковой инверсией. Несмотря на то, что артериальное переключение стало операцией выбора при коррекции аномалии Taussig-Bing, операция Damus-Kaye-Stancel используется как резервный вариант в случаях, когда отсутствует возможность трансплантации коронарных артерий при таких анатомических факторах, как отхождение огибающей артерии от правой коронарной артерии, или при раннем ветвлении левой главной коронарной артерии, которое ограничивает мобильность левого коронарного устья.
-
Внутрижелудочковая коррекция аномалии Taussig-Bing.
Наиболее привлекательным методом лечения ДВПЖ с подлегочным дефектом является полная внутрижелудочковая коррекция без артериального переключения и использования экстракардиального кондуита. Известно 4 типа таких операций:
1. Задний тубулярный кондуит по Abe.
2. Передний тубулярный кондуит по Doty.
3. Передний спиралевидный туннель по Patrick и McGoon.
4. Задний прямой туннель по Kawashima.
-
Операции Abe и Doty.
Обе методики предусматривают создание внутрижелудочкового целиком или частично тубулярного кондуита, соединяющего ДМЖП с аортой. Abe предлагал помещать его позади легочной артерии, когда магистральные сосуды располагаются «бок о бок». Для переднезадней ориентации крупных сосудов Doty предложил конструкцию пути из желудочка прямо кпереди вдоль перегородки к свободной стенке правого желудочка. Затем тубулярный кондуит поворачивают резко вправо и кпереди от легочной артерии и пришивают к субаортальному конусу. Линия шва проходит в передней стенке правого желудочка и служит заплатой в выводном тракте правого желудочка. Таким образом, бесклапанный внутрижелудочковый кондуит функционирует с нативным аортальным клапаном. Обеим операциям присущи одинаковые недостатки: отсутствие роста, формирование псевдоинтимы и, следовательно, развитие субаортального стеноза. По этой причине данные операции не применяются.
-
Операции Patrick-McGoon и Kawashima.
Для коррекции ДВПЖ с подлегочным стенозом предложены два метода конструирования внутрижелудочкового туннеля между ДМЖП и аортой: операция Patrick-McGoon и операция Kawashima. Создание туннеля между ДМЖП и аортой представляется хорошей альтернативой операции переключения, однако зачастую является технически невыполнимой.
Операция Kawashima производится при расположении магистральных сосудов «бок о бок», когда расстояние между трехстворчатым и легочным клапанами достаточно для формирования свободного внутрижелудочкового туннеля. Операцию выполняют доступом через трехстворчатый клапан или поперечную вентрикулотомию. Туннель, соединяющий левый желудочек с аортой, проходит позади легочной артерии между легочным и трехстворчатым клапанами. Конусная перегородка должна быть резецирована для обеспечения свободного выводного тракта.
ДМЖП расширяют, только если он небольшой. Для больных с косой или переднезадней ориентацией магистральных сосудов операция Kawashima непригодна из-за близости легочного и трехстворчатого клапанов. В этих случаях показана операция Patrick-McGoon или артериальное переключение.
При аномальном прикреплении хордального аппарата трехстворчатого клапана к конусной перегородке и при наличии нависающего или «верхом сидящего» митрального клапана выполнение этого типа операции невозможно. Операцию рекомендуют выполнять в раннем младенческом возрасте как первичное вмешательство.
-
Операция Patrick-McGoon.
Если трехстворчатый и легочный клапаны расположены слишком близко, заплата должна быть размещена вокруг передневерхнего края легочного клапана.
Техника Patrick-McGoon была разработана для коррекции порока с косой или переднезадней ориентацией магистральных сосудов. Она предусматривает формирование длинного и геометрически сложного внутрижелудочкового туннеля, который проходит слева и спереди клапана легочной артерии, соединяя ДМЖП с аортой. Поскольку туннель проходит впереди легочной артерии, формирование его не зависит от расстояния между легочным и трехстворчатым клапанами. При этой методике часто требуется расширение ДМЖП, даже когда он нерестриктивный. Хирургическая летальность — около 15%.
Операция Patrick-McGoon впоследствии была заменена на артериальное переключение.
Артериальное переключение с одновременным созданием внутрижелудочкового туннеля между ДМЖП и легочной артерией является предпочтительной операцией. Ее выбирают в случаях, когда отсутствует обструкция выходного тракта правого желудочка и когда левый желудочек технически проще соединить с легочной артерий, чем с аортой. Операция должна быть выполнена в течение первого месяца жизни. Эталонный уровень летальности ниже 10%.
-
Удаленный ДМЖП.
При удаленном ДМЖП у большинства больных технически возможно внутрижелудочковое туннелирование, за исключением случаев предсердного изомеризма, сочетающегося с выраженным в разной степени желудочковым дисбалансом. В этих ситуациях показана операция Fontan. Анатомическую коррекцию этого варианта порока впервые выполнил Kirklin в 1977 г. Несмотря на удобное для туннелирования расположение дефекта, летальность в недалеком прошлом достигала 50%. Сравнительно большую группу — 23 пациента — представили Belli и соавторы, которыми была произведена двухжелудочковая коррекция:
-
у 21 пациента выполнено туннелирование;
-
у 2 — операция артериального переключения с отведением легочной артерии в левый желудочек.
В половине случаев понадобилось расширение дефекта кпереди. У 2 пациентов с рестриктивным приточным ДМЖП и аномальным прикреплением хорд трехстворчатого клапана, препятствующим формированию субаортального тракта, пришлось отказаться от двухжелудочковой коррекции. Двое больных умерли на госпитальном этапе. Восемь пациентов подвергнуты 9 повторным операциям, 6 из них — по поводу субаортального стеноза. Примерно такие же результаты с применением артериального переключения и внутрижелудочковым туннелированием у 10 пациентов с одним летальным исходом представили Lacour-Gayet и соавторы. Barbero-Marcial и соавторы предложили использование нескольких заплат для коррекции ДВПЖ с удаленным ДМЖП. Эта техника облегчает операцию, делая ее реальной, когда коррекция с помощью одной заплаты представляется невозможной.
Одним из наиболее сложных вариантов удаленного дефекта является полная форма AВСД. Некоторым больным из этой подгруппы может быть выполнена двухжелудочковая коррекция, другим — одножелудочковая паллиативная гемодинамическая операция по Fontan. Wilkinson в 2002 г. представил результаты хирургических вмешательств у 23 пациентов, перенесших различные радикальные и паллиативные операции, с одним летальным исходом. Tchervenkov считает условием, облегчающим создание тракта оттока левого желудочка, резекцию перегородки и увеличение дефекта кпереди, назвав его «транслокацией дефекта межжелудочковой перегородки». При сопутствующем сужении легочного выводного пути использовался кондуит.
Сопутствующий клапан-наездник, крисс-кросс сердце и гипоплазия одного из желудочков практически исключают возможность выполнения двухжелудочковой коррекции. Для лечения сложных анатомических комплексов применяется гемодинамическая коррекция по Fontan. В последние годы непосредственные и среднесрочные результаты этого типа операций значительно улучшились благодаря внедрению этапного лечения и фенестрации внутрипредсердного туннеля.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания








Комментарии