Аномалии легочных вен: лечение
При отсутствии легочной венозной обструкции по мере естественного снижения ЛСС прогрессивно увеличивается объемная перегрузка правого желудочка. Развивается застойная сердечная недостаточность, лечение которой проводят гликозидами и диуретиками. Если межпредсердное сообщение недостаточно для обеспечения системного кровотока и безотлагательная операция не показана, должна быть выполнена баллонная септостомия для увеличения сообщения.
После внедрения в клиническую практику простогландина Е1 обструктивная форма ТАДЛВ остается единственным пороком, требующим неотложного хирургического вмешательства. Паллиативные методы операций не существуют. В связи с состоянием крайней тяжести перед проведением диагностических процедур и оперативного вмешательства пациенты должны быть интубированы и вентилироваться с 100% содержанием кислорода в дыхательной смеси и положительным давлением на выдохе. Проводится коррекция метаболического ацидоза. Инфузия простогландина Е1 может быть полезной. Открытие боталлова протока простогландином увеличивает сердечный выброс за счет право-левого шунта через проток. Однако у детей с тяжелой гипоксемией из-за сниженного легочного кровотока увеличение системного выброса сердца достигается только ценой дальнейшего снижения легочного кровотока. Тем не менее, если насыщение смешанной венозной крови повышается с увеличением сердечного выброса, инфузия простогландина оправдана.
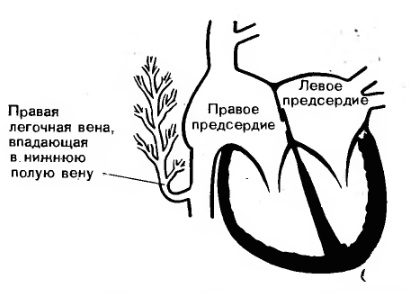
Временная стабилизация состояния не является поводом для малейшей отсрочки операции. В некоторых центрах родившегося ребенка непосредственно из родильного зала переводят в кардиохирургическую операционную, где эхокардиографический диагноз подтверждается на операционном столе.
Для увеличения системного сердечного выброса иногда применяют атриосептостомию, хотя при готовности к ургентному вмешательству она не нужна. Другие катетерные вмешательства бесполезны при обструктивном ТАДЛВ.
Хирургическое лечение
Смысл коррекции вне зависимости от типа аномалии состоит в направлении легочного венозного возврата в левое предсердие путем создания свободного сообщения между общей легочной веной и левым предсердием, прерывания связи коллектора легочных вен с системным венозным кровообращением и закрытия ДМПП. Перед коррекцией порока следует идентифицировать все четыре легочные вены и их аномальное соединение для исключения смешанного типа порока. Операцию выполняют в условиях ИК или во время периода остановки кровообращения и глубокой гипотермии. Остановка кровообращения, как правило, необходима из-за интенсивного поступления крови из венозного коллектора.
Уместно привести некоторые проблемы и оптимальные технические приемы их решения, общие для всех типов ТАДЛВ. У ряда пациентов левое предсердие имеет маленькие размеры. Расширение его с помощью заплаты не повлияло на выживаемость, поэтому хирургическое увеличение объема левого предсердия не стало обязательным элементом операции.
До настоящего времени существуют различные мнения о том, следует ли перевязывать восходящую или нисходящую вертикальные вены. При малом левом желудочке вертикальная вена разгружает левые отделы благодаря лево-правому сбросу крови в течение первых часов или дней после коррекции. И, наоборот, во время легочного гипертонического криза системный кровоток может поддерживаться за счет право-левого сброса через вертикальную вену. Описан некроз печени после лигирования нисходящей вертикальной вены. Stark принимает решение после отключения ИК: если при пробном пережатии турникетом вертикальной вены давление в левом предсердии не повышается, а артериальное давление не падает, вертикальную вену необходимо перевязать. В противном случае ее оставляют открытой. Чаще всего так поступают у пациентов с инфрадиафрагмальным ТАДЛВ. Только изредка вертикальная вена в отдаленном периоде не закрывается спонтанно и сохраняется сброс крови слева направо. В этих случаях ее перекрывают с помощью катетерной технологии или хирургическим путем.
Аналогичный эффект оказывает небольшой дефект овальной ямки, когда при легочной гипертензии благодаря право-левому шунту поддерживается системный кровоток.
В некоторых случаях расстояние между коллектором легочных вен и левым предсердием слишком велико для выполнения анастомоза без натяжения. В этих условиях вертикальную вену дважды перевязывают и пересекают, достигая большой мобильности общей легочной вены. Если принято решение о лигировании вертикальной вены, ее перевязывают вблизи от безымянной вены, чтобы избежать ошибочного направления верхней левой легочной вены в безымянную вену.
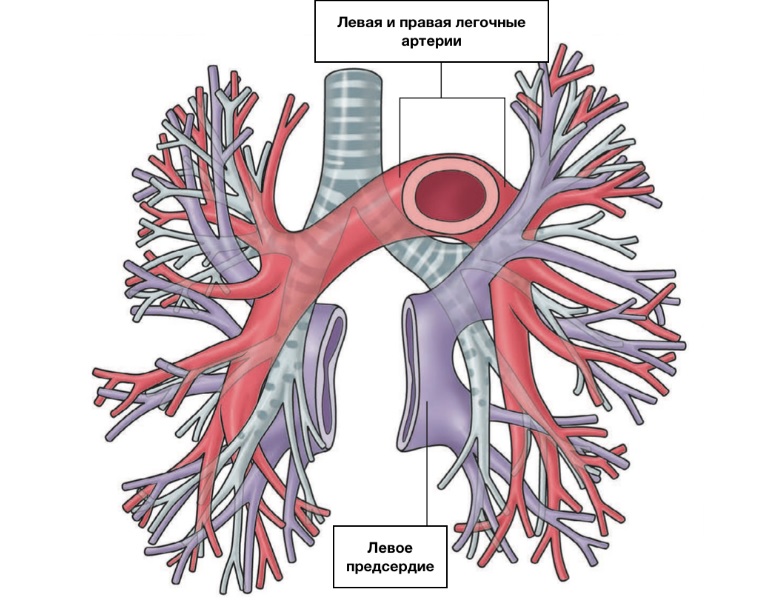
Анестезия и ИК при ТАДЛВ
Новорожденный в состоянии гипоксии и ацидоза требует педантичного анестезиологического обеспечения. Необходимо максимально снизить сопротивление легочных артерий путем гипервентиляции 100% кислородом. Анестезию проводят высокими дозами фентанила, который снижает реактивность легочных сосудов. Если требуется инотропная поддержка, ее целесообразно осуществлять в сочетании с изопротеренолом для предупреждения чрезмерной тахикардии. При этом следует учитывать, что при умеренной гипоплазии левых отделов сердца высокая частота сердечных сокращений – до 200 уд/мин – может быть необходимой для поддержания адекватного сердечного выброса. Проводят коррекцию ацидоза, уровня сахара и дефицита кальция. Иногда у ребенка обнаруживают сепсис и почечную недостаточность. Дигоксин, скорее всего, мало полезен, кроме того, он снижает порог для фибрилляции желудочков.
Перед началом операции должен быть обеспечен венозный доступ и мониторирование артериального давления предпочтительно проводить через пупочную артерию. Датчики пульсоксиметра следует установить на нескольких конечностях. Важно не допускать чрезмерного наружного охлаждения, поскольку у этих крайне тяжелых детей может возникнуть фибрилляция желудочков при сравнительно высокой температуре тела, особенно если ребенок при поступлении получал высокие дозы дигоксина.
После выполнения срединной стернотомии удаляют левую долю вилочковой железы. Очень важно избегать лишних манипуляций на сердце, так как можно спровоцировать фибрилляцию желудочков. Канюлируют восходящую аорту и правое предсердие через ушко одной канюлей. Выделяют и сразу после начала ИК перевязывают артериальный проток. Это следует сделать во всех случаях, так как легочная гипертензия может маскировать проходимость протока на дооперационной ЭхоКГ и даже при аортографии. При нестабильном состоянии больного проток не закрывают до начала перфузии. Незакрытый артериальный проток может привести не только к перегрузке легких, но и к воздушной эмболии системных артерий во время остановки кровообращения.
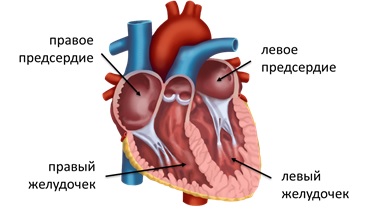
Коррекция обструктивного инфракардиального ТАДЛВ
Больного охлаждают. По достижении температуры тела 25 0С пережимают аорту и вводят кардиоплегический раствор в корень аорты. При продолжающейся перфузии и дальнейшем охлаждении сердце осторожно выворачивают из полости перикарда для выделения аномальной вертикальной нисходящей вены. Важно пережимать аорту перед вывихиванием сердца, иначе могут перегнуться коронарные артерии и возникнет недостаточность аортального клапана. Нельзя сильно мять сердце при выделении. Вертикальную вену перевязывают 5/0 проленом на уровне диафрагмы, затем ее пересекают и разрезают вдоль до уровня верхних легочных вен. После этого сердце опускают в перикард. После снижения ректальной температуры до 18 0С, температуры в пищеводе – до 13-14 0С, а височной – до 15 0С кровообращение останавливают, кровь дренируют в аппарат, венозную канюлю удаляют и тесьмой обжимают полые вены.
Существуют три способа выполнения анастомоза коллектора легочных вен с левым предсердием. Один из них предусматривает выполнение соустья при вывернутом из перикарда или ротированном вправо во вскрытую плевральную полость сердцем. Производят разрез задней стенки левого предсердия, параллельный разрезу коллектора легочных вен. Выполняют анастомоз, стараясь не сузить соустье. Сердце опускают в полость перикарда. Через правую атриотомию закрывают ДМПП.
Второй, более щадящий для сердца способ описан Jonas. Он аналогичен методу, который чаще всего применяется для коррекции супракардиального ТАДЛВ. Производят поперечный разрез стенки правого предсердия от ушка, далее кзади через овальное окно в левое предсердие. Поскольку правые легочные вены не связаны с левым предсердием, достигается хорошая экспозиция ранее выделенной вертикальной вены. Выполняют разрез задней стенки левого предсердия книзу, параллельно вертикальной вене. Разрез может быть продлен кверху в основание ушка левого предсердия, но не на его стенку, поскольку она очень тонка. Он не должен также подходить близко к кольцу митрального клапана, чтобы не повредить огибающую коронарную артерию. Анастомоз выполняют 6/0 рассасывающейся нитью. Преимуществами данного способа являются удобный доступ, минимальная возможность перегиба или неточного совпадения отверстий в левом предсердии и в коллекторе легочных вен, что возможно при альтернативной технике, предусматривающей выворачивание сердца из полости перикарда. Кроме того, вынутое из полости перикарда сердце быстрее согревается.
Для минимизации частоты одного из осложнений послеоперационного периода – недостаточного размера соустья между легочными венами и левым предсердием – предложена новая техника создания левого предсердия с использованием заднего перикарда. Этот метод первоначально был предложен Lacour-Gayet и соавторами в 1996 г. в качестве повторной «бесшовной» коррекции остаточного нарушения оттока из легочных вен. Левое предсердие отсекали от легочных вен и пришивали к заднему перикарду in situ, избегая прохождения линии шва по краям разреза легочных вен. Отечественные хирурги оперировали этим методом 16 пациентов, у которых в среднем через 4 мес. развилась прогрессирующая легочная венозная обструкция. Госпитальная летальность составила 27% при билатеральной обструкции. У 5 из 7 выживших больных зарегистрировано нормальное давление в легочной артерии в сроки наблюдения 26 мес.
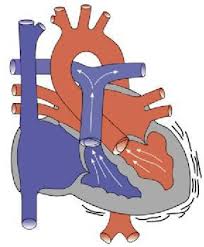
Овальное окно закрывают перикардиальной заплатой. Прямое ушивание овального окна нежелательно, так как может сузить анастомоз. Использование заплаты из перикарда позволяет по выбору оставить дозируемое отверстие для декомпрессии правого предсердия справа налево в раннем послеоперационном периоде. Это целесообразно делать при исходной тяжелой обструкции и ожидаемых легочных гипертонических кризах в первые дни после операции. В заплате высекают отверстие диаметром 3 мм. Перед закрытием межпредсердного дефекта левые отделы сердца заполняют физиологическим раствором и воздух удаляют через отверстие для кардиоплегии в восходящей аорте. После ушивания разреза правого предсердия производят его реканюляцию и возобновляют ИК. Снимают зажим с аорты, оставляя открытым отверстие для кардиоплегии. Во время периода согревания вводят катетеры для мониторирования давления в легочной артерии и в правом предсердии. Давление в левом предсердии не мониторируют из-за малого диаметра легочных вен и возможности кровотечения из левого ушка. Несмотря на относительное недоразвитие левых отделов сердца, именно правый желудочек определяет сердечный выброс в условиях сохраняющейся легочной гипертензии, поэтому с точки зрения оценки объемной нагрузки определение давления в правом предсердии сразу после операции и в отделении интенсивной терапии является наиболее информативным.
Попытку отлучения от ИК можно начинать при температуре в прямой кишке около 35 0С. Это критический момент, так как в ответ на ИК временно повышается сопротивление легочных сосудов. Нередко в течение 10-15 мин после отключения насоса давление в легочной артерии достигает системного уровня. В это время решающее значение приобретает режим вентиляции легких. Она должна проводиться 100% кислородом, желательно с оксидом азота и с рСО2, сниженным по крайней мере до 30 мм рт. ст., но не ниже 25 мм, при котором может ухудшиться перфузия мозга. При отсутствии оксида азота полезен изопротеренол в качестве инотропного средства, обладающего способностью снижать сопротивление легочных артерий. При достаточно широком анастомозе давление в легочной артерии падает в течение 15-30 мин после отлучения от перфузии до 2/3-1/2 системного уровня. Если давление не снижается, следует заподозрить недостаточные размеры соустья. Интраоперационная двухмерная ЭхоКГ с эпикардиальным датчиком дает хорошее изображение места анастомоза. Чреспищеводная ЭхоКГ у новорожденных чревата опасностью сдавления анастомоза даже при использовании очень маленького датчика.
Коррекция супракардиального ТАДЛВ
Существует несколько методов коррекции супракардиального ТАДЛВ, которые с одинаковым успехом применяют различные хирургические школы.
Одним из вариантов операции является создание экстракардиального соустья между общей легочной веной и куполом левого предсердия с использованием верхнего доступа. Эти структуры находятся между аортой и верхней полой веной. Для обеспечения оптимальной экспозиции восходящую аорту и легочную артерию отодвигают влево, а ВПВ – вправо. Вертикальную вену перевязывают у места ее впадения в безымянную вену, не повреждая диафрагмальный нерв, который проходит вдоль латеральной стенки вертикальной вены и места впадения правой верхней легочной вены. Доступ удобен и не искажает естественного расположения сердца и венозных структур. Производят поперечный разрез коллектора легочных вен и параллельно ему разрез купола левого предсердия, начиная от основания ушка левого предсердия. Коллектор и левое предсердие анастомозируют между собой, стараясь не сузить соустье. Шов выполняют рассасывающейся мононитью или полипропиленом. Через правую атриотомию закрывают ДМПП. Изредка возникает необходимость увеличить левое предсердие.
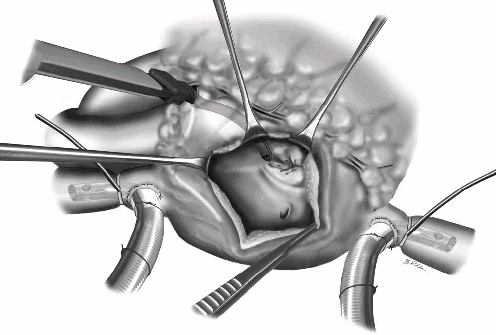
При правом латеральном доступе заднее прикрепление перикарда пересекают, правые легочные вены отделяют от правого и левого предсердий. Таким образом, полые вены и предсердия можно свободно поднять над перикардом, покрывающим коллектор легочных вен. Левую вертикальную вену выделяют изнутри перикарда. Если требуется экстраперикардиальный доступ, диафрагмальный нерв отделяют от перикарда и вены. Используют острую препаровку при условии хорошей видимости, так как повреждение вены может вызвать необходимость преждевременной перевязки. В этом случае коллектор должен быть немедленно открыт продольным разрезом для предупреждения тяжелого легочного венозного застоя. Разрез передней стенки коллектора может быть сделан во время охлаждения. Этот прием предупреждает застой в легких, когда сокращения сердца становятся неэффективными в поздней фазе охлаждения.
После удаления венозной канюли останавливают кровообращение. Желудочки остаются в их естественном положении, а предсердия оттягивают вперед и влево, экспонируя левое предсердие. Заднюю стенку левого предсердия открывают разрезом, перпендикулярным к межпредсердной борозде. Его продолжают в направлении к межпредсердной перегородке вправо, стараясь не вскрыть полость правого предсердия. Для создания достаточного по размеру соустья разрез при необходимости продлевают до основания ушка левого предсердия. Если есть сомнения в определении места разреза задней стенки левого предсердия, используют полезный прием: через короткое атриотомическое отверстие и овальное окно вводят изогнутый зажим в левое предсердие и его кончиком выпячивают заднюю стенку, намечая место разреза.
Задний перикард, покрывающий коллектор легочных вен, и переднюю стенку коллектора рассекают между двумя ранее наложенными швами-держалками. Разрез должен быть сделан на всю длину общей легочной вены. Необходимо четко видеть и не повредить устья всех четырех легочных вен.
Коллектор легочных вен анастомозируют с левым предсердием 6/0 полипропиленовым швом. Шов начинают с дальней от хирурга точки таким образом, чтобы вколы были изнутри коллектора. Швы-держалки позволяют избежать перекоса верхней и нижней губы анастомоза. Линию шва завершают отдельными или непрервными стежками. Перед завершением анастомоза левые отделы сердца заполняют холодным физиологическим раствором. Поскольку анастомозируемые структуры тесно прилегают друг к другу, формируется широкое соустье без натяжения. Овальное окно или ДМПП могут быть закрыты со стороны левого предсердия или через небольшой разрез правого предсердия. После завязывания швов возобновляют ИК вначале с небольшой объемной скоростью. Оставляют кардиоплегическое отверстие в аорте для удаления воздуха. После снятия зажима с аорты начинают согревание. При восстановлении тонуса сердца аорту вновь пережимают на короткий период, легкие ритмично раздувают для удаления воздуха через пункционное отверстие в аорте. Венозное давление удерживают на уровне 5-6 мм рт.ст. для возобновления сердечного выброса.
Чрездвухпредсердная коррекция, которой чаще всего пользуются на территории СНГ, предложена Shumacher и King. Разрез начинают от основания ушка правого предсердия и направляют к межпредсердной борозде. Далее его продолжают кзади через межпредсердную перегородку в левое предсердие. Разрез на задней стенке левого предсердия направляют к устью ушка левого предсердия, которое остается интактным. Таким образом, разрез открывает оба предсердия, создавая удобный доступ для анастомоза. Затем рассекают переднюю стенку общего коллектора легочных вен. Анастомоз между коллектором и левым предсердием начинают от дальнего угла близко к устью ушка. Используют с двумя иглами нить 7/0 пролена. Шов должен быть выполнен тщательно, так как кровотечение из этой области трудно остановить после отключения аппарата. Ушко левого предсердия иногда инвагинируется, прикрывая место начала шва. Полезно наложить лигатуру на его верхушку. Легкое подтягивание ее влево облегчает экспозицию. Сначала анастомозируют верхний, затем нижний край общей вены. Когда обе линии шва встречаются, перегородку закрывают ушиванием или заплатой. Предпочтение отдается пластике перикардом, так как ушивание дефекта может привести к сужению анастомоза.
Отечественные хирурги возобновляют ИК после завершения анастомоза, если использовалась бикавальная канюляция. Если же использовалась одна венозная канюля, кровообращение возобновляется после ушивания предсердия.
-
Коррекция чреспредсердным доступом.
Стенку правого предсердия разрезают параллельно атриовентрикулярной борозде. Иссекают мембрану овального окна. Заднюю стенку левого предсердия рассекают поперечно, попадая в полость перикарда. Рассекают переднюю стенку коллектора легочных вен длинным разрезом от бифуркации левых легочных вен до правых вен. Общую легочную вену анастомозируют с левым предсердием непрерывным швом 7/0 проленом. Линию шва ведут, начиная от левых легочных вен и далее вправо. Вколы делают изнутри легочной вены. Овальное окно закрывают заплатой из перикарда, чтобы увеличить вместимость левого предсердия.
Коррекция интракардиального ТАДЛВ
Существуют два метода коррекции ТАДЛВ в коронарный синус. Обе техники предусматривают рассечение «крыши» коронарного синуса для обеспечения свободного оттока легочной венозной крови в левое предсердие. Вначале иссекают мембрану коронарного синуса, затем после рассечения коронарного синуса в направлении задней стенки сердца образовавшийся большой дефект закрывают заплатой из аутоперикарда.
В целях снижения частоты брадиаритмий после операции Van Praagh с коллегами предложили методику «фенестрации», которая заключается в рассечении общей стенки между коронарным синусом в глубину левого предсердия и закрытии отдельно устья коронарного синуса в правом предсердии и овального окна. В случае повреждения задней стенки предсердия ее ушивают изнутри, так как снаружи сердца это сделать сложнее.
Данная техника позволяет сохранить ткань между коронарным синусом и овальным окном, где расположены важные межузловые проводящие пути. Их пересечение при использовании традиционной методики приводит к брадиаритмиям. Потенциальным недостатком данной техники является возможность получения рестриктивного сообщения между коронарным синусом и левым предсердием, хотя в Бостонском центре, где она была предложена, это осложнение не возникало.
Если двухмерная ЭхоКГ обнаруживает обструкцию в месте соединения коронарного синуса с коллектором легочных вен, следует выполнить коррекцию, которая применяется при супракардиальном ТАДЛВ. Переднюю стенку общей легочной вены рассекают и производят параллельный разрез задней стенки левого предсердия, продленный до основания ушка левого предсердия. Выполняют прямой анастомоз непрерывным швом.
-
Коррекция ТАДЛВ в правое предсердие.
У новорожденных используют гипотермическую остановку кровообращения, а у старших грудных детей – бикавальную канюляцию. С помощью перикардиальной заплаты отводят устья легочных вен в левое предсердие через ДМПП, который при необходимости расширяют.
Коррекция смешанного ТАДЛВ
Техника операции зависит от конкретной анатомии порока. Обычно часть легочных вен дренируется в коронарный синус, а другие впадают непосредственно в правое предсердие. Если только одна вена дренируется аномально, ее можно не корригировать без существенных гемодинамических последствий. Разумно оставить аномальное дренирование в случаях, когда коррекция чревата осложнениями, например, при изолированном дренаже одной легочной вены высоко в верхнюю полую вену. Отведение ее в левое предсердие может осложниться повреждением синусового узла или питающей артерии.
Проблемы отлучения от ИК
Иногда правый желудочек не способен генерировать высокое давление, которое необходимо в раннем периоде после отлучения от ИК. В этих редких случаях проводят ЭКМО в течение нескольких дней, пока постепенно не снизится ЛСС. Те же канюли, которые использовали во время операции, применяют для подключения ЭКМО. Их выводят через разрез грудины. Рану не стягивают, закрывают пришитой к коже заплатой и покрывают клеящейся синтетической пластиной.
Ранние осложнения
У многих младенцев с ТАДЛВ имеется различная степень отека легких перед операцией, поэтому в некоторых случаях отек сохраняется и после операции. У этих пациентов давление в левом предсердии обычно выше, чем в правом. Важно мониторировать давление в обоих предсердиях и пытаться поддерживать максимально низкое давление в левом предсердии, совместимое с достаточным сердечным выбросом. Причинами длительного сохранения отека легких могут быть недостаточной величины анастомоз и малые размеры левого желудочка. Эхокардиографическое исследование в послеоперационном периоде может подтвердить или исключить эти версии. По наблюдениям, конечно-диастолический объем левого желудочка у маленького ребенка обычно увеличивается в первые дни после операции вдвое, например, с 5 до 10 мл, особенно если вертикальная вена после соответствующей пробы была перевязана. Если возросшая преднагрузка левого желудочка привела к снижению его сократимости, это означает, что резерв Франка-Старлинга исчерпан. При неэффективности диуретической терапии возникает необходимость перевезти ребенка в операционную и удалить лигатуру на вертикальной вене, будучи уверенными, что при этом не снижается сердечный выброс. Изредка хирурги прибегают к этому приему.
Легочные гипертонические кризы нередко осложняют ранний послеоперационный период у детей с ТАДЛВ. В связи с утолщением мышечного слоя легочные артерии особенно лабильны в течение нескольких дней после операции. Различные раздражающие факторы могут вызвать сокращение резистивных сосудов и легочные гипертонические кризы. Вентиляция и постоянный наркоз являются главными средствами для снижения сопротивления легочных сосудов. Артериальное рСО2 следует поддерживать на уровне 30 мм рт. ст. Концентрация кислорода и оксида азота во вдыхаемой смеси должны поддерживать давление в легочной артерии на уровне менее двух третей системного давления. Показано введение бета-адренергических блокаторов, таких, как феноксибензамин, или малых доз изопротеренола до 0,1 мкг/кг массы тела в минуту в течение 24-48 ч. После указанного периода гемодинамической стабильности глубину наркоза можно уменьшить, наблюдая за эпизодами рецидива гипертонических кризов. Обычно они возникают в ответ на эндотрахеальное отсасывание, которое следует проводить осторожно после гипервентиляции.
Повреждение диафрагмального нерва может произойти при выделении вертикальной вены или при наружном охлаждении сердца льдом. Ранняя пликация диафрагмы сокращает продолжительность послеоперационного восстановления.
Результаты хирургического лечения
В течение последнего десятилетия опубликованы совокупные данные о динамике госпитальной летальности в различные исторические периоды хирургического лечения ТАДЛВ. Хирургическая летальность снизилась с 85% в 1960-х годах до 5% в некоторых центрах в 1990-х годах. Pédiatrie Cardiac Care Consortium представил результаты первичных операций у 437 пациентов с ТАДЛВ, выполненных между 1985 и 1993 гг. Госпитальная летальность при различных типах ТАДЛВ составила:
-
14,2% – при супракардиальном;
-
11,6% – при интракардиальном;
-
32,6% – при инфракардиальном;
-
15,8; – при смешанном;
-
31% – при невыясненном месте аномального соединения.
Общая хирургическая летальность при изолированном ТАДЛВ достигает 16%. В большинстве центров происходит постоянное улучшение непосредственных результатов, в том числе и новорожденных с тяжелыми обструктивными формами порока. Этого удалось достичь, в частности, благодаря применению ЭКМО. Существует множество вариантов анатомии смешанных типов ТАДЛВ, хирургическое лечение которых по-прежнему сопровождается повышенным риском.
Хирургическая летальность среди пациентов, имеющих дополнительные сложные пороки сердца, исключая асплению, составляет 31%, а в случаях асплении она достигала 54,5%. Среди 127 пациентов, оперированных в Детском госпитале Бостона в 1980-2000 гг., общая летальность составила 17%, из них 34% – у больных с одним желудочком и 9% – у больных с двумя желудочками. Похожие результаты получены в Toronto Hospital for Siek Children. Летальность в простых случаях снизилась с 26 до 8% за период с 1982 по 1996 гг., в то время как в сложных случаях она оставалась постоянной на уровне 52%. Ни возраст, ни предсердный изомеризм не влияли на летальность. Только одножелудочковое сердце и сопутствующие аномалии являлись факторами риска.
Актуарная выживаемость больных по Kaplan-Meier до 1970-х годов составляла на первой неделе 74%, к 6 мес. – 67%, к 5 годам – 63% и к 20 годам – 59%. С 1970 г. значительного улучшения выживаемости после операции не происходило. С 1990 г. выживаемость в течение первой недели составила 94%, к 6 мес. – 85% и к 5 годам – 75%.
Несмотря на улучшение результатов лечения ТАДЛВ, стеноз легочных вен после операции остается одной из ведущих причин непосредственной и отдаленной летальности. Это осложнение чаще всего отмечается при инфракардиальном и смешанном дренаже. Обструкция легочных вен может быть как односторонней, так и двусторонней. Дооперационные сужения легочных вен встречаются у 2,2-7,6% пациентов с ТАДЛВ. Однако стриктуры отдельных легочных вен могут развиться после операции вследствие гиперплазии интимы.
Результаты реопераций по поводу обструкции легочных вен неоднозначны. При односторонних сужениях повторные вмешательства достаточно эффективны, даже в случаях почти полной окклюзии. Попытки установить с помощью катетерной технологии стенты в легочные вены не имели успеха. При двусторонней обструкции результаты повторных операций неудовлетворительные. Единичные случаи успеха связывают с новой техникой создания левого предсердия с использованием заднего перикарда, хотя при первичной коррекции достоверные преимущества этого метода не выявлены. Ожидается, что эта техника будет способствовать снижению ныне высокой летальности при обструктивных формах ТАДЛВ, сочетающихся с одножелудочковым AV-соединением.
Техника бесшовной коррекции стеноза легочных вен после операций по поводу ТАДЛВ была предложена Lacour-Gayet и предусматривает использование in situ перикарда для создания нового предсердия. Операция предполагает рассечение передней стенки суженных легочных вен от места их анастомозирования с левым предсердием до корня легкого. Выделяют широкую полу перикарда, не повреждая задних сращений. Перикард изгибают над открытыми устьями легочных вен и пришивают к стенке левого предсердия на расстоянии от венозных устий. Таким образом, создается новое предсердие, в которое дренируются легочные вены.
Отечественные хирурги сообщили о 14 пациентах с двусторонним сужением легочных вен, подвергнутых повторной операции. Они сравнили два метода – ре конструкцию вен с помощью заплаты и описанный выше метод создания нового левого предсердия. В первой группе было 67% неудач, во второй – 29%. Хотя количество наблюдений у разработчиков нового метода и у их последователей невелико, новая операция предоставляет новые возможности лечения этого грозного осложнения.
Для оценки состояния пациентов в отдаленном послеоперационном периоде используют комплекс инструментальных исследований:
-
рентгенографию грудной клетки;
-
сканирование легких;
-
цветное допплеровское исследование отдельных легочных вен.
Односторонний отек легкого на рентгенограмме является признаком перераспределения кровотока в ответ на обструкцию венозного возврата на противоположной стороне. Это можно подтвердить перфузионным сканированием легких, которое демонстрирует наличие преимущественного кровотока во «влажном» легком. Цветное допплеровское исследование дает представление о нарушении потока крови из легочных вен противоположной стороны. Место и механизм обструкции выявляются также при ангиографии легочного сосудистого русла методом заклинивания или при селективной инъекции контрастного вещества в легочные вены. Для изучения послеоперационной анатомии легочных вен чрезвычайно полезны МРТ, ангиография. Гемодинамическое значение стеноза можно оценить с помощью фазовой контрастной МРТ.
После анатомически успешной коррекции ТАДЛВ у части пациентов зарегистрированы суправентрикулярные аритмии, несмотря на отсутствие симптоматики, а также редкие случаи полной AV-блокады, поэтому рекомендуется периодический амбулаторный ЭКГ-контроль.
У некоторых пациентов, перенесших коррекцию инфракардиального ТАДЛВ, отмечаются эпизоды желудочно-кишечных кровотечений.
В целом функциональные отдаленные результаты хирургического лечения ТАДЛВ отличные. Предоперационными факторами, которые могут ухудшить отдаленные исходы, являются обструкция легочных вен и сопутствующие пороки, особенно предсердный изомеризм и одножелудочковое сердце.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания








Комментарии