Подготовка к операции на сердце. Мониторинг новорожденного
Лечение детей с врожденными пороками сердца представляет анестезиологу широкий спектр анатомических и физиологических аномалий. По тяжести пациенты ранжируются от здоровых и не имеющих симптомов патологии детей младшего возраста с небольшим ДМПП, который требует закрытия, до новорожденных с синдромом гипоплазии левых отделов сердца, требующих агрессивной послеоперационной гемодинамической и респираторной поддержки. Психологические факторы в переплетении с медицинским разнообразием данных о пациентах оказывают влияние, как на самих пациентов, так и на их родителей. Подготовка пациента и его семьи отнимает много времени, но исключение или компромисс в этом вопросе является главным препятствием к успешному исходу и удовлетворенности пациента и родителей. Кроме того, такой командно-ориентированный подход является гарантией для предотвращения ошибок и упущений в придирчивом послеоперационном наблюдении, столь необходимом в комплексной хирургии врожденных пороков сердца. Дооперационный визит дает возможность семье пациента встретиться с хирургом и анестезиологом.

Родители должны быть опрошены об общем состоянии здоровья и активности их ребенка. По существу, общее состояние здоровья и активность будут отражать его кардиореспираторный резерв. Дефицит резерва может указывать на сердечно-сосудистую или другие системы, которые могут влиять на анестезиологический и хирургический риск. Важно определить, имеет ли ребенок сниженную переносимость физических нагрузок. Набирает ли он (или она) вес надлежащим образом или демонстрирует признаки плохой прибавки в весе по причине кахексии на фоне патологии сердца? Имеет ли ребенок признаки застойной сердечной недостаточности (повышенное потоотделение, тахипное, плохое питание, повторные респираторные инфекции)? Имеется ли прогрессирующий цианоз или появление цианотических приступов? Должны быть выявлены любые интеркуррентные заболевания, такие как недавние инфекции верхних дыхательных путей или пневмония. Инфекции нижних дыхательных путей могут потребовать отсрочки проведения предполагаемого вмешательства, исходя из негативного влияния, которое оказывают реактивность дыхательных путей и повышение легочного сосудистого сопротивления на хирургический результат. Повторная пневмония часто ассоциируется с избыточной легочной циркуляцией и изменяет податливость легких у пациентов с повышенным легочным кровотоком.
Хороший анамнез должен описывать предшествующие оперативные и интервенционные вмешательства. Они могут иметь значение, как для хирургического, так и для анестезиологического планирования предстоящей операции. У пациентов, которым выполнялось устранение коарктации аорты с помощью подключичной артерии или накладывался шунт по Блелоку-Тауссиг, измерение системного артериального давления или даже пульсоксиметрические данные не будут корректными, если их мониторирование выполняется на левой руке. Подобным образом, дети с окклюзией бедренной вены после ее катетеризации не могут рассматриваться кандидатами на использование бедренного венозного доступа, особенно для подключения аппарата искусственного кровообращения через бедренную вену, если стернотомия оказывается невозможной. В равной степени важно уточнить прием лекарств в настоящее время, предшествующие анестезиологические проблемы и семейный анамнез, касающийся анестезиологических осложнений.
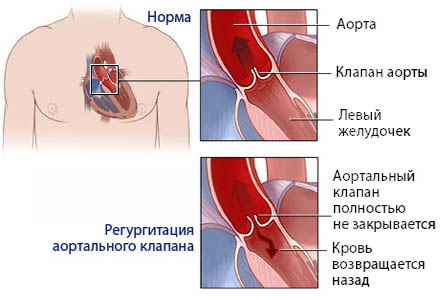
В современную эпоху эхокардиографии и катетеризации камер сердца физикальное обследование редко позволяет получить дополнительную анатомическую информацию о соответствующем пороке сердца. Однако оно чрезвычайно полезно для оценки общего клинического состояния ребенка. Например, болезненный по внешнему виду, кахектичный ребенок с дыхательной недостаточностью имеет ограниченный кардиореспираторный резерв, поэтому применение избыточной премедикации или длительной ингаляционной индукции может привести к выраженной гемодинамической нестабильности.
Медикаменты и лекарственные взаимодействия
Лекарственные взаимодействия существуют как среди сердечно-сосудистых медикаментов, так и между сердечно-сосудистыми и анестезиологическими препаратами. Понимание механизмов воздействия и взаимодействия между лекарствами весьма полезно для детского кардиоанестезиолога.
Дети с онкологическими заболеваниями, которым предстоит операция на сердце или некардиальные вмешательства, могут иметь более высокий сердечно-сосудистый риск, обусловленный кардиотоксической химиотерапией. К часто встречающимся кардиотоксичным веществам относятся:
-
антиметаболит 5-флуроурацил;
-
антрациклиновые антибиотики доксорубицин и даунорубицин;
-
алкилирующий препарат циклофосфамид.
Острый период токсических проявлений характеризуется острыми изменениями сегмента ST и зубца Т на электрокардиограмме (ЭКГ), выраженными дизритмиями, застойной сердечной недостаточностью, обусловленной перикардиальным выпотом. Хроническая кардиотоксическая сердечная недостаточность является кумулятивной, зависимой от дозы и невосприимчивой к терапии дигоксином. Возможно возникновение тяжелой кардиомиопатии, которая связана с дозой препарата, облучением и использованием антрациклина. Летальность при этом может превышать 50%. Такие пациенты должны подвергаться доскональному дооперационному обследованию, включая полный анализ крови, оценку почечной и печеночной функции, коагуляционных параметров и эхокардиограммы. У таких пациентов базовая анестезия изофлураном с N2O дает лучшую гемодинамическую стабильность, чем базовая опиоидная анестезия.
Анестезиологические препараты способны вызывать желудочковую тахикардию типа «torsades de pointes» и злокачественную аритмию. Факторами риска для возникновения желудочковой тахикардии типа «torsades de pointes» являются:
-
женский пол;
-
электролитный дисбаланс (как, например, гипокалиемия и гипомагниемия);
-
генетический полиморфизм ионных каналов при врожденном синдроме удлиненного интервала QT (congenital long QT syndrome - LQTS);
-
субклинический LQTS;
-
базовое удлинение интервала QT и применение лекарств, увеличивающих интервал QT, особенно в высоких концентрациях или при их быстром внутривенном введении.
Состояния с редуцированным резервом реполяризации, такие как застойная сердечная недостаточность или интоксикация дигоксином, также могут способствовать возникновению torsades de pointes.
Лабораторная оценка должна включать анализ уровня гемоглобина, гематокрита, пульсовую оксиметрию и у отдельных пациентов (например, принимающих диуретики или имеющих поврежденную почечную функцию) электролитов сыворотки. Повышенный гематокрит у ребенка с нормоволемическим статусом дает представление о значимости и длительности существования гипоксемии. Уровень гематокрита выше 60% предрасполагает к капиллярному сладжу и вторичному повреждению органов, включая паралич. Несмотря на эти риски, либерализация правила «ничего через рот», которая допускает потребление детьми чистой воды за 2 ч до индукции в анестезию, фактически устраняет необходимость назначения пациентам дооперационной внутривенной гидратации.
Эхокардиография с отображением потока цветным допплером (эхо-допплером) является неоценимым инструментом, который обеспечивает неинвазивное средство оценки внутрисердечной анатомии, вариантов кровотока и оценок физиологических данных. Для большинства пороков сердца при доступности качественной эхокардиографической оценки более инвазивные исследования, как правило, не требуются. Эхо-допплер особенно эффективен для определения внутрисердечных аномалий. Внесердечные аномалии, такие как стенозы легочных артерий или вен, более сложны для распознавания посредством эхо-допплера и часто требуют катетеризации камер сердца. Возможность точной интерпретации анатомии и физиологии требует наличия высококвалифицированного эхокардиографиста, вновь подтверждая необходимость наличия хорошо взаимодействующей интерактивной команды. Несмотря на то, что сложность экстремальных анатомических вариаций и меняющихся условий нагрузки при интерпретации интраоперационной эхо-допплер кардиограммы бросает вызов даже опытному эхокардиографисту. Детский кардиоанестезиолог должен развивать определенную осведомленность в возможностях и ограничениях этого метода, чтобы принимать участие в принятии решений по лечению критических интраоперационных ситуаций.
Магнитно-резонансная томография (МРТ) сердца и магистральных сосудов стала весьма полезным методом неинвазивной визуализации у детей с пороками сердца. Обычно МРТ используется для:
-
сегментарного описания сердечных аномалий;
-
оценки грудной аорты;
-
неинвазивного выявления и качественной оценки шунтов, стенозов и регургитаций;
-
для оценки конотрункальных мальформаций и сложных пороков;
-
для выявления аномалий легочных и системных вен;
-
для периоперационного изучения и оценки врожденной патологии сердца у взрослых.
МРТ особенно полезна для количественной оценки функции желудочков, региональной сократимости, состоятельности клапанного аппарата и картирования скоростных показателей потоков крови. МРТ является крайне полезной для визуализации дуги аорты, легочных артерий и сосудов средостения у детей со сложными пороками сердца. В перечень заболеваний, при которых МРТ обеспечивает точную и нужную информацию входят: коарктация аорты, аномалии легочных артерий, аномалии соединения легочных вен и персистирующая левая верхняя полая вена, а также внутрисердечные туннели, кондуиты и шунты. Выполнение МРТ также целесообразно у пациентов старшего возраста с плохими акустическими окнами и у пациентов с деформациями грудной стенки. У некоторых пациентов МРТ может использоваться как альтернатива катетеризации камер сердца. Однако при использовании этого метода будет невозможно получить такие физиологические данные, как кислородная сатурация. Стресс-МРТ с аденозином используется для выявления зон индуцируемой ишемии.
Катетеризация камер сердца остается золотым стандартом для оценки анатомии и функции у пациентов с врожденной патологией сердца. Несмотря на то, что на многие вопросы, касающиеся анатомии порока, сейчас можно достоверно ответить с помощью неинвазивных методов, при решении комплексных анатомических задач или необходимости получения физиологических данных катетеризация остается важным диагностическим инструментом. Для анестезиолога при катетеризации важными являются следующие данные:
-
Ответная реакция ребенка на седативные препараты.
-
Давление и сатурация во всех камерах и магистральных сосудах.
-
Локализация и величина всех внутри- и внесердечных шунтов.
-
Легочное и системное сосудистое сопротивление.
-
Размеры камер и функция сердца.
-
Анатомия и функция клапанного аппарата.
-
Деформация системных или легочных артерий, связанная с предшествующей операцией.
-
Анатомия коронарных артерий.
-
Анатомия, локализация и функция шунтов, наложенных прежде.
-
Приобретенные или врожденные анатомические варианты, которые могли бы оказать влияние на планируемый сосудистый или хирургический доступ.
Внимательное изучение данных катетеризации и понимание их потенциального влияния на хирургический и анестезиологический план являются жизненно необходимым. Не все медицинские проблемы могут быть оценены и исправлены на дооперационном этапе; хирург, кардиолог и анестезиолог должны обсудить потенциальные проблемы лечения и необходимость дополнительного обследования до поступления больного в операционную. Соответствующий обмен информацией и сотрудничество между специалистами оптимизирует лечение пациента и будет способствовать периоперационному ведению. Как правило, в центрах проводятся регулярные плановые совместные конференции кардиологов и кардиохирургов по обсуждению кандидатов на проведение оперативных вмешательств, в ходе которых вся необходимая информация показывается и обсуждается. Подобные конференции дают неоценимую возможность изучения особенностей пациентов, планируемых для оперативного лечения, а также являются постоянным образовательным форумом, который обеспечивает междисциплинарный обмен, направленный на использование современных представлений, как в медикаментозном, так и в хирургическом лечении врожденной патологии сердца.
Интраоперационное обеспечение новорожденного
Подготовка операционной
Передовые достижения и тщательная подготовка операционной являются базовым принципом. Наркозный аппарат должен иметь возможность подачи воздуха, кислорода, углекислого газа, закиси азота и оксида азота для обеспечения баланса легочного и системного кровотока. Линии для внутривенных инфузий не должны содержать пузырьков воздуха для профилактики парадоксальных воздушных эмболий. Препараты экстренной помощи, промаркированные и готовые к применению, должны включать:
-
сукцинилхолин;
-
хлорид или глюконат кальция;
-
соду;
-
атропин;
-
фенилэфрин (мезатон);
-
лидокаин;
-
адреналин.
Для пациентов высокого риска препараты инотропной поддержки, обычно допамин, должны быть разведены в соответствующих концентрациях и быть готовыми к применению, тогда как дополнительные медикаменты подготавливаются в случае, если вероятность их применения высока. Во всех случаях должны быть доступны определенные анестетики (тиопентал, пропофол, кетамин). В детской кардиоанестезии у многих пациентов имеется ограниченный функциональный резерв, а также высокий эндогенный уровень катехоламинов как адаптационный ответ на имеющуюся патологию сердца. В связи с этим, препараты экстренной помощи должны быть подготовлены и доступны к немедленному применению до индукции в наркоз.
Возможность быстрого изменения температуры тела, как охлаждения, так и согревания, является необходимой в хирургии врожденных пороков сердца. В ходе искусственного кровообращения в условиях глубокой гипотермии пациенты охлаждаются до 18°С. Важными факторами оперативного обеспечения таких пациентов являются наружное охлаждение с помощью водяных согревающих/охлаждающих матрасов и эффективная система контроля температуры в операционной.
Физиологический мониторинг
Мониторинг, используемый у любого пациента, должен зависеть от состояния ребенка и объема планируемого оперативного вмешательства. Неинвазивный мониторинг устанавливается до индукции в наркоз. У беспокойных детей анестезиолог может выбрать отсроченное применение средств мониторинга непосредственно перед индукцией в наркоз. Стандартный мониторинг включает:
-
электрокардиографию;
-
пульсоксиметрию;
-
капнографию;
-
прекардиальную аускультацию;
-
измерение артериального давления манжетой соответствующего размера (осцилометрическим или допплеровским методом).
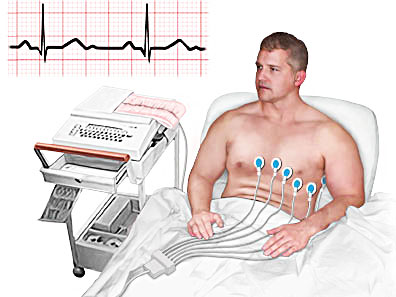
Дополнительный мониторинг включает наличие артериального катетера, температурных датчиков и пищеводного стетоскопа. Катетер Фолея, как правило, используется в тех случаях, когда хирургическое вмешательство предполагает использование искусственного кровообращения или само вмешательство может вызывать ишемию почек, или когда анестезиологический план включает местную анестезию, сопряженную с задержкой мочи. В некоторых центрах при выполнении большинства кардиохирургических операций рутинно осуществляется мониторинг центрального венозного давления (ЦВД). Альтернативно, обычно используют предсердные линии, установленные трансторакально, чтобы получить эту информацию на этапе отключения искусственного кровообращения и в послеоперационном периоде. В этих условиях польза от этой информации или доступа, обеспечиваемого транскутанными катетерами ЦВД в доперфузионном периоде, должна соизмеряться с рисками их постановки.
-
Мониторинг артериального давления.
Непрерывный мониторинг артериального давления возможен только посредством установленного внутриартериального катетера. У детей младшего возраста канюляция лучевой артерии катетерами 22G или 24G размера является предпочтительной. У детей старшего возраста и подростков катетер может быть заменен на размер 20G. Внимательный осмотр, пальпация и определение неинвазивного кровяного давления крови на всех конечностях помогает удостовериться в том, что предыдущие или планируемые в настоящее время оперативные вмешательства (например, предшествующая секция лучевой артерии, подключичный лоскут при коррекции коарктации аорты, шунт Блелока-Таусинг) не повлияют на мониторинг артериального давления в выбранной области. Другие доступные области для канюляции включают локтевую, бедренную, подмышечную и пупочную (у новорожденных) артерии. Канюляции задней большеберцовой (a. tibial posterior) или тыльной артерии стопы (a.dorsalis pedis) обычно недостаточно для сложных оперативных вмешательств. Периферические артериальные катетеры, преимущественно установленные в дистальные отделы нижних конечностей, плохо функционируют после искусственного кровообращения и не отражают центральное давление в аорте, когда температура в дистальных отделах конечностей остается низкой.
-
Мониторинг температуры тела.
Защита миокарда и головного мозга поддерживается, главным образом, за счет гипотермии; поэтому точное и непрерывное измерение температуры тела является чрезвычайно важным. Для этого проводится мониторирование ректальной и назофарингеальной температуры, т.к. они отражают температуру ядра тела и головного мозга, соответственно. Мониторинг пищеводной температуры хорошо отражает температуру сердца и грудной клетки. Тимпанические пробы, хотя и хорошо показывают церебральную температуру, могут привести к разрыву барабанной перепонки.
-
Пульсоксиметрия и капнография.
Пульсоксиметрия и капнография обеспечивают мгновенную обратную связь, касающуюся адекватности вентиляции и оксигенации. Эти показатели весьма полезны для корректировки параметров вентиляции и гемодинамики с целью оптимизации Qp/Qs до и после хирургического наложения шунтов и суживания легочной артерии. Периферический спазм сосудов у пациентов в условиях глубокой гипотермии и остановки кровообращения делает показатели сатурации менее надежными. У новорожденных рекомендуется использование датчика с поверхности языка для обеспечения более «центрального» измерения сатурации с меньшей погрешностью в зависимости от температуры.
Использование трансторакальных (в правом или левом предсердии, легочной артерии) или трансвенозных катетеров в легочной артерии определяется с учетом патогенеза заболевания, физиологического статуса и хирургического вмешательства. Например, у детей, переносящих операцию Фонтена по поводу атрезии трикуспидального клапана или одножелудочкового сердца, крайне полезно наличие катетеров в тракте Фонтена (Fontan pathway) и в легочном венозном предсердии. После операции Фонтена легочная циркуляция должна обеспечиваться уже без непосредственного участия насосной камеры сердца. Едва различимые изменения в преднагрузке, легочном сосудистом сопротивлении и давлении в легочных венах будут оказывать влияние на легочный кровоток и, следовательно, на сердечный выброс. Данные, полученные при измерении системного венозного давления и давления в левом предсердии (left atrial pressure - LAP), помогают оценить относительную значимость внутрисосудистого объема (central venous pressure - CVP), легочного сосудистого сопротивления (CVP-LAP градиент), а также податливость желудочка (LAP), при этом каждый из параметров требует дифференцированного терапевтического подхода.
В качестве общей рекомендации, трансвенозный катетер в легочную артерию у детей массой тела более 7 кг может быть установлен через внутреннюю яремную вену. Катетер 5 Fr используется у детей с массой тела от 7 до 25 кг, и 7 Fr – у детей более 25 кг. Для пациентов весом менее 7 кг чрескожная постановка катетера в легочную артерию может быть выполнена через бедренную вену. Иногда последняя методика требует проведения рентгеноскопии. В большинстве случаев использование интраоперационных трансторакальных линий и допплер-эхокардиографии ограничивает необходимость постановки трансвенозных катетеров в легочную артерию.
Специальный мониторинг новорожденного
Интраоперационная эхокардиография
Среди новейших технологий, доступных для мониторинга пациентов в процессе кардиохирургических вмешательств, наиболее многообещающей является допплер-эхокардиография. В ряде сообщений описывается целесообразность интраоперационной допплер-эхокардиографии при хирургии врожденных пороков. В большинстве операционных ситуаций двухмерная эхокардиография в сочетании с пульсовой допплеровской ультрасонографией и цветным картированием, способна предоставить детальную морфологическую, а также и физиологическую информацию. При помощи допплер-эхокардиографии в операционной могут быть получены анатомические и физиологические данные до начала искусственного кровообращения, помогая, таким образом, уточнению плана операции. Доперфузионная допплер-эхокардиография точно определяет анестезиологическое и хирургическое ведение. По причине отсутствия ограничений доступа при выполнении эпикардиальной и чрезпищеводной эхокардиографии (transesophageal echocardiography - TEE) у пациентов, находящихся под наркозом, нередко выявляются новые данные, изменяющие соответственно и план лечения.
Постперфузионная эхокардиография позволяет дать немедленную оценку результатов хирургической коррекции, а также оценить функцию сердца посредством исследования движения стенок желудочка и систолического утолщения. После завершения искусственного кровообращения эта методика может показать резидуальные структурные дефекты, которые могут быть немедленно устранены в ходе того же оперативного вмешательства, что позволит избежать оставления значимых резидуальных структурных дефектов, которые будут требовать повторной операции в будущем. Выявление пациентов с вновь возникшими нарушениями сократимости правого и левого желудочка после искусственного кровообращения по изменению движения стенок или систолическому утолщению методом допплер-эхокардиографии является руководством к немедленному фармакологическому вмешательству. Важно отметить, что постперфузионная желудочковая дисфункция и резидуальные структурные дефекты, выявленные при допплер-эхокардиографии, сопряжены с повышенной частотой повторных операций и с более неблагоприятным течением болезни, высокой летальностью. Улучшится ли раннее выявление этих нарушений, которые побуждают к соответствующему медикаментозному и хирургическому лечению, еще предстоит установить.
Специализированный мониторинг центральной нервной системы новорожденного
Основной задачей мониторинга головного мозга является улучшение нашего понимания мозговой функции и дисфункции в ходе кардиохирургического вмешательства с целью выработки эффективной стратегии защиты головного мозга. С учетом того, что многие факторы, такие как скорость потока (сердечный выброс), перфузионное давление, температура, гематокрит и PaСО2, определяющие нормальную мозговую перфузию в ходе искусственного кровообращения, становятся управляемыми командой медиков извне, понимание влияния их на головной мозг новорожденных, младенцев и детей является очень важным. Кроме того, исследование головного мозга в необычных биологических условиях, таких как состояние после остановки кровообращения в условиях глубокой гипотермии (deep hypothermic circulatory arrest - DHCA) или в течение непрерывающегося экстракорпорального кровообращения в условиях глубокой гипотермии (18°С), дает уникальную возможность описать цереброваскулярную физиологию и патофизиологию. Многочисленные способы интраоперационного мониторинга головного мозга были использованы для предотвращения вторичного повреждения функции головного мозга без остановки оперативного вмешательства. При оптимальном расположении датчика ТЕЕ крайне полезна для оценки легочного венозного возврата, состоятельности левого атриовентрикулярного клапана после митральной вальвулопластики, для оценки коррекции полного атриовентрикулярного канала и других сложных врожденных пороков сердца. Ранее существовавшие ограничения в визуализации были практически устранены за счет накопления клинического опыта и улучшения двухмерных изображений. В настоящее время детские двухпроекционные чреспищеводные датчики расширили весовые ограничения пациентов до новорожденных 2,5-3 кг. Возможные риски ТЕЕ, которые заслуживают особого внимания, включают компрессию нисходящей аорты и дыхательных путей из-за размера или изгиба датчика. В случае необходимости проведения ТЕЕ до оперативного вмешательства датчик после этого нужно удалить во время операции из-за опасности повреждения пищевода при гипотермии, редуцированном или остановленном искусственном кровообращении.
Вторым методом интраоперационного эхокардиографического исследования является эпикардиальный доступ. Для этого метода необходим короткофокусный 5,0 или 7,0-MHz датчик, помещенный в стерильный чехол, перекинутый от анестезиолога к хирургу через стерильную преграду, который может быть позиционирован на эпикардиальной поверхности сердца. Такая технология способствует наилучшему манипулированию датчиком, которое необходимо для всесторонней оценки основных структур и динамической функции сердца. Преимуществом этого метода является возможность получения всех изображений у пациентов любого размера. Среди недостатков метода выделяют:
-
необходимость достаточных навыков и опыта для проведения исследования;
-
необходимость остановки хода операции для выполнения манипуляций с датчиком;
-
возможное негативное влияние прямого механического воздействия датчика на миокард.
С учетом современных возможностей ТЕЕ эпикардиальный доступ применяется редко.
Главным образом, они включали следующие три методики, изолированно или в комбинации:
-
параинфракрасную спектроскопию (near-infrared spectroscopy - NIRS) для обеспечения измерения венозной составляющей в тканевом насыщении оксигемоглобина;
-
транскраниальный допплер для измерения артериального кровотока и сосудистого сопротивления;
-
электроэнцефалографию (EEG) для определения изменений кортикальной активности, сопряженных с перфузией.
Кроме того, измерение мозгового кровотока и метаболизма в рамках специализированных клинических исследований было крайне важным для нашего дальнейшего понимания функции головного мозга в ходе и после операции. Мультимодальный неврологический мониторинг также используется для того, чтобы обеспечивать проведение искусственного кровообращения, глубокую гипотермию с остановкой кровообращения (DHCA) и регионарную низкопоточную мозговую перфузию (regional low flow cerebral perfusion - RLFP) у новорожденных при реконструкции дуги аорты.
Электроэнцефалографический мониторинг позволяет выявить ишемию или распознать соответствующее снижение мозговой метаболической активности в ходе гипотермии перед DHCA. Электроэнцефалография является полезной для мониторирования физиологических функций центральной нервной системы в течение сердечно-легочного обхода с глубокой гипотермией и полной остановкой кровообращения. Например, в ходе глубокой гипотермии перед полной остановкой кровообращения электроэнцефалограмма (EEG) может выявить остаточную церебральную электрическую активность. Изоэлектрическое безмолвие может быть индуцировано дальнейшим охлаждением, а последующая мозговая активность обнаружена при помощи электроэнцефалографии. Так как резидуальная электрическая активность в течение DHCA сопряжена с продолжающимся церебральным метаболизмом, стремление поддержать состояние изоэлектрического статуса может предотвратить повреждение мозга в течение остановки кровообращения. Электроэнцефалограмма также помогает в определении уровня и глубины анестезии. Послеоперационный электроэнцефалографический анализ показал наличие субклинической судорожной активности у ряда пациентов высокого риска, потенциально связывая данные отклонения с более негативным нейрофизиологическим исходом. Значение интраоперационного электроэнцефалографического мониторинга после искусственного кровообращения и важность полученных данных еще требуют уточнения.
Транскраниальный допплер (TCD) использовался у младенцев в основном с научными целями и позволял выявить аномалии венозного или артериального кровотока, а также микроэмболы. Данная технология использует принцип допплера для определения смещения в частоте отраженных сигналов от крови в средней мозговой артерии с тем, чтобы рассчитать скорость кровотока. Так как диаметр этой крупной мозговой артерии сравнительно постоянный, скорость потока в ней должна приблизительно соответствовать скорости мозгового кровотока (CBF).
Транскраниальный допплер имеет несколько преимуществ:
-
неинвазивность;
-
не требует использования рентгеновского излучения;
-
является средством непрерывного мониторинга.
Дополнительным преимуществом этого метода является его способность оценивать быстрые изменения скорости кровотока, вызванные температурными или перфузионными изменениями, которые часто имеют место в ходе кардиохирургического вмешательства.
К недостаткам транскраниального допплеровского мониторинга относятся:
-
нестабильность данных, особенно при низких скоростях потока, когда малейшие изменения положения головы пациента способны значительно изменять интенсивность сигнала и базовые измерения;
-
недостаток достоверных исследований в течение гипотермического искусственного кровообращения, когда температура наряду с редуцированной скоростью потока и ламинарными характеристиками потока при непульсирующей перфузии способны ограничить точность измерений скорости мозгового кровотока.
Измерения скорости мозгового кровотока при помощи TCD имеют приемлемую корреляцию с большим количеством стандартных измерений мозгового кровотока при нормотермии, а некоторые исследования были посвящены его достоверности и при гипотермическом искусственном кровообращении.
Метод транскраниального допплера использовался для исследования эффектов искусственного кровообращения и остановки кровообращения в условиях глубокой гипотермии на церебральную гемодинамику у детей, а также для оценки частоты мозговой эмболии. Недавние исследования, изучавшие головной мозг с помощью TCD, позволили нескольким исследовательским группам предоставить важную информацию относительно вопросов нормальной и патологической мозговой перфузии при кардиохирургических операциях у детей. Вопросы, касающиеся мозгового перфузионного давления, ауторегуляции, эффекта РаСО2 и температуры были исследованы у детей с помощью транскраниального допплера. Этот метод также позволяет получить качественные данные о наличии газовых эмболов в средней мозговой артерии в ходе вмешательства. Количественное определение этого важного механизма мозгового повреждения при проведении кардиохиругических операций было бы поучительным. Будущие исследования с использованием транскраниального допплера также должны обратить внимание на данный механизм повреждения.
Центры с превосходными результатами могут сообщать об использовании NIRS в послеоперационном периоде у новорожденных с врожденными пороками сердца «всегда» или «никогда». Учитывая тот факт, что была показана корреляция значений церебральной NIRS с венозной сатурацией в луковице яремной вены, интерес к использованию NIRS как способа неинвазивной оценки доставки кислорода к головному мозгу является целесообразным. Austin и соавт. сообщили о значении интраоперационного мониторинга церебральной NIRS. Ими было отмечено, что десатурация мозгового оксигемоглобина являлась причиной большинства нейрофизиологических нарушений в ходе мультимодального мониторирования с использованием NIRS, транскраниального допплера и электроэнцефалографии. Более двух третей пациентов в этом исследовании имели выявляемые при нейромониторировании изменения, а аналогичный процент этих изменений потребовал вмешательств со стороны перфузиолога, хирурга или анестезиолога. Вмешательство хирурга, такое как изменение положения канюли, было выполнено в одной четверти случаев, а вмешательство перфузиолога – более чем в половине случаев. Частота послеоперационных неврологических осложнений также была выше у тех пациентов, у которых данные изменения не корригировались. Мониторирование NIRS в течение некоторых специальных хирургических техник, таких как регионарная мозговая перфузия, продемонстрировало полезность ее использования при интраоперационном ведении. Однако пока еще нет исследований, которые показали бы, что использование NIRS в послеоперационном периоде сопряжено с лучшими результатами неврологического исхода. Изучение церебрального кровотока с помощью технологии клиренса ксенона улучшило понимание цереброваскулярной динамики у младенцев в ходе искусственного кровообращения и, особенно, при глубокой гипотермии и после периода остановки кровообращения. В целом, с помощью этого исследовательского инструмента были описаны эффекты искусственного кровообращения, влияние температуры, различных перфузионных техник на мозговой кровоток, а также, косвенно, на метаболизм головного мозга. Исследования, использующие эту методику, показали, что некоторые механизмы ауторегуляции мозгового кровотока, такие как регуляция «давление – объемный кровоток», утрачиваются при глубокой гипотермии и что церебральная реперфузия ухудшается после периода полной остановки кровообращения.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания








Комментарии