Искусственное кровообращение: принципы, показания, последствия
Физиологические эффекты искусственного кровообращения у новорожденных, младенцев и детей старшего возраста отличаются от таковых у взрослых. В ходе искусственного кровообращения дети подвергаются воздействию биологических крайностей, которые не встречаются у взрослых, включая глубокую гипотермию (18°С), гемодилюцию (от 3 до 4 раз превышающую объем циркулирующей крови), низкое перфузионное давление (20-30 мм. рт. ст.), широкий разброс объемной скорости потока (от 200 мл/кг/мин до полной остановки кровообращения) и различные техники поддержания pH крови (a-stat или рН-stat, либо оба последовательно). Данные параметры существенно отличаются от физиологически нормальных условий и оказывают влияние на способность сохранять нормальную функцию органов в течение и после искусственного кровообращения. Кроме этих заметных изменений, важными факторами могут быть трудноуловимые колебания в пополнении глюкозы, положения канюли, наличие аорто-легочных коллатералей и возраст пациента, влияющие на функцию органов в ходе искусственного кровообращения.
Взрослые пациенты нечасто подвергаются подобным биологическим воздействиям. Так, у взрослых кардиохирургических пациентов температура редко опускается ниже 25°С, гемодилюция является более умеренной, перфузионное давление, как правило, поддерживается на уровне 50-80 мм. рт. ст., объемная скорость потока поддерживается в пределах 50-65 мл/кг/мин, а рН-стратегия имеет меньшее значение из-за использования умеренно низких температур и редкого использования остановки кровообращения. Такие показатели, как пополнение глюкозы, редко представляют собой проблему у взрослых пациентов, вследствие больших запасов гликогена в печени. Венозные и артериальные канюли имеют у них больший размер, но меньше деформируют предсердие и аорту, а их положение более предсказуемо. Несмотря на внешнее сходство, проведение искусственного кровообращения у детей имеет существенные отличия от такового у взрослых. Вследствие этого, у детей предполагаются явные физиологические различия в ответе на искусственное кровообращение. Кроме того, имеются некоторые видоизменяемые интраоперационные факторы, которые могут влиять на нейрофизиологические нарушения.
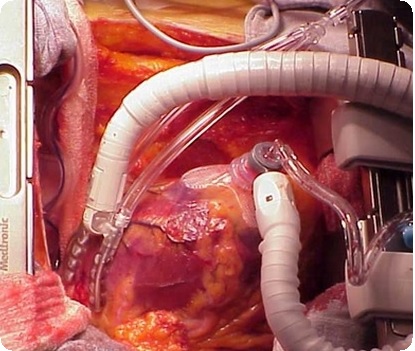
Первичный объем заполнения
Растворы для первичного заполнения, используемые для искусственного кровообращения у детей, имеют огромное значение, ввиду непропорционально большого соотношения первичного объема заполнения с объемом циркулирующей крови. У взрослых первичный объем заполнения эквивалентен 25-33% объема циркулирующей крови пациента, тогда как у новорожденных и младенцев первичный объем заполнения может превышать объем циркулирующей крови на 200%. С использованием современных низкообъемных перфузионных контуров (например, оксигенатор малого объема, магистральные трубки меньшего диаметра) первичный объем заполнения у новорожденных не превышает одного объема циркулирующей крови. Поэтому необходимо заботиться о том, чтобы достигнуть физиологически сбалансированного заправочного раствора и ограничить его объем настолько, насколько это возможно. Большинство педиатрических заправочных растворов, однако, имеют довольно вариабельные уровни электролитов, кальция, глюкозы и лактата. Уровни электролитов, глюкозы и лактата могут быть достаточно высокими, если раствор включает большое количество донорской крови, или низкими, если донорская кровь добавляется в минимальном количестве. Уровень кальция в заправочном растворе обычно очень низкий, это может способствовать быстрому замедлению работы сердца с началом искусственного кровообращения.
Основные компоненты заправочного раствора включают:
-
кристаллоиды;
-
донорскую кровь (чтобы поддержать гематокрит, соответственный температуре);
-
коллоиды.
Другими компонентами, которые могут быть добавлены в заправочный раствор, являются:
-
маннитол;
-
буферные растворы (бикарбонат натрия или тригидрооксиметиламинометан – THAM);
-
стероиды.

Во многих центрах в первичный объем экстракорпорального контура у новорожденных и младенцев добавляют коллоиды или свежезамороженную плазму или используют цельную кровь в заправочном растворе. В эксперименте было показано, что низкая концентрация белков плазмы ухудшает лимфатический отток, изменяет легочную функцию за счет увеличенной капиллярной утечки. Несмотря на то, что у взрослых пациентов добавление альбумина в заправочный объем не продемонстрировало изменений в течение искусственного кровообращения, в одном из исследований высказано предположение о том, что поддержание нормального коллоидного осмотического давления может улучшить выживаемость у детей младшего возраста, подвергающихся искусственному кровообращению.
Добавление свежезамороженной плазмы или цельной крови является попыткой восстановить уровень прокоагулянтов, которые подвергаются значительной дилюции при искусственном кровообращении у детей младшего возраста. У новорожденных и младенцев кровь должна добавляться в заправочный раствор. Большинство центров использует донорскую эритроцитарную взвесь, однако в некоторых применяется и цельная кровь. Использование цельной крови пополняет как уровень эритроцитов, так и факторы свертывания крови от одного донора. Фактически, низкообъемные перфузионные контуры дают возможность перфузиологам и анестезиологам совместно использовать единственную дозу цельной крови, ограничивая, таким образом, контакт пациента с донорской кровью только до одного донора на протяжении всего периоперационного периода.
Добавление любых компонентов крови будет вызывать гораздо большую нагрузку глюкозой в заправочном растворе. Гипергликемия может повышать риск неврологического повреждения, если в процессе перфузии возникает ишемия головного мозга. Добавление маннитола обеспечивает осмотический диурез и удаление из циркуляции свободных кислородных радикалов. Стероиды добавляются для стабилизации мембран, чтобы обеспечить теоретическое преимущество в снижении ионного смещения в течение периода ишемии. Однако стероиды могут повышать уровень глюкозы, что может оказаться пагубным, если случается период мозговой ишемии. Стероиды остаются одним из наиболее дискуссионных дополнений к заправочному раствору. Выбор температурного режима искусственного кровообращения принимается на основании требующихся хирургических условий, учета габаритов пациента, на основании типа вмешательства и потенциального физиологического влияния на организм.
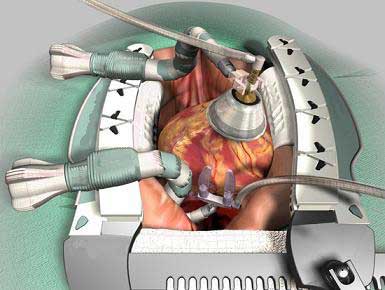
Искусственное кровообращение в условиях умеренной гипотермии является основным методом перфузии, применяемым у детей старшего возраста и подростков. У пациентов данной возрастной группы венозные канюли являются менее выпячивающимися, поэтому сердце способно легко приспособиться к канюляции верхней и нижней полых вен. Бикавальная канюляция сокращает возврат крови в правое предсердие и улучшает хирургическую визуализацию внутрисердечной анатомии. Умеренная гипотермия может быть выбрана и у детей раннего возраста при менее трудоемких вмешательствах, таких как ДМПП или неосложненный ДМЖП. Большинство хирургов охотно канюлируют нижнюю и верхнюю полые вены у новорожденных и младенцев. Однако у этих пациентов подобный подход является технически более сложным и с большей вероятностью способствует возникновению короткого периода гемодинамической нестабильности. Кроме того, эластичность полых вен в сочетании с ригидностью канюль может вызывать обструкцию полых вен, ухудшая венозный возврат и повышая венозное давление в мезентериальном и церебральном сосудистом бассейне.
Искусственное кровообращение в условиях глубокой гипотермии, как правило, резервируется за новорожденными и младенцами, требующими сложных хирургических коррекций. Однако и некоторые дети старшего возраста со сложными пороками сердца или тяжелыми поражениями дуги аорты имеют преимущество при использовании низких температур. В целом, глубокая гипотермия выбирается для того, чтобы позволить хирургу проводить оперативное вмешательство в условиях искусственного кровообращения с редуцированным потоком или при полной остановке кровообращения. Перфузия в условиях низкого потока (50 мл/кг/ мин) улучшает операционные условия для хирурга за счет обеспечения практически «сухого» поля. Глубокая гипотермия с полной остановкой кровообращения позволяет хирургу удалить предсердную и аортальную канюли. При использовании этой методики достигается более точная хирургическая коррекция вследствие «сухого» операционного поля с отсутствием перфузионных канюль. Остановка кровообращения, даже в условиях глубокой гипотермии, привносит обеспокоенность относительно того, насколько хорошо глубокая гипотермия защищает функцию органов и головной мозг, подвергающийся наибольшему риску.

Гемодилюция
Считается, что применение гемодилюции в ходе экстракорпорального кровообращения снижает использование гомологичной крови и улучшает микроциркуляцию за счет уменьшения вязкости крови. Хотя концентрированная кровь обладает улучшенной кислородно-транспортной емкостью, ее вязкость снижает эффективный кровоток через микроциркуляторное русло. При низких температурах вязкость крови существенно повышается и снижается кровоток. Гипотермия в сочетании с непульсирующим потоком при искусственном кровообращении ухудшает текучесть крови через микроциркуляторное русло. При этом возможно возникновение сладжа эритроцитов, развитие окклюзии мелких сосудов и множественных зон тканевой гипоперфузии. Следовательно, гемодилюция является важным аспектом при гипотермическом искусственном кровообращении. Однако необходимый уровень гемодилюции для конкретных температур не вполне определен. Кроме того, гемодилюция снижает перфузионное давление, увеличивает церебральный кровоток, потенциально повышая тем самым микроэмболию головного мозга, и снижает кислородно-транспортную емкость крови.
Одна группа исследователей в эксперименте на животных моделях обнаружила, что чрезмерная гемодилюция до уровня гематокрита менее 10% приводит к недостаточной доставке кислорода, а при уровне гематокрита более 30% имело место лучшее церебральное восстановление после DHCA. Jonas с соавт. подтвердили эти данные в рандомизированном исследовании, в котором использовались два гемодилюционных протокола у детей младше 9 месяцев (гематокрит 20% против 30%). Результаты развития детей были оценены при дальнейшем наблюдении за ними в возрасте 1 года с использованием шкалы Bayley (Bayley Scales of Infant Development). В краткосрочном плане в группе пациентов с более низким уровнем гематокрита имелись самые низкие показатели сердечного индекса, более высокий уровень лактата в сыворотке через 1 ч после искусственного кровообращения и более выраженное увеличение общего содержания воды в тканях в первый послеоперационный день. В возрасте одного года индекс умственного развития был сопоставим, однако, индекс психомоторного развития был существенно ниже в группе пациентов с более низким уровнем гематокрита. Кроме того, дети раннего возраста в группе с более низким уровнем гематокрита имели уровень психомоторного развития в 2 стандартных отклонения ниже среднего. Так как при остановке кровообращения эритроциты служат основным резервуаром кислорода, значение гематокрита близкое к 30%, особенно в ходе согревания, является предпочтительным, когда предполагается использование глубокой гипотермии. В настоящее время большинство центров в ходе искусственого кровообращения поддерживает уровень гематокрита около 25-30%, улучшая доставку кислорода к жизненно важным органам, таким как головной мозг. Доставка кислорода к мозгу является особенно важной, так как мозговая ауторегуляция при глубокой гипотермии и после DHCA ухудшается.
В настоящее время нет данных, определяющих оптимальный уровень гематокрита у пациента после отключения искусственного кровообращения. Решения относительно постперфузионного уровня гематокрита у пациента принимаются на основании функции сердца и анатомии порока после его коррекции. Для пациентов с резидуальной гипоксемией, с умеренной или выраженной миокардиальной дисфункцией целесообразна улучшенная кислородо-транспортная емкость с уровнем гематокрита 40% и выше. Пациенты с физиологической коррекцией и хорошей миокардиальной функцией могут переносить уровень гематокрита 25-30%. Для пациентов с незначительной или умеренной миокардиальной дисфункцией допустимые значения гематокрита, находящиеся между вышеуказанными значениями, представляются вполне разумными. Следовательно, у пациентов с физиологической коррекцией, с умеренно хорошей функцией желудочков и гемодинамически стабильных, риски, сопряженные с трансфузией крови и ее компонентов, должны быть обоснованы непосредственно в течение постперфузионного периода.
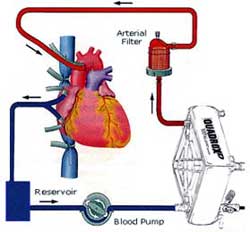
Методы поддержания газового состава крови новорожденного
Теоретическое преимущество метода a-stat перед pH-stat режимом в поддержании газового состава крови во время гипотермического искусственного кровообращения является предметом широкой дискуссии. Несмотря на то, что метод pH-stat, вероятно, не является оптимальным для взрослых пациентов, для которых основным риском повреждения головного мозга является микроэмболия, считается, что у младенцев данные риски ниже из-за отсутствия атеросклеротического поражения. При pH-stat методе добавление СО2 во вдыхаемую газовую смесь при охлаждении в ходе экстракорпорального кровообращения увеличивает церебральный кровоток и может улучшать оксигенацию тканей мозга и конечные результаты.
Спорные вопросы, касающиеся коррекции рН в ходе искусственного кровообращения, были рассмотрены в большом исследовании Бостонского детского госпиталя. В их исследовании дети младше 9 месяцев были рандомизированы на группы с a-stat и pH-stat методиками в ходе искусственного кровообращения и глубокой гипотермии с последующим длительным наблюдением. У детей младше 9 месяцев после бивентрикулярной коррекции различных пороков сердца были оценены результаты неврологического развития. Краткосрочные преимущества, выявленные при рН-stat методе, включают тенденцию к меньшим послеоперационным нарушениям и более короткому периоду восстановления до появления первой электроэнцефалографической активности. У пациентов с транспозицией магистральных артерий была выявлена меньшая длительность интубации и нахождения в отделении ИТ. Однако использование a-stat или pH-stat методики не имело соответствующей связи с лучшими или худшими результатами неврологического развития при наблюдении этих же детей через 2 и 4 года.
Начало искусственного кровообращения
Артериальная и венозная канюли, установленные до начала искусственного кровообращения, могут вызывать серьезные проблемы в периперфузионном периоде. Неправильно расположенная венозная канюля может вызвать обструкцию полой вены. Проблемы венозной обструкции особенно возрастают при искусственном кровообращении у новорожденных, так как артериальное давление у них обычно низкое (20-40 мм рт. ст.), а крупные и относительно жесткие канюли легко деформируют крайне податливые венозные сосуды. Канюля в нижней полой вене может вызывать обструкцию венозного возврата из бассейна внутренних органов, приводя к асциту из-за повышенного гидростатического давления или прямого понижения перфузионного давления в мезентериальных, почечных и печеночных сосудистых ложах. У детей раннего возраста с необъяснимым асцитом может последовать и должна предполагаться значимая почечная, печеночная и гастроинтестинальная дисфункция. Аналогичные проблемы с канюляцией могут привести и к обструкции верхней полой вены. Такое состояние может быть более угрожающим уже в ходе искусственного кровообращения. Следствием подобных обстоятельств могут быть три проблемы:
-
отек головного мозга;
-
ограничение локального или глобального мозгового кровотока;
-
уменьшение доли перфузионного потока, достигающего мозговой циркуляции, и, как следствие, неэффективное охлаждение головного мозга.
В операционной давление в верхней полой вене должно мониторироваться через катетер во внутренней яремной вене, при этом необходимо наблюдать за головой пациента для выявления признаков гиперемии после начала экстракорпорального кровообращения. Обсуждение с перфузиологом вопроса неадекватности венозного возврата и значимого градиента температур во время охлаждения, возникающего между верхней и нижней частями тела, должно насторожить анестезиолога и хирурга относительно наличия потенциальных проблем с венозными канюлями. Пациенты с аномалиями крупных системных вен (дополнительная левая верхняя полая вена или azygos-соединение с прерванной нижней полой веной) представляют собой особенный риск возникновения проблем с венозной канюляцией и дренажом.
Также возможно возникновение проблем с положением аортальной канюли. Аортальная канюля может «соскользнуть» в просвет брахиоцефального ствола и, следовательно, селективно направлять поток крови к правой стороне циркуляции в мозге. Кроме того, положение кончика канюли может вызвать преимущественный поток крови вниз по аорте или вызывать эффект Venturi, обкрадывая мозговую циркуляцию. Наличие такой проблемы было подтверждено в ходе мониторирования церебрального кровотока обнаружением значительной разницы в величинах потоков между правой и левой гемисферами после начала искусственного кровообращения. Наличие крупных коллатералей от аорты к легочной артерии, таких как широкий ОАП, может вызывать сброс крови из русла системной циркуляции в легочное русло, уменьшая, таким образом, церебральный кровоток и эффективность охлаждения головного мозга в ходе искусственного кровообращения. Хирург должен контролировать проток до или непосредственно после начала искусственного кровообращения с тем, чтобы устранить данную проблему, а крупные аорто-легочные коллатерали, если это возможно, должны быть эмболизированы в катетеризационной лаборатории до оперативного вмешательства. Новорожденным с выраженными аномалиями дуги аорты (например, атрезия аорты, перерыв дуги аорты) может потребоваться радикальное изменение техник канюляции, таких как помещение артериальной канюли в ствол легочной артерии с временной окклюзией ее ветвей для обеспечения перфузии тела через ОАП или даже выполнения двойной артериальной канюляции, как восходящей аорты, так и ствола легочной артерии. Подобные приспособления требуют особой бдительности для того, чтобы обеспечить эффективную, полную перфузию и равномерное охлаждение жизненно важных органов.
Как только аортальная и венозные канюли установлены и соединены с артериальной и венозной магистралями экстракорпорального контура, начинается искусственное кровообращение. Работа артериального насоса увеличивается медленно, и, как только обеспечивается беспрепятственный поток, венозная кровь дренируется в кардиотомический резервуар. Скорость потока постепенно увеличивается до тех пор, пока не будет достигнута полная поддержка циркуляции. Если венозный возврат уменьшается, давление в артериальной магистрали высокое или наблюдается чрезмерное среднее артериальное давление, скорость потока должна быть понижена. Высокое давление в артериальной магистрали и неадекватный венозный возврат обычно вызываются неправильным положением или перегибом артериальной или венозной канюль, соответственно. Скорость, с которой венозная кровь дренируется из пациента, определяется разницей высот между пациентом и входным отверстием венозного порта кардиотомического резервуара, диаметром венозной канюли и просвета венозной магистрали. При некоторых обстоятельствах венозный дренаж может быть увеличен за счет использования системы вакуумного ассистирующего дренирования.
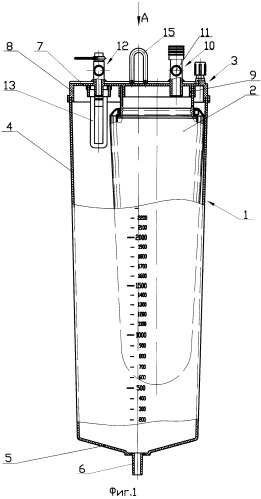
У новорожденных и детей младшего возраста часто используется глубокая гипотермия. По этой причине заправочный раствор сохраняется холодным (от 18° до 22°C). Когда с началом искусственного кровообращения холодный перфузат контактирует с миокардом, частота сердечных сокращений немедленно урежается и сокращение сердца ослабляется. Вклад в общий объем потока крови, нагнетаемый сердцем ребенка, быстро уменьшается. Следовательно, чтобы поддерживать адекватную системную перфузию при нормотермических температурах или близких к ним, артериальный насос должен быстро достигать полной производительности потока.
У новорожденных и младенцев искусственное кровообращение начинается с включения артериального насоса. Как только безопасность аортального потока гарантирована, венозная магистраль разжимается, и кровь начинает перетекать из правого предсердия в экстракорпоральный контур. Поток крови в аорту до раскрытия венозной магистрали имеет целью предотвратить возможные проблемы с кровопотерей, если имеет место диссекция аорты или неправильное положение аортальной канюли. Новорожденные и дети раннего возраста имеют низкое соотношение объема крови к первичному объему заполнения, поэтому, если венозный дренаж будет опережать аортальный поток крови, то внутрисосудистый объем будет стремительно снижаться. После того, как положение аортальной канюли проверено, скорость потока быстро увеличивают с тем, чтобы поддерживать эффективную системную перфузию. Так как у детей патология коронарных артерий встречается редко, миокард должен охлаждаться равномерно, если не происходит деформации коронарных артерий канюлями. При использовании холодного прайма необходимо соблюдать осторожность при использовании артериального насоса до начала искусственного кровообращения. Инфузия холодного перфузата может привести к брадикардии и ослаблению сердечной сократимости еще до того, как хирург подготовится к началу искусственного кровообращения.
С началом искусственного кровообращения тщательное наблюдение должно быть сфокусировано на моментах, гарантирующих правильную сборку контура, адекватную перфузию миокарда и оптимальную декомпрессию сердца. Неэффективный венозный дренаж может быстро привести к перерастяжению желудочка. Это особенно важно для новорожденных и младенцев, у которых имеется низкий комплайнс желудочков, а сердце относительно плохо переносит избыточный прирост преднагрузки. Если все-таки перерастяжение желудочка происходит, скорость потока должна быть быстро снижена, а венозная канюля переустановлена. Альтернативно, сердце может быть разгружено постановкой кардиотомического отсосного катетера или небольшого дренажа в соответствующую камеру сердца.
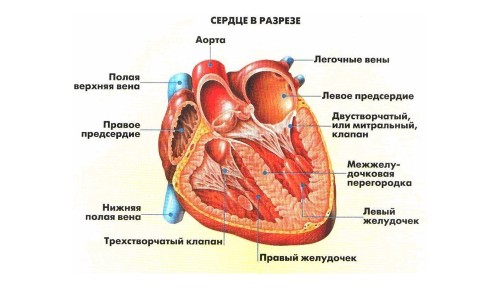
Исторически рекомендации по расчету оптимальной скорости перфузионного потока для детей основывались на массе тела пациента и на признаках эффективности органной перфузии, определяемой по артериальным газам крови, кислотно-основному балансу и общему потреблению кислорода в ходе искусственного кровообращения. При гипотермических значениях температур метаболизм снижается, и, следовательно, скорость перфузионного потока может быть снижена и при этом все еще соответствовать или превышать потребности тканевого метаболизма.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания








Комментарии