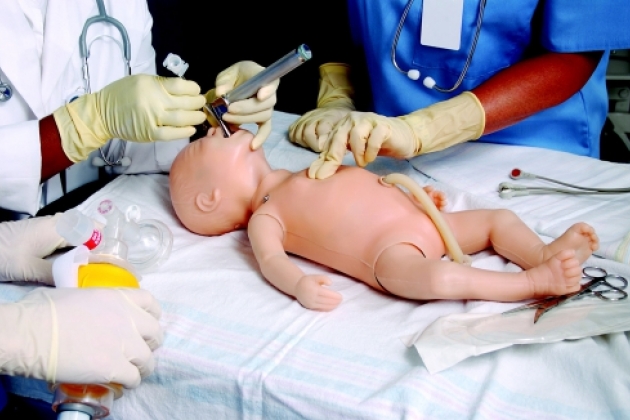
Интубация трахеи у новорожденных. Подготовка к экстубации новорожденного
Размер эндотрахеальной трубки является принципиально важным. Если выбрана слишком большая трубка, она будет оказывать излишнее давление на внутреннюю поверхность крикоидных хрящей, вызовет отек слизистой оболочки и, как следствие, обструкцию дыхательных путей после ее удаления. У детей в возрасте до 10 лет рекомендуется использовать трубки без манжеты, внутренний диаметр которых больше, чем у трубок с манжетой, при том же наружном размере. Внутренний диаметр интубационной трубки определяют в соответствии с возрастом и массой тела пациента.
Из-за более высокого положения глотки и характерной формы надгортанника у новорожденных и детей младшего возраста интубацию трахеи следует проводить, используя прямой клинок ларингоскопа. Им удобнее, чем изогнутым клинком Макинтоша, приподнимать надгортанник. Учитывая, что длина трахеи варьирует, после интубации обязательно проводят аускультативный контроль положения трубки справа и особенно слева, после чего выставляют параметры ИВЛ соответственно возрасту, массе тела и особенностям порока. Интубационная трубка должна быть фиксирована, желательно к верхней челюсти, так как нижняя – подвижная. Оротрахеальный путь интубации считается предпочтительным в большинстве случаев. При назотрахеальной интубации возможно повреждение слизистой оболочки носа, отрыв аденоидов и, как следствие, носовое кровотечение, попадание аденоидной ткани в просвет интубационной трубки с последующей ее обтурацией. Тем не менее, при этом способе интубации трубка фиксируется более надежно. Его также используют, если предполагается длительная ИВЛ.
Введение желудочного зонда рекомендуется проводить после окончания фиксации интубационной трубки. Его используют для контроля количества и качества желудочного отделяемого и разгрузки желудка после интубации, если во время масочной вентиляции в желудок попал воздух. Постановка зонда должна быть аккуратной, так как при повреждении слизистой оболочки пищевода или желудка на фоне применения гепарина возможно неконтролируемое кровотечение.
Для оценки эффективности механической вентиляции необходимо убедится в наличии повторяющейся экскурсии грудной клетки. Частоту ИВЛ – приблизительно 20-35 в 1 мин – устанавливают в зависимости от возраста. Кислородный режим во время ИВЛ у детей младшего возраста и особенно у новорожденных является одним из ключевых условий. Так как интубацию трахеи чаще всего проводят на фоне вентиляции 100% О2, сразу же после определения газов артериальной крови FiO2 снижают до 50-70% под контролем пульсоксиметра, с тем чтобы насыщение крови кислородом было не ниже дооперационного уровня для каждого отдельного порока, а РаО2 – на 45-50 % выше исходного. Такая коррекция FiO2 проводится для того, чтобы предотвратить разрушение сурфактанта – основного фактора, поддерживающего соответствующий уровень поверхностного натяжения в альвеолах. В линию вдоха аппарата ИВЛ должен быть включен нагреватель-увлажнитель дыхательной смеси для поддержания проходимости дыхательных путей и снижения потери жидкости. Обязательно в такой дыхательный контур включают термометр для контроля температуры на вдохе, которая не должна превышать 30-32 ОС, чтобы избежать перегревания больного. Устанавливают PEEP 0-4 см вод. ст., объем вдоха – 10-15 мл/кг. Пиковое давление должно быть не более 20-25 см вод. ст., время вдоха – 0,7-1 с, отношение вдох/выдох – 1:1,2. При обструктивных заболеваниях легких предпочтительнее продлить время выдоха и снизить время вдоха. Увеличение продолжительности вдоха может быть полезным у пациентов с отеком легких, а инверсия отношения вдох/выдох может быть полезной у пациентов с постперфузионным респираторным дистресс-синдромом. Окончательную коррекцию параметров вентиляции проводят по данным газов артериальной и венозной крови.
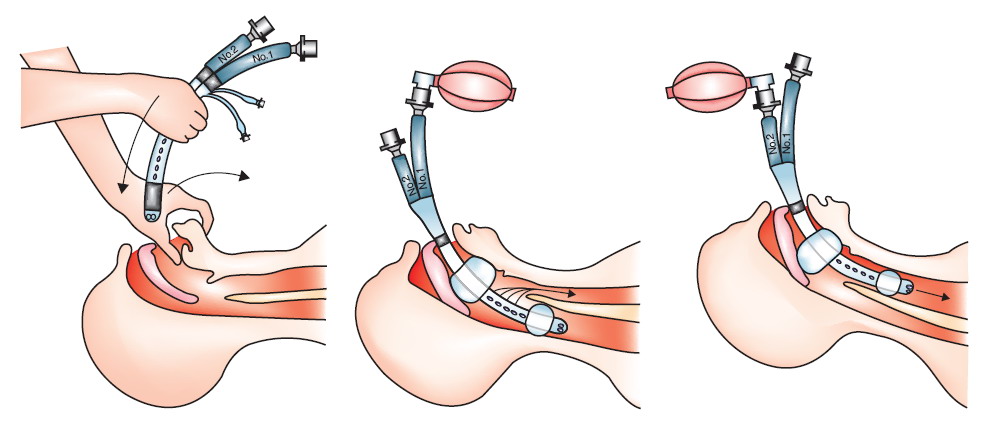
Во время коррекции ВПС, особенно с использованием ИК, режим вентиляции меняют на протяжении операции в зависимости от ее этапа. До начала ИК механическую вентиляцию легких в
большинстве случаев проводят стандартно. РЕЕР на этом этапе используют очень редко, а у пациентов с инфундибулярным стенозом легочной артерии такой режим противопоказан, так как повышает постнагрузку для правого желудочка. В период ИК, когда достигнута расчетная производительность, ИВЛ прекращают. В этот период рекомендуется поддерживать постоянное давление в легких воздухом в пределах 2-4 см вод. ст. для профилактики спонтанного ателектазирования, которое может быть причиной неадекватной оксигенации после окончания ИК. Особенностью маленьких детей является их гидрофильность, поэтому интерстициальное накопление жидкости в легких на протяжении ИК, создавая барьер для диффузии кислорода через альвеолокапиллярную мембрану, вызывает необходимость перехода на ручную вентиляцию и применение 100 % О2 в период выхода из ИК. Такой режим вентиляции позволяет полностью расправить легкие и обеспечить адекватную оксигенацию. Обычно ручную вентиляцию проводят в течение 10-20 мин, после чего ее возвращают в обычный режим ИВЛ. В этот период в линию вдоха должен быть включен нагреватель-увлажнитель дыхательной смеси.
Уход за трахеобронхиальным деревом проводят по мере необходимости. Полезно применение капнографа, но он не заменяет постоянный аускультативный контроль дыхания, который возможен при использовании прекордиального или эзофагеального стетоскопа. Контрольная санация ТБД является обязательной во время параллельной перфузии. Ручная вентиляция в этом случае позволяет более эффективно проводить данную манипуляцию. Процедуру производят осторожно, чтобы не повредить слизистую оболочку, стерильным одноразовым катетером, а для промывания ТБД используют теплый физраствор.

Мониторинг
Контроль венозного давления начинают после постановки центральной венозной линии, обычно после перевода больного на ИВЛ. При операциях с применением ИК обязательным условием является наличие минимум двух венозных линий, так как часто возникает необходимость в применении симпатомиметиков и сосудорасширяющих препаратов. Затем производят пункцию a. radialis или a. dorsalis pedis для инвазивного контроля АД.
Практически при всех операциях на открытом сердце применяется управляемая гипотермия, глубина которой определяется тяжестью корригируемого порока сердца и длительностью ИК. Очень важно не допустить неуправляемого переохлаждения новорожденных и грудных детей, которое может привести к ацидозу и угнетению сердечно-сосудистой системы. Чем меньше ребенок, тем больше риск значительной интраоперационной потери тепла. Для профилактики этого осложнения применяют согревание и увлажнение вдыхаемой газовой смеси, согревание всех вводимых внутривенно жидкостей, используют водяные подогреваемые матрасы, специальные пластиковые пакеты, содержащие теплоемкую субстанцию. Температурный режим во время операции контролируют пищеводным носовым и ректальным температурными датчиками. Пищеводный датчик отражает центральную температуру тела, а носовой – периферическую. До начала ИК температура тела должна поддерживаться в пределах нормы. Согревающие устройства выключают в начале ИК, и охлаждение проводят с помощью теплообменника оксигенатора. Наружное охлаждение головы ребенка ледяной крошкой в период охлаждения применяют в случае, когда планируется операция с гипотермической остановкой ИК. Это наиболее эффективный способ защиты мозга от ишемии. Градиент температур крови и теплоносителя, как во время охлаждения, так и во время согревания больного не должен превышать 10 0С во избежание разрушения эритроцитов. В процессе согревания используют те же устройства, что и перед ИК. Оптимальным является градиент центральной и периферической температуры не более 2-5 0С, а после полного согревания больного – отсутствие такового. После операции для поддержания нормального температурного режима могут применяться специальные прикроватные обогреватели, повышение окружающей температуры воздуха и воздушные фены.
Инфузионная поддержка для каждого ребенка зависит от величины преднагрузки, которая определяется особенностями самого порока сердца и возрастом пациента.
Инфузионная тактика:
-
поддержание адекватной преднагрузки;
-
гемодилюцию для улучшения реологических свойств крови;
-
внутривенное введение лекарств;
-
восполнение кровопотери.
Показателем гемодинамической стабильности также является диурез, который во время основного наркоза должен быть не менее 0,5 мл/кг/ч, поэтому постановка мочевого катетера является неотъемлемой частью интраоперационного контроля при операциях на сердце и производится очень тщательно. Анестезиолог должен лично убедиться в проходимости мочевыводящих путей. Если на фоне стабильной гемодинамики и адекватной инфузионной терапии диурез недостаточен, можно применить маннитол или фуросемид.
Выбор переливаемого раствора до начала ИК также зависит от возраста ребенка. Так, избыточное количество декстрозы может привести к гипергликемии, особенно после операций с остановкой ИК. В то же время упорная гипергликемия после операций с ИК может быть признаком повреждения ЦНС, поэтому глюкозосодержащие растворы следует применять только у детей с высоким риском гипогликемии и у детей в возрасте младше 1 года. Использование 10% декстрозы и 0,25% NaCl у новорожденных и 5% декстрозы и 0,25% NaCl у детей в возрасте от 1 мес. до 1 года является наиболее приемлемой инфузионной тактикой. Детям старше 1 года желательно применять солевые растворы без глюкозы. Дополнительный объем жидкости для замещения потерь в третье пространство и незначительной кровопотери вводят с использованием раствора Рингера со скоростью 4 мл/кг/ч. Поддержание должного водного баланса расчитывают за каждый час голодания с учетом массы тела по формуле: 4 мл/кг на первые 10 кг + 2 мл/кг на вторые 10 кг + 1 мл/кг на каждый 1 кг свыше 20 кг. Рекомендуемый темп восполнения дефицита жидкости такой: за 1-й час операции вводится 50% объема недополученной за время голодания жидкости + расчетный объем часовой потребности + объем потерь за этот час. За 2-й и 3й час операции вводят по 25 % объема недополученной за время голодания жидкости + расчетный объем часовой потребности + объем потерь за это время.

Контроль газов крови, электролитов и биохимических параметров на протяжении операции проводят, как правило, в плановом порядке. Обычно первый анализ газов крови, электролитов и биохимических параметров производят сразу после интубации трахеи, когда выставлены соответствующие возрасту, массе тела и виду порока сердца параметры вентиляции. Контроль кислотно-щелочного состояния проводят до достижения его нормальных значений. После введения гепарина в дозе 300-400 ЕД/кг обязательным является контроль активированного времени свертывания или протромбинового индекса, а также КЩС. Только после лабораторного подтверждения ожидаемого эффекта от введения гепарина разрешается канюляция аорты, полых вен и начало ИК. Обычно рекомендуют дополнительное введение миорелаксантов в период канюляции магистральных сосудов, так как гемодилюция может снизить желаемый уровень миорелаксации.
Гиперцианотические приступы
Необходимо помнить, что у детей с тетрадой Фалло перед началом ИК может развиться вторичный цианотический криз вследствие повышения право-левого сброса через ДМЖП. В развитии этой острой гипоксемии лежат два основных механизма. Первый из них – это гипотензия вследствие снижения системного сосудистого сопротивления, которая способствует увеличению праволевого сброса крови и нарастанию артериальной гипоксемии. Этот механизм чаще всего срабатывает, когда среднее системное АД падает ниже 60 мм рт.ст. Стандартным лечением может быть применение болюсного введения препаратов а-адренергического ряда, например мезатона. У маленьких детей можно снять такой гиперцианотический криз путем нажатия на область брюшной аорты. Как профилактическое мероприятие в этой ситуации рекомендуется ранняя коррекция ацидоза, которому сопутствует депрессия миокарда. Вторым механизмом развития гиперцианотического эпизода является симпатомиметическая или прямая механическая стимуляция выводного тракта правого желудочка, которая приводит к его спазмированию. При этом мезатон, повышая системное сосудистое сопротивление и меняя направление сброса, может способствовать увеличению выброса крови через выводной тракт в легочную артерию. Более эффективным является применение в-адреноблокаторов, которые расслабляют выводной тракт правого желудочка. Препаратом выбора является эсмолол, так как при его применении быстрее наступает эффект, он быстрее метаболизируется и оказывает менее выраженное отрицательное инотропное действие на миокард.
Основной наркоз
Наиболее популярным среди внутривенных препаратов для анестезии является фентанил. Средняя доза 50-60 мгк/кг может быть увеличена в зависимости от длительности оперативного вмешательства. Как дополнительный компонент широко применяется кетамин в дозе 1-4 мг/кг внутривенно. Однако необходимо помнить, что при его использовании может повышаться ЛСС, особенно у пациентов с гипертензией малого круга кровообращения. Суфентанил в дозе 5-10 мкг/кг также используют как основной компонент наркоза. Гемодинамическая стабильность и снижение гормонального ответа на стресс такие же, как при введении фентанила. В педиатрической анестезии на фоне ингаляционного наркоза может также использоваться альфентанил. Морфин чаще применяют у взрослых. Необходимо помнить, что у пациентов с цианотическими пороками его применение опасно из-за снижения системного сосудистого сопротивления, которое усиливает право-левый сброс. Пропофол как наиболее управляемый гипнотик с минимальным депрессивным влиянием на миокард прекрасно заменил натрия тиопентал. Инфузия раствора пропофола с кетамином у детей в возрасте старше 3 лет позволяет снизить необходимую для адекватной аналгезии дозу фентанила до 15-20 мкг/кг на всю операцию.
Среди ингаляционных анестетиков предпочтение отдают галотану и изофлюрану. Основным неблагоприятным эффектом галотана является его дозозависимое в-блокирующее действие, которое может приводить к сердечно-сосудистому коллапсу у детей при скомпрометированном миокарде. Его угнетающий эффект на миокард больше выражен у новорожденных, чем у взрослых. Из-за повышения чувствительности миокарда к собственным катехоламинам и дозозависимой депрессии миокарда необходимо тщательно отслеживать дозировку галотанового наркоза. У детей с тяжелыми ВПС максимальная доза галотана не должна превышать 2 %. Изофлюран также используется как основной анестетик в хирургии ВПС. В отличие от галотана изофлюран вызывает дозозависимое угнетение миокарда, которое компенсируется увеличением ЧСС или предупреждается применением атропина в премедикации.
Выбор мышечных релаксантов при операции на сердце зависит от ее продолжительности и основывается на гемодинамическом эффекте и длительности действия препарата. У новорожденных еще незрелая нейромышечная передача, но, несмотря на это, чем младше ребенок, тем большая доза миорелаксанта необходима для поддержания адекватной релаксации. Наиболее распространенным среди деполяризирующих миорелаксантов является сукцинилхолин, вводимый внутривенно в дозе 1-2 мг/кг и внутримышечно в дозе 3-4 мг/кг. Однако его применение ограничено короткой продолжительностью действия, поэтому сукцинилхолин используют в основном во время интубации трахеи, так как эффект при его внутривенном введении наступает значительно быстрее, чем при введении недеполяризующих миорелаксантов. Его необходимо с осторожностью применять у новорожденных и детей младшего возраста, так как он вызывает значительное повышение уровня калия в плазме крови и может провоцировать тяжелую брадикардию, особенно при повторном введении. Сукцинилхолин рекомендуется вводить разбавленным до концентрации 0,5%. Среди недеполяризующих миорелаксантов наиболее широко применяются панкурониум и ардуан внутривенно в дозе 0,1 мг/кг. Продолжительность действия этих миорелаксантов – 30-45 мин. При их применении может наблюдаться незначительное увеличение ЧСС из-за ваголитического эффекта и облегчения атриовентрикулярной проводимости.
Искусственное кровообращение и постперфузионный период
Как только началось ИК, головной конец операционного стола необходимо приподнять, чтобы облегчить отток из бассейна верхней полой вены.
Существует прямая зависимость метаболизма от глубины гипотермии. Однако снижение температуры повышает вязкость крови, из-за чего ухудшается периферическая перфузия. Если возникает сомнение, истинное ли давление показывает периферическая линия контроля АД, необходимо сравнить ее показания с центральным давлением, прежде чем осуществлять какое-либо лечение. Среднее перфузионное давление можно поддерживать на уровне 30-80 мм рт.ст., чтобы сохранить адекватность почечного кровотока и предупредить развитие метаболического ацидоза. Адекватная перфузия не сопровождается постперфузионными неврологическими осложнениями и интеллектуальным дефицитом. Во время перфузии контроль газов крови, электролитов и биохимических параметров проводится соответственно установленному в лечебном учреждении протоколу. Через 5 мин после окончания ИК проверяют КЩС, гемоглобин, гематокрит и электролиты. Биохимические показатели и коагулограмму контролируют через 15-20 мин после нейтрализации гепарина протамином. В дальнейшем все исследования повторяют по мере необходимости, но обязательно при доставке больного в реанимационный зал и далее регулярно не реже чем 1 раз в 3-4 ч.
После завершения хирургической коррекции порока сердца и снятия зажима с аорты сердечная деятельность обычно восстанавливается спонтанно и нормализуется синусовый ритм. Иногда возникает необходимость в проведении электрической деполяризации. Если ЧСС не поднимается выше 90-100 ударов в 1 мин, электрокардиостимулятором навязывают ритм с частотой от 120 до 150 в 1 мин в зависимости от возрастной нормы. Искусственную вентиляцию легких возобновляют после герметизации левых отделов сердца. Инотропную поддержку нужно начинать в том случае, если систолическое давление и заполнении полостей сердца не превышает перфузионное давление. При этом больной должен быть согрет. Выбор инотропного средства может варьировать, но при правожелудочковой недостаточности предпочтение отдается амринону или изопротеренолу как препаратам, которые не только оказывают положительное инотропное действие, но и уменьшают ЛСС, снижая постнагрузку для правого желудочка. Возможно применение добутамина. Допамин – эффективный инотропный препарат при левожелудочковой недостаточности, особенно при снижении диуреза. При использовании лекарств с положительным инотропным эффектом очень важно нормализовать рН, так как их инотропная активность при метаболическом ацидозезначительно снижается. Детям с высокой легочной гипертензией и высоким периферическим сопротивлением рекомендуется назначение натрия нитропруссида, нитроглицерина. Какая бы комбинация инотропных препаратов и вазодилататоров не применялась, решающим для исхода операции является поддержка сердечного индекса выше 2 л/мин/м2.
Применение инотропных средств и вазодилататоров невозможно без соответствующего технического обеспечения, так как требуется очень точное введение расчетной дозы со скоростью в несколько микрограммов в 1 мин. Для новорожденных и детей младшего возраста имеет значение каждый миллилитр внутривенно введенной жидкости, поэтому растворы симпатомиметиков и сосудорасширяющих препаратов готовятся высококонцентрированными по номограммам и схемам.
При нормотермической перфузии аналгезия и мышечная релаксация продолжаются по обычной схеме. Дополнительные дозы анальгетиков вводят по необходимости. Возможно применение вазодилататоров. При температуре пациента во время ИК ниже 33 0С дозы наркотических анальгетиков и миорелаксантов могут быть снижены в зависимости от глубины гипотермии. Анестезию с использованием препаратов, которые обладают угнетающим действием на миокард, не следует применять до тех пор, пока не будет отключен АИК и не стабилизируется гемодинамика. Условия, которые необходимо учитывать при отлучении от ИК:
-
синусовый ритм с частотой, соответствующей возрасту, или устойчивый ответ на ЭКС;
-
отсутствие нарушений ритма;
-
восстановление ИВЛ – удостовериться в том, что пиковое давление на вдохе соответствует доперфузионному;
-
носоглоточная температура выше 34 0С, а температура в пищеводе выше 37 0С;
-
нормальный уровень электролитов;
-
нормальные показатели газов артериальной крови;
-
гематокрит выше 21%;
-
готовая для инфузии инотропная поддержка или применяется уже подобранный симпато- миметик;
-
дополнительно перепроверены датчики для инвазивного контроля АД, а также готовы линии для прямого измерения давлений в полостях сердца;
-
готовы для переливания в достаточном количестве препараты крови и её компоненты;
-
диурез 2-3 мл/кг/ч;
-
насыщение по пульсоксиметру 100%;
-
удалена одна из венозных канюль.
Постперфузионный период
После полной остановки ИК и удаления канюль из сердца проводят нейтрализацию гепарина протамина сульфатом. Протамин вводят медленно через периферическую венозную линию, так как при его инфузии образуется комплекс с кальцием, который может вызвать периферическую вазодилатацию, отрицательную инотропную реакцию и гипотензию. Применение кальция хлорида, который параллельно вводят в центральную венозную линию, является препаратом выбора для лечения гипотензии, вызванной протамином. Также необходимо помнить, что при введении протамина может возникнуть анафилактическая реакция, сопровождающаяся резким снижением АД, повышением ЛСС, бронхоспазмом и снижением насыщения крови кислородом. Поэтому анестезиолог должен быть готов к экстренному подключению АИК при возникновении такого осложнения. Желательно вводить тест-дозу прота- мина, когда аортальная канюля еще не извлечена.

Для обеспечения адекватного уровня послеоперационного гемостаза применения только протамина недостаточно, особенно у пациентов с «синими» пороками сердца, у которых уже до операции наблюдаются нарушения свертывающей системы, поэтому дополнительно применяют викасол, дицинон. Разведение факторов свертывания во время перфузии, разрушение тромбоцитов в АИК, их секвестрация в легких и селезенке, активация фибринолитической активности вследствие повреждения эндотелия сосудов усугубляют нарушения гемостаза после операции. Для восстановления факторов свертывающей системы и улучшения качества гемостаза применяют инфузию тромбоцитарной массы и свежезамороженной плазмы. Дополнительно рекомендуется применение ингибиторов фибринолиза и ингибиторов протеаз для снижения постперфузионной потери крови.
Для успешного послеоперационного ухода за пациентами с ВПС, которым была произведена реконструктивная или паллиативная операция, необходимы исчерпывающие знания:
-
точного анатомического диагноза врожденного порока;
-
патофизиологического действия порока на сердечно-сосудистую систему и другие органы до операции;
-
соматического состояния до операции и дооперационного лечения;
-
средств, примененных для анестезии в операционной;
-
деталей операции, включая продолжительность ИК и прекращения циркуляции, технические особенности, вероятность остаточных дефектов и неблагоприятных последствий, с которыми обычно сталкиваются после определенной операции;
-
интраоперационных осложнений и способов их коррекции;
-
данных, полученных при обследовании.
Кроме того, должна быть обеспечена готовность в отделении интенсивной терапии к приему пациента:
-
проверенные в работе аппараты ИВЛ, кардиомонитор, ЭКС, дефибриллятор, отсос, наборы интубационных трубок и ларингоскоп;
-
фармакологические препараты, включая инотропные, сосудорасширяющие, анестезирующие, седативные, мочегонные и противоаритмические средства, инфузионные среды, антимикробные препараты и парентеральное питание;
-
стерильные наборы для экстренных процедур.
К детскому кардиохирургическому ОИТ предъявляются особые требования. Необходимо, чтобы пациенты могли безопасно транспортироваться из операционной в пределах 5 мин. Доступ к кровати должен быть открытым и свободным со всех сторон и в то же время следует обеспечить возможность изоляции пациента. Детская сердечная интенсивная терапия требует не только стандартного оборудования и лабораторного обеспечения, но и дополнительного специализированного оборудования со следующими комплектующими:
-
термодилюционный компьютер для определения сердечного выброса;
-
кардиостимуляторы;
-
аппарат для эхокардиографии;
-
оборудование для экстракорпоральной мембранной оксигенации;
-
система подачи NO;
-
аппарат контрапульсации.
Прикроватные мониторы должны обеспечивать непрерывный контроль ЧСС, ЭКГ, АД инвазивно и неинвазивно, дополнительный контроль давления в легочной артерии, правом предсердии, в левом предсердии или другой центральной венозной линии, дыхательной функции и температуры тела. Мониторы должны иметь систему аварийной индикации с незамедлительным ответом при возникновении отклонений от заданных пределов. Каждый монитор должен быть связан с принтером так, чтобы копия ЭКГ или графические профили мониторируемых параметров могли быть интерпретированы. Обязательным является наличие возле каждого пациента устройства для непрерывного контроля насыщения артериальной крови кислородом. Должен быть доступен компьютер для определения сердечного выброса термодилюционным методом. Идеально, чтобы все мониторы были объединены в систему для сетевой индикации данных, их хранения и анализа.
Переход из операционной в ОИТ – время повышенного риска для пациентов, так как полная оценка их состояния не может быть выполнена из-за уменьшенного объема мониторинга. Для того чтобы снизить этот риск, реаниматолог, который будет принимать ребенка в ОИТ, должен ознакомиться с хирургическим планом и деталями операции на дооперационной конференции. Приблизительно за 30 мин до окончания операции он должен получить краткую информацию от анестезиолога о выполненной процедуре, состоянии гемодинамики, дыхательной системы, режиме лечения и любых важных осложнениях. Это время требуется для того, чтобы до прибытия пациента подготовить оборудование соответственно состоянию его в операционной. Если операция особенно трудная или происходят существенные изменения в хирургическом плане, реаниматологу полезно посетить операционную, чтобы обсудить технические проблемы или план лечения с анестезиологом и хирургом. Пациенты транспортируются анестезиологом вместе с хирургами при ручной ИВЛ с подачей 100% кислорода, постоянном контроле за насыщением артериальной крови и ЧСС.
По прибытии пациента в ОИТ главная цель – быстро подключить его к прикроватной контрольной аппаратуре и четко сообщить самые важные детали операции. Основное внимание должно быть направлено на обеспечение адекватного газообмена и оксигенации, непрерывного введения вазоактивных лекарств. Существенные детали операции включают: хирургическую процедуру, продолжительность ИК и прекращения циркуляции, любые замечания относительно качества защиты миокарда, восстановления его функции, системного артериального и внутрисердечного давлений после ИК, любые аритмии или проблемы с гемостазом. Рапорт должен включать информацию об особенностях дыхательной системы и параметрах ИВЛ, использованных анестезирующих средствах, функции почек и гемогидробалансе. Следует также обсудить использование аналгезирующих и седативных средств, нервно-мышечных релаксантов, длительность послеоперационной ИВЛ.

В листе наблюдения должны документироваться такие жизненные показатели, как температура, ЧСС и ритм, параметры ИВЛ или дыхания, величины АД, давления в полостях и насыщение по пульсоксиметру. Должен быть сделан расчет суточного объема внутривенных инфузий, исходя из площади поверхности тела пациента, оценка уровня диуреза и отделяемого по дренажным трубкам. Если отмечается чрезмерный уровень отделяемого по дренажам, с хирургом обсуждается необходимость реторакотомии после лабораторной оценки состояния коагуляции. Общая кровопотеря после операции, составляющая 10 мл/кг, является прямым показанием к реторакотомии. Если темп кровотечения высокий, реторакотомию необходимо предпринимать независимо от объема кровопотери. Очень важно поддерживать проходимость дренажных трубок, так как возможна тампонада сердца.
Обычно анестезиолог выставляет начальные параметры ИВЛ. Реаниматолог должен знать дыхательный режим и параметры настройки, чтобы оценить адекватность газового обмена и оксигенации в течение раннего послеоперационного периода. Детали проблем с верхними дыхательными путями или низкие дыхательные резервы также должны быть учтены.
Необходимо сравнить пред- и послеоперационные рентгенограммы грудной клетки, чтобы оценить изменения в размере и форме сердечной тени, изменения паренхимы, объемов легких, плевральных полостей, определить положение всех трубок, внутрисердечных и других катетеров, проводов при различных вариантах навязывания сердечного ритма. Положение трубок и зондов, которые неправильно установлены, должно быть откорректировано и проконтролировано рентгенограммой, чтобы оценить результат.
По ЭКГ документируют сердечный ритм и сравнивают его с дооперационным. Важно определить, какой ритм у пациента, так как при синусовом ритме с соответствующей функцией AV-узла сокращения предсердий способствуют более полному заполнению желудочков и увеличению сердечного выброса. В связи с этим при возникновении полной АV-блокады предпочтительнее навязывать двукамерную стимуляцию. ЭКГ должна быть оценена и для выявления ишемических расстройств.
Правильная интерпретация газов артериальной крови требует понимания послеоперационной сердечной анатомии и новых условий гемодинамики, особенно после паллиативных операций. Изменения параметров ИВЛ должны производиться с учетом необходимости обеспечить адекватную вентиляцию и оксигенацию на основании оценки клинического состояния пациента. Причина неожиданных изменений pH, рС02, или р02 должна быть установлена быстро и так же быстро произведена их коррекция. У пациента с физиологически откорригированным кровообращением при Fi02 100% Ра02 часто больше 300 мм рт.ст. Соответственно pH должно быть 7,34-7,45, а рС02 – 35-45 мм рт.ст. Напротив, у пациента с единственным желудочком, когда имеется смешивание артериальной и венозной крови, также должны быть нормальными pH и рС02, но р02 обычно меньше 55 мм рт.ст. В любом случае при смешивании артериальной и венозной крови даже 100% Fi02 не нормализует Ра02 из-за внутрисердечного шунтирования. Другими причинами уменьшения Ра02 могут быть внутрилегочное шунтирование или альвеолярная гиповентиляция. Пациенты с акроцианозом могут иметь нормальные значения Ра02. Их цианоз объясняется низким сердечным выбросом или полицитемией.
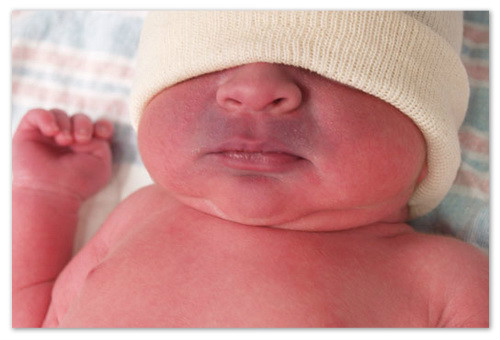
Если отмечается ацидоз или алкалоз, должна быть определена причина этого нарушения и произведено соответствующее вмешательство для коррекции. При метаболическом ацидозе в первую очередь должно быть заподозрено ухудшение функционального состояния сердца.
Определение уровней К+, №+, Сl-, ионизированного Са2+ и гемограммы завершает начальное послеоперационное исследование крови.
Все полученные данные объединяют, чтобы сформулировать вывод о состояния пациента и разработать план дальнейшего лечения.
Гемодинамический статус после операции зависит от ЧСС, внутрисосудистого объема, системного и легочного сосудистого сопротивления, сократимости миокарда и регулируется соответствующей лекарственной терапией.
Среднее давление в левом предсердии и ЦВД у пациентов после операций на сердце обычно выше нормы на 6-8 мм рт. ст., но при этом не должно превышать 12-14 мм рт. ст. Обычно среднее давление в левом предсердии на 1-2 мм рт.ст. выше, чем в правом предсердии, и изменяется вместе с дыханием. Причинами патологически высокого давления в левом предсердии могут быть:
-
повышенное конечно-диастолическое давление в желудочке;
-
сниженная системная систолическая или диастолическая функция желудочка;
-
гипертрофия желудочка;
-
перегрузка желудочка объемом;
-
стеноз митрального клапана с отсутствующим или ограниченным межпредсердным сбросом;
-
недостаточность митрального клапана;
-
миксома или тромб в левом предсердии;
-
большой право-левый шунт;
-
гипоплазия левого предсердия;
-
тампонада перикарда;
-
тахиаритмия;
-
попадание катетера в желудочек;
-
датчик давления выставлен ниже «нулевого» уровня, неправильно откалиброван или нерабочий.
Причинами патологически низкого давления в левом предсердии могут быть: низкий ОЦК; повреждение катетера; датчик давления расположен выше «нулевого» уровня, неправильно откалиброван или нерабочий.
Причины повышеного давления в правом предсердии: нарушение предсердно-желудочковой синхронизации, патология систолической или диастолической функции правого желудочка, гипертрофия правого желудочка; перегрузка правого желудочка объемом, нарушение функции трехстворчатого клапана; оставленный недостаточный межпредсердный шунт; тампонада перикарда; тахиаритмия; повреждение катетера; датчик давления расположен ниже «нулевого» уровня, неправильно откалиброван или нерабочий. Низкое давление в правом предсердии может быть из-за: низкого ОЦК, повреждения катетера, расположения датчика давления выше «нулевого» уровня или он нерабочий.
В норме давление в легочной артерии колеблется между 10 и 20 мм рт. ст. После операции оно часто больше, чем 13 мм рт. ст., но не должно превышать 25 мм рт. ст. Легочная гипертензия – частая причина правожелудочковой недостаточности.
Показатели газов крови в левом предсердии, правом предсердии и легочной артерии дополняют информацию о состоянии пациента и также важны для оптимального послеоперационного лечения. Поставленные в операционной катетеры для контроля внутрисердечных давлений и газов крови могут также использоваться для внутривенного переливания жидкостей, крови, инфузии лекарств и парентерального питания.
Послеоперационное восполнение жидкости и электролитов
У пациентов, прооперированных с использованием ИК, часто наблюдаются нарушения баланса жидкостей и равновесия электролитов. Гомеостаз и почечная функция также должны быть восстановлены после доставки в ОИТ. После операции в условиях ИК обычно имеется избыток жидкости в интерстициальном пространстве, особенно у новорожденных и младенцев, которые за время операции прибавляют в массе от 600 до 1000 г. Эта избыточная жидкость распределяется в мягких тканях, легких, почках, мозге и миокарде. Дополнительно к стимуляции диуреза применяют ультрафильтрацию во время ИК или перитонеальный диализ для быстрого удаления избытка жидкости.
После поступления в реанимационное отделение у большинства пациентов, которые подверглись операции в условиях ИК, диурез более 1 мл/кг/ч. Начальный период ускоренного мочеотделения — это осмотический диурез, который вызван гипергликемией или действием введенного во время операции маннитола. В первые 24 ч. внутривенную инфузию рассчитывают по площади поверхности тела или по методу суточного расхода: + 50 мл/кг/сут + 20 мл/кг/сут. Уровни глюкозы крови и электролитов в сыворотке должны быть исследованы в течение 1 ч после доставки пациента в ОИТ и затем каждые 4 ч в течение первых суток после операции. Электролиты рассчитывают, исходя из суточной потребности, и добавляют в переливаемые растворы с учетом уровня диуреза и лабораторных показателей.
При внутривенных инфузиях в первую очередь должно быть ограничено вливание натрия. Потребность в жидкости диктуется состоянием гемодинамики пациента и показаниями для переливания крови или коллоидных растворов. Водно-электролитный баланс оценивают не менее 1 раза в день. Необходимо учитывать объемы всех жидкостей, введенных и выведенных из организма по всем магистралям, включая забор крови для лабораторного контроля. Может быть полезным ежедневное измерение массы тела, но часто это трудно выполнить, особенно в раннем послеоперационном периоде.
Вид жидкости для внутривенной инфузии зависит от послеоперационного состояния пациента, гематокрита, качества гемостаза и типа продолжающихся потерь. Если гематокрит адекватен и отсутствует кровотечение, то предпочтение отдают кристаллоидам или коллоидным растворам с 5% глюкозой. Если пациент анемичен, но нет кровотечения, переливают отмытые эритроциты. При значительном кровотечении применяют эритроцитарную массу и свежезамороженную плазму, тромбоциты или криопреципитат в зависимости от показателей коагулограммы.
После операции обычно широко используют диуретики, особенно у пациентов с устойчивой гемодинамикой. Чаще всего применяют фуросемид болюсно или в виде постоянной инфузии, которая предпочтительна у пациентов с неустойчивой гемодинамикой. При недостаточном эффекте можно добавить второе мочегонное с иным местом действия на нефрон, например хлортиазид или осмотический диуретик. Маннитол следует использовать с осторожностью у пациентов с низким сердечным выбросом, при избыточной преднагрузке и сниженной почечной перфузии. Можно использовать и другую стратегию, чтобы повысить диурез – применить «почечные» дозы допамина.
Основные электролиты, уровень которых необходимо контролировать постоянно – это калий, кальций, магний, натрий и хлор.
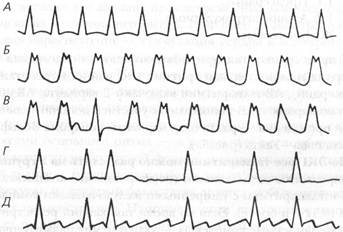
Гипокалиемия проявляется увеличением продолжительности потенциала действия и эффективного рефрактерного периода миокарда, уменьшением его автоматизма. На ЭКГ проявления гипокалиемии начинаются с выравнивания Г-волны или инверсии U-волн, может регистрироваться предсердная или чаще желудочковая аритмия, особенно при приеме дигоксина. Нормализации уровня K+ в сыворотке крови достигают путем внутривенной инфузии раствора KCl, которую следует проводить под контролем ЭКГ, так как этот процесс может иметь драматические последствия. Поэтому при внутривенной инфузии необходимо соблюдать следующие правила: дозу 0,5 мэкв/кг переливают более чем за 1 ч под непрерывным контролем ЭКГ; концентрация KCl в переливаемом растворе не должна превышать 0,25%. Концентрированные растворы следует вводить только в центральную венозную линию через дозатор.
Хотя с гиперкалиемией не сталкиваются так часто, как с гипокалиемией, она также может иметь угрожающие жизни последствия. Острая почечная недостаточность, метаболический алкалоз, краш-синдром, применение деполяризующих миорелаксантов и передозировка KCl – это основные причины гиперкалиемии. На ЭКГ она проявляется соответственно степени гиперкалиемии: высокая Г-волна, уменьшение амплитуды R-волны, расширение комплекса QRS, удлинение интервала PR, выравнивание или исчезновение P-волны и смешивание P- и QRS-волн. Если уровень K+ сыворотки больше, чем 8,0 мэкв/л, могут возникнуть фибрилляция желудочков и асистолия в диастоле.
Если уровень K+ сыворотки больше, чем 6,5 мэкв/л, и наблюдаются изменения на ЭКГ, необходимо произвести следующие действия:
-
внутривенную инъекцию кальция хлорида в течение нескольких минут через центральную венозную линию;
-
инфузию натрия бикарбоната 1-2 мэкв/кг в течение нескольких минут, чтобы создать алкалоз и перераспределить K+ в клетку;
-
ввести инсулин с глюкозой внутривенно в течение 15-30 мин;
-
ввести мочегонное средство;
-
приготовиться к гемодиализу или перитонеальному диализу у пациентов с почечной блокадой.
Адекватные уровни кальция являются необходимыми для нормальной сократительной функции миокарда, скелетных мышц и гладкой мускулатуры сосудов. Нормальный уровень кальция сыворотки крови – 1,14-1,30 ммоль/л. Ионизированный Ca2+ – мощный положительный инотропный агент, поэтому важно предотвращение существенной гипокальциемии. При Di George синдроме, переливании больших объемов цитратной крови, применении мочегонных средств, остром дыхательном алкалозе уменьшается уровень ионизированного Ca2+. Безотлагательность коррекции гипокальциемии зависит, прежде всего, от гемодинамического состояния пациента, и необходимость в ней возрастает, если уровень Ca2+ меньше 0,8-1,0 ммоль/л. Болюсно 10% кальция хлорид можно вводить в дозе 10 мг/кг внутривенно в центральную венозную линию. Для достижения нормального уровня можно использовать непрерывное вливание Ca2+, исходя из суточных потребностей и лабораторных данных.
У 81% детей в течение 5 дней после операций отмечается гипомагнезиемия, но лишь недавно стали уделять внимание уровню Mg2+ у послеоперационных пациентов. Физиологически активная форма Mg2+, как и Ca2+, ионизирована. Он влияет на аденозинтри- фосфатзависимые процессы, участвует в формировании электрического потенциала во время сокращения миоцита и регуляции сосудистого тонуса. Стандартное измерение уровня ионизированного Mg2+ большинству диагностических лабораторий еще недоступно, поэтому рекомендуется назначение MgSu4 в переливаемые растворы, исходя из суточных потребностей.
Экстубация
Решение об экстубации пациента, которому была произведена операция на открытом сердце, принимается индивидуально и базируется на показателях гемодинамики, дыхательных резервах, типе оперативного вмешательства, адекватности гемостаза и общего состояния. Наиболее благоприятной считается ранняя экстубация, но всегда необходимо помнить о вероятности повторного вмешательства в раннем послеоперационном периоде. В связи с этим ближайшие несколько часов после окончания оперативного вмешательства являются критическими. В этот период необходимо не только стабилизировать гемодинамику, состояние дыхательной системы, обеспечить адекватность гемостаза, т.е. критерии готовности к экстубации:
-
пробуждение и признаки сознания;
-
хороший мышечный тонус, давление на вдохе достигает 20 мм рт.ст.;
-
сердечный индекс выше 2 л/мин/м2 при минимальной инотропной поддержке;
-
РаО2 выше 150 мм рт.ст. при FiО2 < 50%;
-
ректальная температура выше 36 0С;
-
отделяемое по дренажам менее 1 мл/кг/ч;
-
адекватный диурез.

Для обезболивания в послеоперационном периоде применяют морфина сульфат в дозе 0,05 мг/кг внутримышечно каждые 4 ч новорожденным и младенцам; 20-40 мкг/кг/ч непрерывной инфузией, если ребенок находится на пролонгированной ИВЛ, и 10-15 мкг/кг/ч, если предполагается экстубация, а в дозе 0,1-0,2 мг/кг внутримышечно каждые 4 ч применяют детям старше 1 года. Фентанил используют у детей с неустойчивой гемодинамикой. Как седативный препарат широко используют диазепам в дозе 0,1-0,2 мг/кг каждые 2-4 ч. Возможно применение у-оксимасляной кислоты в дозе 25-50 мг/кг внутривенно. В качестве ненаркотических анальгетиков широко применяют парацетамол и диклофенак в виде сиропа.
- Аллергия
- Ангиология
- Болезни глаз
- Венерология
- Гастроэнтерология
- Гинекология
- Дерматология
- Здоровое питание
- Инфекционные болезни
- Кардиология
- Косметология
- Лекарства
- Лекарственные растения
- ЛОР-заболевания
- Мужское здоровье
- Неврология
- Неотложная помощь
- Новости
- Онкология
- Ортопедия
- Паразитология
- Педиатрия
- Пульмонология
- Расшифровка анализов
- Симптомы
- Системные заболевания
- Стоматология
- Травматология
- Урология
- Хирургия
- Эндокринология
- Нужно знать
- Еда
- Профессиональные заболевания








Комментарии